第43页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
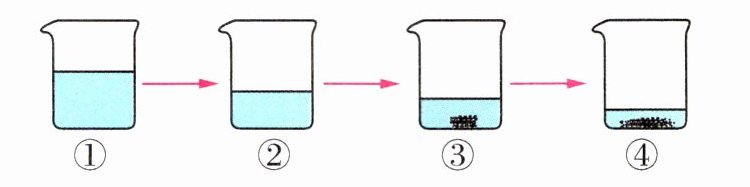
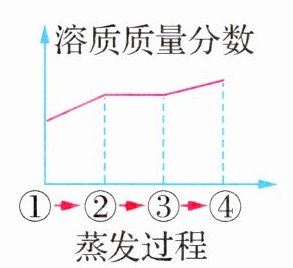
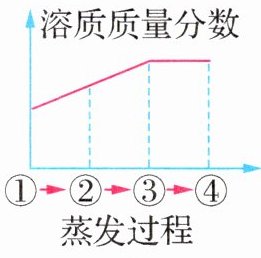
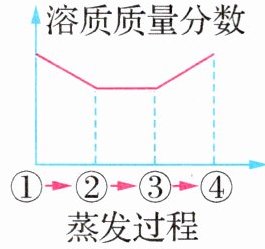
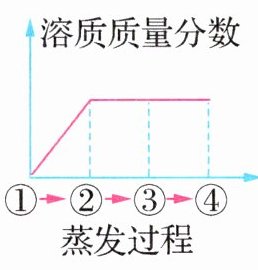
8.(2024·福建福州模拟)下图所示为蒸发氯化钠溶液的过程,其中①→②→③为恒温蒸发过程,③→④为升温蒸发过程,溶液②恰好为饱和状态,下列溶液质量分数与蒸发过程描述正确的是 ( )





答案:
A 【解析】在①→②过程中,氯化钠的溶解度不变,溶质质量分数变大,②与③都是同温度下的饱和溶液,所以溶质质量分数相等,③→④升温蒸发,此时溶解度变大,溶质的质量分数④>③,故A正确。
9. 亮点原创 北宋沈括所著的《梦溪笔谈》中记载了“湿法炼铜”,即在硫酸铜溶液中加入铁,可得到铜。小华同学在实验室模拟湿法炼铜。他取46.0 g铁片放入102 g硫酸铜溶液中,反应一段时间后,得到48.0 g固体。则所得溶液的溶质质量分数为 ( )
A. 28.0%
B. 37.2%
C. 38%
D. 45.0%
A. 28.0%
B. 37.2%
C. 38%
D. 45.0%
答案:
C 【解析】设反应生成硫酸亚铁的质量为x。
Fe + CuSO₄ = Cu + FeSO₄ 固体质量变化量
56 64 152 64 - 56 = 8
x 48.0 g - 46.0 g = 2.0 g
$\frac{152}{8}=\frac{x}{2.0\ g}$ x = 38 g
则所得溶液中溶质的质量分数为$\frac{38\ g}{46.0\ g + 102\ g - 48.0\ g}×100\% = 38\%$,故C正确。
10. 一定温度和压强下,乙腈(CH₃CN)是极易溶于水的无色液体,已知相同条件下质量分数为a₁的乙腈溶液的密度为d₁,水的密度为d₂,且d₁<d₂。若向质量分数为a₁的乙腈溶液中加入等体积的水,所得溶液中乙腈的质量分数为a₂。则下列说法正确的是 ( )
A. 0.5a₁>a₂
B. 0.5a₁<a₂
C. 0.5a₁=a₂
D. 无法确定
A. 0.5a₁>a₂
B. 0.5a₁<a₂
C. 0.5a₁=a₂
D. 无法确定
答案:
A 【解析】设乙腈溶液的体积和加入水的体积都为V,溶液混合后溶质的质量分数a₂ = $\frac{a_1Vd_1}{Vd_1 + Vd_2}×100\%$,则a₂ = a₁$\frac{d_1}{d_1 + d_2}$,又因为d₁<d₂,所以0.5a₁>a₂,故A正确。
11. 20 ℃时,取一定质量的固体硝酸钾于烧杯中,把100 g水平均分成四份依次加入烧杯中,不断搅拌,使之充分溶解,实验过程如下图所示。下列分析正确的是 ( )

A. 烧杯甲中,硝酸钾溶液是不饱和溶液
B. 烧杯丁中,硝酸钾溶液是不饱和溶液
C. 乙→丙过程中,硝酸钾溶液的溶质质量分数一定变大
D. 丙→丁过程中,硝酸钾溶液的溶质质量分数一定不变

A. 烧杯甲中,硝酸钾溶液是不饱和溶液
B. 烧杯丁中,硝酸钾溶液是不饱和溶液
C. 乙→丙过程中,硝酸钾溶液的溶质质量分数一定变大
D. 丙→丁过程中,硝酸钾溶液的溶质质量分数一定不变
答案:
B 【解析】由题图可知,20 ℃时,烧杯甲中还有未溶解的硝酸钾固体,所以烧杯甲中硝酸钾溶液是饱和溶液,故A错误;由题图可知,20 ℃时,烧杯丙中没有未溶解的硝酸钾固体,所以烧杯丙中硝酸钾溶液可能是饱和溶液,也可能是不饱和溶液,在此基础上继续加水得到烧杯丁中溶液,溶剂增多,烧杯丁中硝酸钾溶液是不饱和溶液,故B正确;烧杯乙中是硝酸钾的饱和溶液,乙→丙过程中,硝酸钾溶液的溶质质量分数不变或减小,故C错误;丙→丁过程中,继续加入溶剂,溶质质量不变,所以硝酸钾溶液的溶质质量分数减小,故D错误。
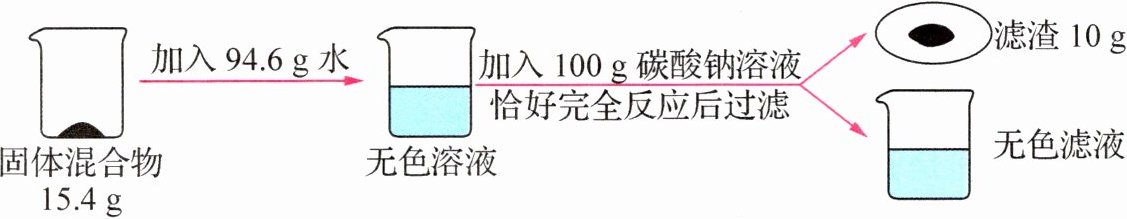
12.(2024·黑龙江齐齐哈尔)现有氯化钙和氯化钠的固体混合物,进行如下实验(已知CaCl₂+Na₂CO₃ ===CaCO₃↓+2NaCl,氯化钠与碳酸钠不反应)。
请计算:
(1)反应生成沉淀的质量是________g。
(2)恰好完全反应时,所得溶液中溶质的质量分数是多少(写出计算过程)?

请计算:
(1)反应生成沉淀的质量是________g。
(2)恰好完全反应时,所得溶液中溶质的质量分数是多少(写出计算过程)?
答案:
10@@解:设生成氯化钠的质量为x,原固体混合物中氯化钙的质量为y。
Na₂CO₃ + CaCl₂ = 2NaCl + CaCO₃↓
111 117 100
y x 10 g
$\frac{111}{100}=\frac{y}{10\ g}$ y = 11.1 g
$\frac{117}{100}=\frac{x}{10\ g}$ x = 11.7 g
所得溶液中溶质的质量分数为$\frac{15.4\ g - 11.1\ g + 11.7\ g}{15.4\ g + 94.6\ g + 100\ g - 10\ g}×100\% = 8\%$
答:所得溶液中溶质的质量分数是8%。
查看更多完整答案,请扫码查看


