第6页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
12. 金属及金属材料广泛用于生产、生活及科学实验中,金属材料的应用推动了社会的发展。
(1)四川三星堆遗址出土的青铜人面面具属于________材料。
(2)右图是出土的“金面具”,多年来光亮如初,是因为金的化学性质________(填“稳定”或“不稳定”),块状的黄金可以加工成薄片面具,说明金具有________性。
(3)向一定量的金属R中加入一定量稀硫酸,金属完全溶解,再向该溶液中加入铁粉,有气泡产生,则加入铁粉后产生气泡的化学方程式为______________________________。
(4)等质量的同一种稀硫酸分别与金属X、Y反应,产生气体的质量与金属质量变化的图象如右下图所示。下列说法正确的是________(填字母)。
A. $m_{1}$时,产生气体的质量:$X>Y$
B. 金属X比金属Y活泼
C. $m_{2}$时,消耗金属的质量:$X<Y$
D. $m_{2}$时,消耗稀硫酸的质量:$X = Y$
(1)四川三星堆遗址出土的青铜人面面具属于________材料。
(2)右图是出土的“金面具”,多年来光亮如初,是因为金的化学性质________(填“稳定”或“不稳定”),块状的黄金可以加工成薄片面具,说明金具有________性。

(3)向一定量的金属R中加入一定量稀硫酸,金属完全溶解,再向该溶液中加入铁粉,有气泡产生,则加入铁粉后产生气泡的化学方程式为______________________________。
(4)等质量的同一种稀硫酸分别与金属X、Y反应,产生气体的质量与金属质量变化的图象如右下图所示。下列说法正确的是________(填字母)。

A. $m_{1}$时,产生气体的质量:$X>Y$
B. 金属X比金属Y活泼
C. $m_{2}$时,消耗金属的质量:$X<Y$
D. $m_{2}$时,消耗稀硫酸的质量:$X = Y$
答案:
金属@@稳定@@延展@@Fe + H₂SO₄ = FeSO₄ + H₂↑@@ACD
13. (2023·江苏镇江期末)已知金属与$O_{2}$反应生成氧化物,向一定量铜、镁混合粉末中加入足量的稀硫酸,充分反应后过滤,将洗净的滤渣在$O_{2}$中充分灼烧。实验中固体质量的变化如下图所示。下列说法正确的是 ( )
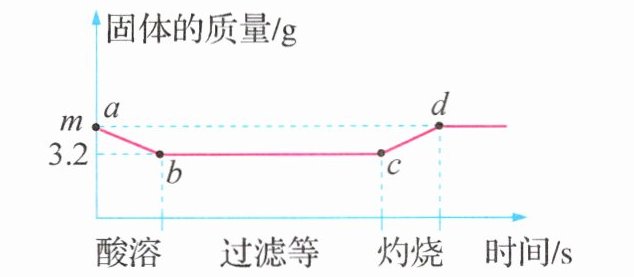
A. $a~b$段反应得到蓝色溶液
B. 混合物中铜、镁的质量比为4∶1
C. 酸溶过程放出0.025 g气体
D. $c~d$段上每个点的组成均为Cu和CuO

A. $a~b$段反应得到蓝色溶液
B. 混合物中铜、镁的质量比为4∶1
C. 酸溶过程放出0.025 g气体
D. $c~d$段上每个点的组成均为Cu和CuO
答案:
B 【解析】铜与稀硫酸不反应,开始加入稀硫酸只有镁与稀硫酸反应生成硫酸镁和氢气。因加入足量的稀硫酸,所以过滤后的固体只有铜。a~b段发生的是镁与稀硫酸的反应,铜不参加反应,所以溶液为无色,故A错误;铜与氧气在加热的条件下反应生成氧化铜,反应后固体的质量与开始时铜、镁混合粉末的质量相同,所以氧化铜中氧元素的质量与混合物中镁的质量相等,所以混合物中铜、镁的质量比为64 : 16 = 4 : 1,故B正确;由题图可知,铜的质量为3.2 g,铜与镁的质量比为4 : 1,则镁的质量为0.8 g,设生成氢气的质量为x。
Mg + H₂SO₄ = MgSO₄ + H₂↑
24 2
0.8 g x
$\frac{24}{2}=\frac{0.8 g}{x}$ x≈0.067 g,故C错误;c点还未与氧气反应,则固体中只有铜,d点之后固体质量不变,则d点铜完全反应,只有氧化铜,故D错误。
14. (2024·新疆昌吉模拟)从某废旧电子产品中可以提炼贵重金属并得到硫酸铜溶液。工艺流程如下图所示。
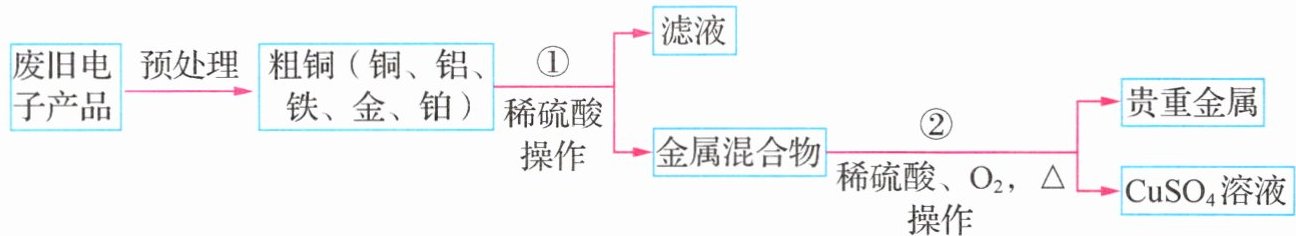
(1)图中“操作”的名称是________,该操作在实验室用到的玻璃仪器有烧杯、玻璃棒和________(填仪器名称)。
(2)流程①中发生反应的化学方程式为______________________(写出一个即可),该反应的基本反应类型为__________。流程①中滤液颜色是__________。
(3)通过流程②可以证明,铜与金相比活泼性较强的是________,贵重金属的成分是________和________。

(1)图中“操作”的名称是________,该操作在实验室用到的玻璃仪器有烧杯、玻璃棒和________(填仪器名称)。
(2)流程①中发生反应的化学方程式为______________________(写出一个即可),该反应的基本反应类型为__________。流程①中滤液颜色是__________。
(3)通过流程②可以证明,铜与金相比活泼性较强的是________,贵重金属的成分是________和________。
答案:
过滤@@漏斗@@2Al + 3H₂SO₄ = 3H₂↑ + Al₂(SO₄)₃(或Fe + H₂SO₄ = H₂↑ + FeSO₄)@@置换反应@@浅绿色@@铜(或Cu)@@金(或Au)@@铂(或Pt)
查看更多完整答案,请扫码查看


