2025年教材帮高中化学选择性必修第二册鲁科版
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2025年教材帮高中化学选择性必修第二册鲁科版 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
第80页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
考法 [新情境·“准液体”](2025湖北部分高中协作体期中)冰面为什么滑?这与冰层表面的结构有关(如图所示)。下列有关说法错误的是
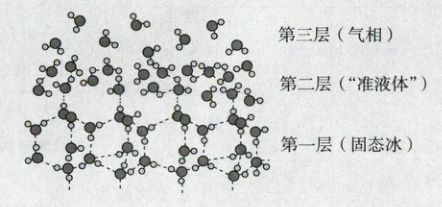
A.由于氢键的存在,水分子的稳定性好,高温下也很难分解
B.第一层固态冰中,水分子间通过氢键形成空间网状结构
C.第二层“准液体”中,水分子间形成氢键的机会比固态冰中少
D.当达到一定温度时,“准液体”中的水分子与下层固态冰中的水分子连接的氢键断裂,产生“流动性的水分子”,使冰面变滑

A.由于氢键的存在,水分子的稳定性好,高温下也很难分解
B.第一层固态冰中,水分子间通过氢键形成空间网状结构
C.第二层“准液体”中,水分子间形成氢键的机会比固态冰中少
D.当达到一定温度时,“准液体”中的水分子与下层固态冰中的水分子连接的氢键断裂,产生“流动性的水分子”,使冰面变滑
答案:
A
解析 水分子的稳定性好,是由于水分子中H—O键的键能较大,与水分子间形成的氢键无关,A项错误;固态冰中,1个水分子与周围的4个水分子通过氢键相连接,从而形成空间网状结构,B项正确;“准液体”中,水分子间的距离不完全相等,1个水分子与少于4个间距适合的水分子形成氢键,形成氢键的机会比固态冰中少,C项正确;当达到一定温度时,“准液体”中的水分子与下层固态冰中的水分子连接的氢键被破坏,使一部分水分子能够自由流动,从而产生“流动性的水分子”,使冰面变滑,D项正确。
答案 A
解析 水分子的稳定性好,是由于水分子中H—O键的键能较大,与水分子间形成的氢键无关,A项错误;固态冰中,1个水分子与周围的4个水分子通过氢键相连接,从而形成空间网状结构,B项正确;“准液体”中,水分子间的距离不完全相等,1个水分子与少于4个间距适合的水分子形成氢键,形成氢键的机会比固态冰中少,C项正确;当达到一定温度时,“准液体”中的水分子与下层固态冰中的水分子连接的氢键被破坏,使一部分水分子能够自由流动,从而产生“流动性的水分子”,使冰面变滑,D项正确。
答案 A
例7 根据表1和表2数据,回答问题:
表1 ⅤA、ⅥA、ⅦA族元素简单氢化物的沸点

表2 常见物质的沸点

(1)表1中a的范围是。
(2)根据表1数据,同主族元素简单氢化物的沸点的变化规律是。
(3)根据表2数据找规律,由②③⑥得出:;由③④得出:。
表1 ⅤA、ⅥA、ⅦA族元素简单氢化物的沸点

表2 常见物质的沸点

(1)表1中a的范围是。
(2)根据表1数据,同主族元素简单氢化物的沸点的变化规律是。
(3)根据表2数据找规律,由②③⑥得出:;由③④得出:。
答案:
(1)$a > -62$
(2)不存在氢键时,同主族元素简单氢化物的沸点随相对分子质量的增大而升高,如果存在氢键,该氢化物沸点反常得高
(3)结构和组成相似的分子,相对分子质量越大,范德华力越大,沸点越高;分子间存在氢键,会使其沸点升高,且分子间氢键越多,沸点越高
(2)不存在氢键时,同主族元素简单氢化物的沸点随相对分子质量的增大而升高,如果存在氢键,该氢化物沸点反常得高
(3)结构和组成相似的分子,相对分子质量越大,范德华力越大,沸点越高;分子间存在氢键,会使其沸点升高,且分子间氢键越多,沸点越高
查看更多完整答案,请扫码查看


