2025年教材帮高中化学选择性必修第二册鲁科版
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2025年教材帮高中化学选择性必修第二册鲁科版 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
第74页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
例16[新考法·模块融合|热重曲线+配合物结构](2025河南卷)自旋交叉化合物在分子开关、信息存储等方面具有潜在的应用价值。某自旋交叉化合物的结构及在氦气气氛下的热重曲线分别如图1和图2所示。该化合物的相对分子质量$M_r=870 + 32x$($x$为整数)。
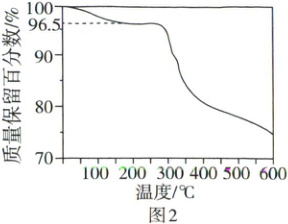
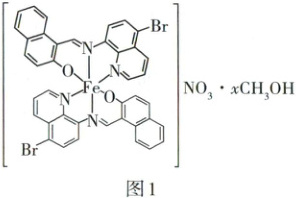
下列说法正确的是
A.$x = 1$
B.第一电离能:$ C< N< O$
C.该化合物中不存在离子键
D.该化合物中配位数与配体个数相等


下列说法正确的是
A.$x = 1$
B.第一电离能:$ C< N< O$
C.该化合物中不存在离子键
D.该化合物中配位数与配体个数相等
答案:
A
解析▶A项:固体开始失去的为$ CH_3 OH$,根据热重曲线,失去$ CH_3 OH$后剩余物质的质量保留百分数为$96.5\%$,则根据该化合物的相对分子质量$M_r = 870 + 32x$($x$为整数)可得:$\frac{870}{870 + 32x}=96.5\%$,解得$x = 1(\surd)$。
B项:随原子序数递增,同周期主族元素第一电离能整体呈增大趋势,但由于N元素2p轨道为半充满的较稳定状态,故其第一电离能大于同周期相邻元素的第一电离能,因此第一电离能:$ C< O< N(×)$。
C项:由该化合物的结构可知,化合物中存在$ NO_3^-$,即该化合物中存在离子键$(×)$。
D项:由该化合物的结构可知,该化合物中的配体有2个,与Fe配位的原子为4个N和2个O,即配位数为6,因此该化合物中配位数与配体个数不相等$(×)$。
答案▶A
解析▶A项:固体开始失去的为$ CH_3 OH$,根据热重曲线,失去$ CH_3 OH$后剩余物质的质量保留百分数为$96.5\%$,则根据该化合物的相对分子质量$M_r = 870 + 32x$($x$为整数)可得:$\frac{870}{870 + 32x}=96.5\%$,解得$x = 1(\surd)$。
B项:随原子序数递增,同周期主族元素第一电离能整体呈增大趋势,但由于N元素2p轨道为半充满的较稳定状态,故其第一电离能大于同周期相邻元素的第一电离能,因此第一电离能:$ C< O< N(×)$。
C项:由该化合物的结构可知,化合物中存在$ NO_3^-$,即该化合物中存在离子键$(×)$。
D项:由该化合物的结构可知,该化合物中的配体有2个,与Fe配位的原子为4个N和2个O,即配位数为6,因此该化合物中配位数与配体个数不相等$(×)$。
答案▶A
例17(高考组合)(1)(山东卷)含有多个配位原子的配体与同一中心离子(或原子)通过螯合配位成环而形成的配合物为螯合物。一种$ Cd^{2+}$配合物的结构如图所示,1 mol该配合物中通过螯合作用形成的配位键有
【链教材】来源于教材P83多齿配体、螯合物
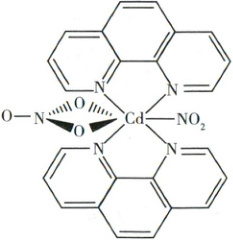
(2)[新角度·根据信息推断配位原子](2025山东卷)尿素分子($ H_2 NCONH_2$)与$ Fe^{3+}$形成配离子的硝酸盐$[ Fe( H_2 NCONH_2)_6]( NO_3)_3$俗称尿素铁,既可作铁肥,又可作缓释氮肥。八面体配离子$[ Fe( H_2 NCONH_2)_6]^{3+}$中$ Fe^{3+}$的配位数为6,碳氮键的键长均相等,则与$ Fe^{3+}$配位的原子是
6
mol,该螯合物中N的杂化方式有1
种。【链教材】来源于教材P83多齿配体、螯合物

(2)[新角度·根据信息推断配位原子](2025山东卷)尿素分子($ H_2 NCONH_2$)与$ Fe^{3+}$形成配离子的硝酸盐$[ Fe( H_2 NCONH_2)_6]( NO_3)_3$俗称尿素铁,既可作铁肥,又可作缓释氮肥。八面体配离子$[ Fe( H_2 NCONH_2)_6]^{3+}$中$ Fe^{3+}$的配位数为6,碳氮键的键长均相等,则与$ Fe^{3+}$配位的原子是
O
(填元素符号)。
答案:
(1)6 1
(2)O
解析▶
(1)该螯合物中$ Cd^{2+}$与杂环中的4个N原子及$ NO_3^-$中的2个O原子通过螯合作用形成配位键,故1 mol该配合物中通过螯合作用形成6 mol配位键。该螯合物中N原子均为$sp^2$杂化,即N只有1种杂化方式。
(2)八面体配离子$[ Fe( H_2 NCONH_2)_6]^{3+}$中$ Fe^{3+}$的配位数为6,则形成6个配位键,$ H_2 NCONH_2$中O和N上有孤对电子,能与$ Fe^{3+}$形成配位键,由碳氮键的键长均相等,知配位原子不能是N,故与$ Fe^{3+}$配位的原子是O。
答案▶
(1)6 1
(2)O
(1)6 1
(2)O
解析▶
(1)该螯合物中$ Cd^{2+}$与杂环中的4个N原子及$ NO_3^-$中的2个O原子通过螯合作用形成配位键,故1 mol该配合物中通过螯合作用形成6 mol配位键。该螯合物中N原子均为$sp^2$杂化,即N只有1种杂化方式。
(2)八面体配离子$[ Fe( H_2 NCONH_2)_6]^{3+}$中$ Fe^{3+}$的配位数为6,则形成6个配位键,$ H_2 NCONH_2$中O和N上有孤对电子,能与$ Fe^{3+}$形成配位键,由碳氮键的键长均相等,知配位原子不能是N,故与$ Fe^{3+}$配位的原子是O。
答案▶
(1)6 1
(2)O
查看更多完整答案,请扫码查看


