2025年教材帮高中化学选择性必修第二册鲁科版
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2025年教材帮高中化学选择性必修第二册鲁科版 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
第4页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
例2-6下列说法正确的是
①M层可以有s、p、d、f能级;
②$3p_x$表示有3个$p_x$轨道;
③3d能级最多容纳5个电子;
④无论哪一电子层的s能级最多容纳的电子数均为2个;
⑤第三电子层最多容纳8个电子;
⑥在一个原子中,不可能出现运动状态完全相同的2个电子。
A.①③
B.②④
C.⑤⑥
D.④⑥
①M层可以有s、p、d、f能级;
②$3p_x$表示有3个$p_x$轨道;
③3d能级最多容纳5个电子;
④无论哪一电子层的s能级最多容纳的电子数均为2个;
⑤第三电子层最多容纳8个电子;
⑥在一个原子中,不可能出现运动状态完全相同的2个电子。
A.①③
B.②④
C.⑤⑥
D.④⑥
答案:
D
解析 ▶M层有s、p、d3个能级,没有f能级,①错误;$3p_x$表示第三电子层的$p_x$轨道,②错误;以s、p、d、f……排序的各能级所能容纳的最多电子数依次为2、6、10、14……的2倍,即d能级最多容纳的电子数是10,③错误;不同电子层的相同类别的能级最多容纳的电子数相同,s能级最多容纳的电子数是2,④正确;每一电子层最多容纳的电子数为$2n^2$,第三电子层最多容纳18个电子,⑤错误;同一原子轨道最多填充2个自旋状态不同的电子,故在一个原子中,不可能出现运动状态完全相同的2个电子,⑥正确。
答案 ▶D
解析 ▶M层有s、p、d3个能级,没有f能级,①错误;$3p_x$表示第三电子层的$p_x$轨道,②错误;以s、p、d、f……排序的各能级所能容纳的最多电子数依次为2、6、10、14……的2倍,即d能级最多容纳的电子数是10,③错误;不同电子层的相同类别的能级最多容纳的电子数相同,s能级最多容纳的电子数是2,④正确;每一电子层最多容纳的电子数为$2n^2$,第三电子层最多容纳18个电子,⑤错误;同一原子轨道最多填充2个自旋状态不同的电子,故在一个原子中,不可能出现运动状态完全相同的2个电子,⑥正确。
答案 ▶D
例2-7(四川成都测试)如图所示是某原子核外第二电子层的原子轨道示意图。
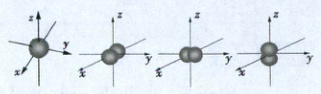
回答下列问题:
(1)请从左到右依次填写对应的原子轨道符号
(2)1个原子轨道最多容纳的电子数是
(3)s轨道、p轨道的半径与

回答下列问题:
(1)请从左到右依次填写对应的原子轨道符号
$2s$、$2p_x$、$2p_y$、$2p_z$
;比较各原子轨道能量的高低$2p_x=2p_y=2p_z>2s$
(按由高到低顺序)。(2)1个原子轨道最多容纳的电子数是
2
,第2电子层最多容纳的电子数是8
。(3)s轨道、p轨道的半径与
电子层序数
有关,规律是电子层序数越大,原子轨道的半径越大
。
答案:
(1)$2s$、$2p_x$、$2p_y$、$2p_z$ $2p_x=2p_y=2p_z>2s$
(2)2 8
(3)电子层序数 电子层序数越大,原子轨道的半径越大
解析 ▶s轨道只有1个原子轨道;p轨道有3个伸展方向,即有$p_x$、$p_y$、$p_z$3个原子轨道。s轨道、p轨道的半径与电子层序数有关;电子层序数越大,原子轨道的半径越大。
答案 ▶
(1)$2s$、$2p_x$、$2p_y$、$2p_z$ $2p_x=2p_y=2p_z>2s$
(2)2 8
(3)电子层序数 电子层序数越大,原子轨道的半径越大
(1)$2s$、$2p_x$、$2p_y$、$2p_z$ $2p_x=2p_y=2p_z>2s$
(2)2 8
(3)电子层序数 电子层序数越大,原子轨道的半径越大
解析 ▶s轨道只有1个原子轨道;p轨道有3个伸展方向,即有$p_x$、$p_y$、$p_z$3个原子轨道。s轨道、p轨道的半径与电子层序数有关;电子层序数越大,原子轨道的半径越大。
答案 ▶
(1)$2s$、$2p_x$、$2p_y$、$2p_z$ $2p_x=2p_y=2p_z>2s$
(2)2 8
(3)电子层序数 电子层序数越大,原子轨道的半径越大
查看更多完整答案,请扫码查看


