2025年教材帮高中化学选择性必修第二册鲁科版
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2025年教材帮高中化学选择性必修第二册鲁科版 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
第29页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
例18 (江苏卷)前4周期主族元素X、Y、Z、W的原子序数依次增大,X是空气中含量最多的元素,Y的周期序数与族序数相等,基态时Z原子3p原子轨道上有5个电子,W与Z处于同一主族。下列说法正确的是
A.原子半径:r(X)<r(Y)<r(Z)<r(W)
B.X的第一电离能比同周期相邻元素的大
C.Y的最高价氧化物对应水化物的酸性比Z的强
D.Z的简单气态氢化物的热稳定性比W的弱
A.原子半径:r(X)<r(Y)<r(Z)<r(W)
B.X的第一电离能比同周期相邻元素的大
C.Y的最高价氧化物对应水化物的酸性比Z的强
D.Z的简单气态氢化物的热稳定性比W的弱
答案:
解析 图示析题·思路具象化
N的2p轨道处于半充满状态,第一电离能C<O<N,B项正确
X是空气中含量最多的元素
X为N
原子半径Al>Cl,最高价氧化物对应水化物酸性HClO₄>Al(OH)₃,A、C项错误
Y的周期序数与族序数相等,原子序数X<Y<Z
Y为Al
基态时Z原子3p原子轨道上有5个电子
Z为Cl
非金属性Cl>Br,热稳定性HCl>HBr,D项错误
W与Z处于同一主族
W为Br
前4周期主族元素原子序数X<Y<Z<W
答案 B

解析 图示析题·思路具象化
N的2p轨道处于半充满状态,第一电离能C<O<N,B项正确
X是空气中含量最多的元素
X为N
原子半径Al>Cl,最高价氧化物对应水化物酸性HClO₄>Al(OH)₃,A、C项错误
Y的周期序数与族序数相等,原子序数X<Y<Z
Y为Al
基态时Z原子3p原子轨道上有5个电子
Z为Cl
非金属性Cl>Br,热稳定性HCl>HBr,D项错误
W与Z处于同一主族
W为Br
前4周期主族元素原子序数X<Y<Z<W
答案 B


6. [变角度](2024湖北卷)主族元素W、X、Y、Z原子序数依次增大,X、Y的价电子数相等,Z的价电子所在能层有16个轨道,4种元素形成的化合物如图。下列说法正确的是
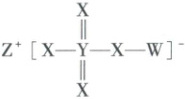
A.电负性:W>Y
B.酸性:W₂YX₃>W₂YX₄
C.基态原子的未成对电子数:W>X
D.氧化物溶于水所得溶液的pH:Z>Y
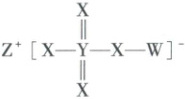
A.电负性:W>Y
B.酸性:W₂YX₃>W₂YX₄
C.基态原子的未成对电子数:W>X
D.氧化物溶于水所得溶液的pH:Z>Y
答案:
6.D Z的价电子所在能层有16个轨道,故Z为第4周期元素,结合题给化合物的结构图可知,Z为K元素;W、X、Y、Z原子序数依次增大,X、Y的价电子数相等,结合题给结构图可知,X为O元素、Y为S元素;W形成一个共价键,则W为H元素。电负性:H<S,A项错误;H₂SO₃为弱酸,故酸性:H₂SO₃<H₂SO₄,B项错误;基态H原子中未成对电子数为1,基态O原子中未成对电子数为2,C项错误;K的氧化物溶于水可产生KOH,溶液pH>7,S的氧化物溶于水生成H₂SO₃或H₂SO₄,溶液pH<7,D项正确。
7. [新考法·第二电离能的比较](2025河北卷改编)W、X、Y、Z为四种短周期非金属元素,W原子中电子排布已充满的能级数与最高能级数中的电子数相等,X与W同族,Y与X相邻且Y原子比X原子多一个未成对电子,Z位于W的对角线位置。下列说法错误的是 (
A.第二电离能:X<Y
B.原子半径:Z<W
C.单质沸点:Y<W
D.电负性:W<X
A
)A.第二电离能:X<Y
B.原子半径:Z<W
C.单质沸点:Y<W
D.电负性:W<X
答案:
7.A W、X、Y、Z为四种短周期非金属元素,W原子中电子排布已充满的能级数与最高能级中的电子数相等,则基态W原子的核外电子排布式为1s²2s²2p²(C)或1s²2s²2p⁶3s²3p⁴(S),X与W同族,若W为C,则X为Si,Y与X相邻且Y原子比X原子多一个未成对电子,则Y为P,根据Z位于W的对角线位置可知,W不可能为C,故W为S,则X为O,Y为N,Z为F。基态X(O)原子失去一个电子后核外电子排布式为1s²2s²2p³,基态Y(N)原子失去一个电子后核外电子排布式为1s²2s²2p²,基态O原子失去一个电子后2p能级为半充满的稳定结构,则第二电离能:O>N,A项错误;同主族元素从上到下,原子半径逐渐增大,故原子半径:O<S,同周期主族元素从左到右,原子半径逐渐减小,故原子半径:F<O,故原子半径:F<S,B项正确;Y对应的单质为N₂,W对应的单质为S,常温下,N₂为气体,S为固体,故沸点:N₂<S,C项正确;同主族元素从上到下,电负性逐渐减小,故电负性:O>S,D项正确。
查看更多完整答案,请扫码查看


