第91页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
- 第107页
- 第108页
- 第109页
- 第110页
- 第111页
- 第112页
- 第113页
- 第114页
- 第115页
- 第116页
- 第117页
- 第118页
- 第119页
- 第120页
- 第121页
- 第122页
- 第123页
- 第124页
- 第125页
- 第126页
- 第127页
- 第128页
- 第129页
- 第130页
- 第131页
- 第132页
- 第133页
- 第134页
- 第135页
- 第136页
- 第137页
- 第138页
- 第139页
- 第140页
- 第141页
20.(10分)某学习兴趣小组开展“制作‘蓝宝石’(硫酸铜晶体)”的实践活动,查得硫酸铜的溶解度曲线如图所示。
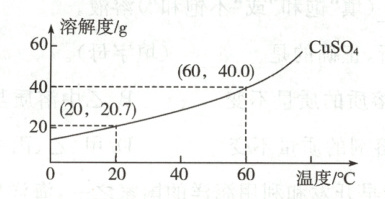
(1)制备$60^{\circ}C$的硫酸铜饱和溶液。用和胶头滴管量取$100mL$蒸馏水,用天平称取g硫酸铜,将硫酸铜溶于蒸馏水中,配制成$60^{\circ}C$的硫酸铜饱和溶液。
(2)制作晶核。将上述$60^{\circ}C$的硫酸铜饱和溶液用硬纸片盖好,静置一夜(忽略水分变化),选取溶液中出现的一个较完整的小晶体作晶核。
①制作晶核的这种方法称为(填“蒸发”或“降温”)结晶法。
②结合硫酸铜溶解度曲线解释采用该方法的原理是。
(3)获得“蓝宝石”。将晶核用丝线绑住,完全浸没在重新配制好的$60^{\circ}C$的硫酸铜饱和溶液中,用硬纸片盖好,静置,一段时间后可获得“长大”的美丽“蓝宝石”。
①若获得“蓝宝石”后的剩余溶液温度为$20^{\circ}C$,则此时溶液的溶质质量分数为(列出计算式即可,不用算出结果)。
②“蓝宝石”的成分为$CuSO_4·5H_2O$,其相对分子质量为250,“蓝宝石”中铜元素的质量分数为%。

(1)制备$60^{\circ}C$的硫酸铜饱和溶液。用和胶头滴管量取$100mL$蒸馏水,用天平称取g硫酸铜,将硫酸铜溶于蒸馏水中,配制成$60^{\circ}C$的硫酸铜饱和溶液。
(2)制作晶核。将上述$60^{\circ}C$的硫酸铜饱和溶液用硬纸片盖好,静置一夜(忽略水分变化),选取溶液中出现的一个较完整的小晶体作晶核。
①制作晶核的这种方法称为(填“蒸发”或“降温”)结晶法。
②结合硫酸铜溶解度曲线解释采用该方法的原理是。
(3)获得“蓝宝石”。将晶核用丝线绑住,完全浸没在重新配制好的$60^{\circ}C$的硫酸铜饱和溶液中,用硬纸片盖好,静置,一段时间后可获得“长大”的美丽“蓝宝石”。
①若获得“蓝宝石”后的剩余溶液温度为$20^{\circ}C$,则此时溶液的溶质质量分数为(列出计算式即可,不用算出结果)。
②“蓝宝石”的成分为$CuSO_4·5H_2O$,其相对分子质量为250,“蓝宝石”中铜元素的质量分数为%。
答案:
(1)量筒;40.0
(2)①降温;②硫酸铜的溶解度随温度降低而减小,饱和溶液降温后析出晶体
(3)①(20.7/(100+20.7))×100%;②25.6
(1)量筒;40.0
(2)①降温;②硫酸铜的溶解度随温度降低而减小,饱和溶液降温后析出晶体
(3)①(20.7/(100+20.7))×100%;②25.6
21.(14分)为了研究物质的溶解现象,进行以下探究活动。
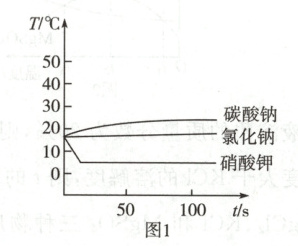
探究Ⅰ:将足量的碳酸钠、氯化钠和硝酸钾三种物质分别溶解在一定量的水中,溶解过程中温度变化如图1所示。
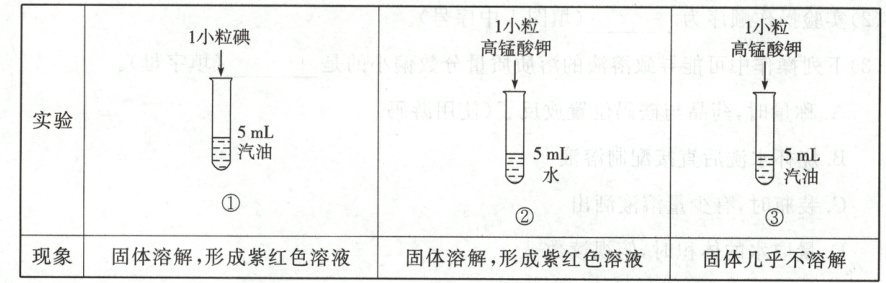
探究Ⅱ:
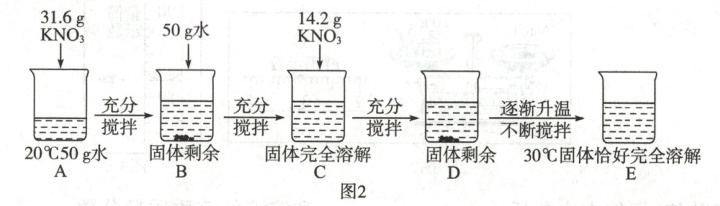
探究Ⅲ:探究过程如图2所示。
回答下列问题:
(1)探究Ⅰ中,溶解过程放出热量的物质是。
(2)对探究Ⅱ中实验现象进行分析,需要做的对比是,分析得出的结论之一是。
(3)探究Ⅲ中,所得溶液一定属于饱和溶液的是。通过该探究得出的结论是(答一点即可)。
(4)在上述探究的基础上,同学们想探究比较食盐和氯化铵在水中的溶解度大小,探究方案应该是。
探究Ⅰ:将足量的碳酸钠、氯化钠和硝酸钾三种物质分别溶解在一定量的水中,溶解过程中温度变化如图1所示。

探究Ⅱ:

探究Ⅲ:探究过程如图2所示。

回答下列问题:
(1)探究Ⅰ中,溶解过程放出热量的物质是。
(2)对探究Ⅱ中实验现象进行分析,需要做的对比是,分析得出的结论之一是。
(3)探究Ⅲ中,所得溶液一定属于饱和溶液的是。通过该探究得出的结论是(答一点即可)。
(4)在上述探究的基础上,同学们想探究比较食盐和氯化铵在水中的溶解度大小,探究方案应该是。
答案:
21.【实验内容与过程】6 94
【实验提示】减少左侧药品的质量,直至天平平衡
【实验说明与解释】大 加快溶解的速率
【实验提示】减少左侧药品的质量,直至天平平衡
【实验说明与解释】大 加快溶解的速率
查看更多完整答案,请扫码查看


