第106页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
- 第107页
- 第108页
- 第109页
- 第110页
- 第111页
- 第112页
- 第113页
- 第114页
- 第115页
- 第116页
- 第117页
- 第118页
- 第119页
- 第120页
- 第121页
- 第122页
- 第123页
- 第124页
- 第125页
- 第126页
- 第127页
- 第128页
- 第129页
- 第130页
- 第131页
- 第132页
- 第133页
- 第134页
- 第135页
- 第136页
- 第137页
- 第138页
- 第139页
- 第140页
- 第141页
19.(11分)(2024·晋中·三模)为探究酸能否与碱发生反应,并认识其微观实质,化学兴趣小组设计了下图实验。
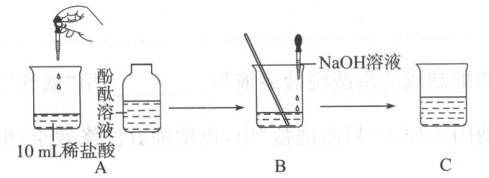
实验方法:在烧杯中加入10 mL稀盐酸,滴入几滴酚酞溶液,再用胶头滴管慢慢滴入足量的氢氧化钠溶液。
(1)实验原理:装置B中发生反应的化学方程式为。
(2)实验现象:装置B中观察到的现象是。
(3)实验结论:。
【问题与思考】
(4)该实验操作存在的问题是。
(5)装置C烧杯溶液中溶质(除酚酞外)为。

实验方法:在烧杯中加入10 mL稀盐酸,滴入几滴酚酞溶液,再用胶头滴管慢慢滴入足量的氢氧化钠溶液。
(1)实验原理:装置B中发生反应的化学方程式为。
(2)实验现象:装置B中观察到的现象是。
(3)实验结论:。
【问题与思考】
(4)该实验操作存在的问题是。
(5)装置C烧杯溶液中溶质(除酚酞外)为。
答案:
24.
(1)$2HCl + CaCO_3 \longrightarrow CaCl_2 + H_2O + CO_2 \uparrow$
(2)$2HCl + Ca(OH)_2 \longrightarrow CaCl_2 + 2H_2O$ 取少量白色固体于试管中,加入适量的水,充分振荡后加入1~2滴无色酚酞溶液(或取少量白色固体于试管中,加入适量的水,充分振荡后加入1~2滴紫色石蕊溶液) 浊液变红(或浊液变蓝)
(3)密封
(1)$2HCl + CaCO_3 \longrightarrow CaCl_2 + H_2O + CO_2 \uparrow$
(2)$2HCl + Ca(OH)_2 \longrightarrow CaCl_2 + 2H_2O$ 取少量白色固体于试管中,加入适量的水,充分振荡后加入1~2滴无色酚酞溶液(或取少量白色固体于试管中,加入适量的水,充分振荡后加入1~2滴紫色石蕊溶液) 浊液变红(或浊液变蓝)
(3)密封
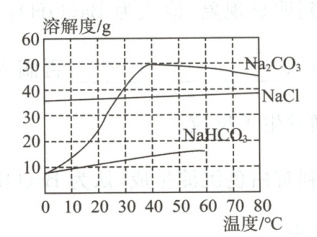
20.(8分)“果蔬洗盐”是一种果蔬清洁剂。某“果蔬洗盐”标签及相关物质的溶解度曲线如图所示。
|果蔬洗盐|
|--|
|配料:氯化钠、碳酸钠、碳酸氢钠(其质量比为4:5:1)|
|使用方法:15 g“果蔬洗盐”加入1 000 g水配成溶液,将果蔬浸入溶液中,3 min后捞出,清水冲洗干净|
(1)在实验室配制该溶液,并将配好的果蔬洗盐溶液分成两份,分别用于清洗蔬菜和水果。分成两份后两溶液中氯化钠的溶质质量分数(填“变大”“变小”或“不变”)。
(2)根据标签信息,15g“果蔬洗盐”含碳酸钠g。除去$NaCl$样品中少量的$Na_2CO_3$,可用溶解→蒸发结晶→过滤的方法,其中过滤要在40℃左右进行的原因是。
(3)根据配料表可知配制成的果蔬洗盐溶液呈(填“酸性”或“碱性”)。有同学提出,可以将氢氧化钠固体加入“果蔬洗盐”中,以增强其洗涤效果,但遭到大家一致反对,理由是。

|果蔬洗盐|
|--|
|配料:氯化钠、碳酸钠、碳酸氢钠(其质量比为4:5:1)|
|使用方法:15 g“果蔬洗盐”加入1 000 g水配成溶液,将果蔬浸入溶液中,3 min后捞出,清水冲洗干净|
(1)在实验室配制该溶液,并将配好的果蔬洗盐溶液分成两份,分别用于清洗蔬菜和水果。分成两份后两溶液中氯化钠的溶质质量分数(填“变大”“变小”或“不变”)。
(2)根据标签信息,15g“果蔬洗盐”含碳酸钠g。除去$NaCl$样品中少量的$Na_2CO_3$,可用溶解→蒸发结晶→过滤的方法,其中过滤要在40℃左右进行的原因是。
(3)根据配料表可知配制成的果蔬洗盐溶液呈(填“酸性”或“碱性”)。有同学提出,可以将氢氧化钠固体加入“果蔬洗盐”中,以增强其洗涤效果,但遭到大家一致反对,理由是。
答案:
25.
(1)<
(2)氧化铜与硫酸反应生成硫酸铜和水。由质量守恒定律可知,溶液增重的质量即为参加反应的氧化铜的质量,即104.0g−100.0g = 4.0g。
设生成硫酸铜的质量为x,则:
$CuO + H_2SO_4 \longrightarrow CuSO_4 + H_2O$
$80$ $160$
$4.0g$ $x$
$\frac{80}{160} = \frac{4.0g}{x}$
$x = 8.0g$
所得溶液中硫酸铜的质量分数为$\frac{8.0g}{104.0g} × 100\% \approx 7.7\%$。
答:所得溶液中硫酸铜的质量分数约为7.7%。
(1)<
(2)氧化铜与硫酸反应生成硫酸铜和水。由质量守恒定律可知,溶液增重的质量即为参加反应的氧化铜的质量,即104.0g−100.0g = 4.0g。
设生成硫酸铜的质量为x,则:
$CuO + H_2SO_4 \longrightarrow CuSO_4 + H_2O$
$80$ $160$
$4.0g$ $x$
$\frac{80}{160} = \frac{4.0g}{x}$
$x = 8.0g$
所得溶液中硫酸铜的质量分数为$\frac{8.0g}{104.0g} × 100\% \approx 7.7\%$。
答:所得溶液中硫酸铜的质量分数约为7.7%。
查看更多完整答案,请扫码查看


