第51页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
- 第107页
- 第108页
- 第109页
- 第110页
- 第111页
- 第112页
- 第113页
- 第114页
- 第115页
- 第116页
- 第117页
- 第118页
- 第119页
- 第120页
- 第121页
- 第122页
- 第123页
- 第124页
- 第125页
- 第126页
- 第127页
- 第128页
- 第129页
- 第130页
- 第131页
- 第132页
- 第133页
- 第134页
- 第135页
- 第136页
- 第137页
- 第138页
- 第139页
- 第140页
- 第141页
20.(8分)(2025·连云港)氢气的发现、制取、贮存和利用意义重大。
【发现氢气】16世纪科学家就发现稀$H_{2}SO_{4}$与Fe反应能生成“易燃空气”。1787年拉瓦锡将$H_{2}O(g)$[表示水蒸气]通过一根烧红的铁制枪管,得到了同样的“易燃空气”。他将“易燃空气”命名为“生成水的元素”,即氢。
(1)拉瓦锡实验中,枪管内壁有黑色固体($Fe_{3}O_{4}$)生成,该反应的化学方程式为。
【制取氢气】一种以$NiFe_{2}O_{4}$为催化剂制氢的反应原理如图所示。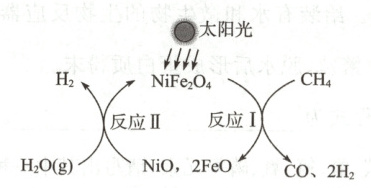
(2)反应Ⅰ中$NiFe_{2}O_{4}$(填“参加”或“未参加”)化学反应。
(3)将16g$CH_{4}$和足量的$H_{2}O(g)$通过该方法制氢,理论上可获得g$H_{2}$。
【贮存氢气】镁基材料固态储氢具有储量大、安全等优点。储氢时,$Mg$与$H_{2}$在一定条件下反应生成$MgH_{2}$固体。1$m^{3}$镁基材料储存的$H_{2}$在常温常压下体积可达1345$m^{3}$。
(4)镁基材料储氢量大的原因是。
【发现氢气】16世纪科学家就发现稀$H_{2}SO_{4}$与Fe反应能生成“易燃空气”。1787年拉瓦锡将$H_{2}O(g)$[表示水蒸气]通过一根烧红的铁制枪管,得到了同样的“易燃空气”。他将“易燃空气”命名为“生成水的元素”,即氢。
(1)拉瓦锡实验中,枪管内壁有黑色固体($Fe_{3}O_{4}$)生成,该反应的化学方程式为。
【制取氢气】一种以$NiFe_{2}O_{4}$为催化剂制氢的反应原理如图所示。

(2)反应Ⅰ中$NiFe_{2}O_{4}$(填“参加”或“未参加”)化学反应。
(3)将16g$CH_{4}$和足量的$H_{2}O(g)$通过该方法制氢,理论上可获得g$H_{2}$。
【贮存氢气】镁基材料固态储氢具有储量大、安全等优点。储氢时,$Mg$与$H_{2}$在一定条件下反应生成$MgH_{2}$固体。1$m^{3}$镁基材料储存的$H_{2}$在常温常压下体积可达1345$m^{3}$。
(4)镁基材料储氢量大的原因是。
答案:
(1) 3Fe + 4H₂O(g) =高温= Fe₃O₄ + 4H₂
(2) 参加
(3) 6
(4) 氢气在固态镁基材料中密度远大于常温常压下的密度
(1) 3Fe + 4H₂O(g) =高温= Fe₃O₄ + 4H₂
(2) 参加
(3) 6
(4) 氢气在固态镁基材料中密度远大于常温常压下的密度
查看更多完整答案,请扫码查看


