第7页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
11. 常温下,向某浓度的硫酸中逐滴滴入某浓度的氢氧化钡溶液,生成沉淀的质量与加入氢氧化钡溶液的体积关系如图所示。$ a $、$ b $、$ c $、$ d $ 分别表示实验时不同阶段的反应结果,下列有关说法中错误的是(
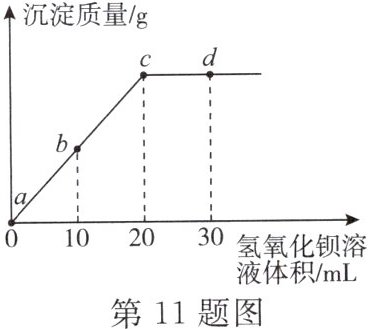
A.溶液的导电能力:$ a > b > c > d $
B.溶液的 $ pH $ 大小:$ a < b < c < d $
C.$ b $ 点溶液呈酸性,$ c $ 点溶液呈中性
D.反应到 $ c $ 点时烧杯中没有任何离子(不考虑水的电离)
A
)
A.溶液的导电能力:$ a > b > c > d $
B.溶液的 $ pH $ 大小:$ a < b < c < d $
C.$ b $ 点溶液呈酸性,$ c $ 点溶液呈中性
D.反应到 $ c $ 点时烧杯中没有任何离子(不考虑水的电离)
答案:
A
12. 稀硫酸是实验室中一种重要的试剂,用途广泛。小叶向盛有稀硫酸的烧杯中加入适量的某种固体与之反应。反应前后烧杯内溶液中主要离子种类及个数比变化如图所示(不考虑大小)。则加入的固体不可能是(
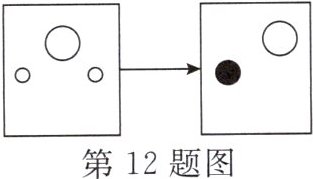
A.铁
B.铝
C.氧化铜
D.氢氧化镁
B
)
A.铁
B.铝
C.氧化铜
D.氢氧化镁
答案:
B
13. 实验室常用锌和稀硫酸反应来制取氢气,向盛有稀硫酸溶液的烧杯中加入足量的锌至反应完全。
(1)写出该反应的化学方程式:________。
(2)图中的 表示溶液中由溶质电离产生的不同离子,则“●”表示
表示溶液中由溶质电离产生的不同离子,则“●”表示
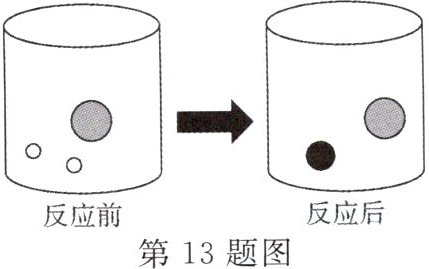
(1)写出该反应的化学方程式:________。
(2)图中的
 表示溶液中由溶质电离产生的不同离子,则“●”表示
表示溶液中由溶质电离产生的不同离子,则“●”表示SO₄²⁻
(填离子符号)。
答案:
(1)Zn+H₂SO₄=ZnSO₄+H₂↑;
(2)SO₄²⁻
(1)Zn+H₂SO₄=ZnSO₄+H₂↑;
(2)SO₄²⁻
14. 某工厂化验室用 $ 15\% $ 的氢氧化钠溶液洗涤一定量石油产品中的残余硫酸(该产品中其他物质不与 $ NaOH $ 反应),消耗氢氧化钠溶液的质量与反应过程中溶液的 $ pH $ 值关系如图所示。求石油产品中残余硫酸的质量。
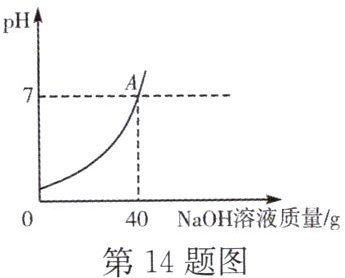

答案:
解:由图可知,恰好完全反应时消耗15%的NaOH溶液质量为40g。
1. 计算NaOH溶质质量:
$m(NaOH) = 40\,g × 15\% = 6\,g$
2. 设石油产品中残余硫酸的质量为$x$,反应方程式为:
$H_2SO_4 + 2NaOH = Na_2SO_4 + 2H_2O$
3. 列出比例式:
$\frac{98}{80} = \frac{x}{6\,g}$
4. 解得:
$x = \frac{98 × 6\,g}{80} = 7.35\,g$
答:石油产品中残余硫酸的质量为7.35g。
1. 计算NaOH溶质质量:
$m(NaOH) = 40\,g × 15\% = 6\,g$
2. 设石油产品中残余硫酸的质量为$x$,反应方程式为:
$H_2SO_4 + 2NaOH = Na_2SO_4 + 2H_2O$
3. 列出比例式:
$\frac{98}{80} = \frac{x}{6\,g}$
4. 解得:
$x = \frac{98 × 6\,g}{80} = 7.35\,g$
答:石油产品中残余硫酸的质量为7.35g。
15. 某实验小组在研究酸的化学性质时,做了如图所示的 5 个实验:
(1)实验后,某试管中溶液呈浅绿色,该试管中发生反应的化学方程式为________。
(2)实验后,向某试管中滴加无色酚酞试液,溶液变红,再向此试管中加稀盐酸,只观察到溶液由红色变为无色。据此推断,该试管中最初发生的反应的化学方程式可能为
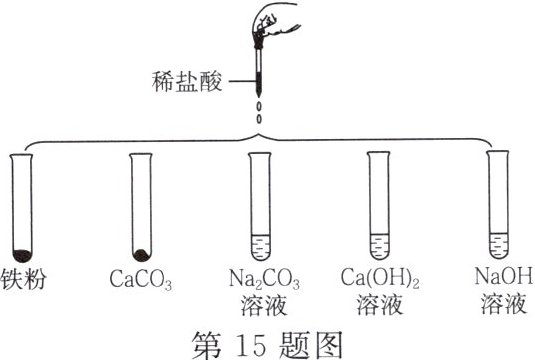
(1)实验后,某试管中溶液呈浅绿色,该试管中发生反应的化学方程式为________。
(2)实验后,向某试管中滴加无色酚酞试液,溶液变红,再向此试管中加稀盐酸,只观察到溶液由红色变为无色。据此推断,该试管中最初发生的反应的化学方程式可能为
NaOH+HCl=NaCl+H₂O(或Ca(OH)₂+2HCl=CaCl₂+2H₂O)
(写出一个即可)。
答案:
(1)Fe+2HCl=FeCl₂+H₂↑;
(2)NaOH+HCl=NaCl+H₂O(或Ca(OH)₂+2HCl=CaCl₂+2H₂O)
(1)Fe+2HCl=FeCl₂+H₂↑;
(2)NaOH+HCl=NaCl+H₂O(或Ca(OH)₂+2HCl=CaCl₂+2H₂O)
查看更多完整答案,请扫码查看


