第41页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
变式 4 实验室中现有氢氧化钠、氢氧化钙、稀硫酸、氯化钠四瓶遗失标签的溶液,为了鉴别这些溶液,将它们随机编号为 A、B、C、D,按如下实验进行鉴别:
步骤一:取适量 A、B、C、D 四种试液于试管中,分别加入试剂①,观察到 A、C 溶液变为红色,B、D 溶液仍为无色;
步骤二:另取适量 A、C 试液于洁净试管中,分别通入无色气体②,A 中出现白色沉淀,C 中无明显现象;
步骤三:另取适量 B、D 试液于洁净试管中,分别加入氯化钡溶液,B 中出现白色沉淀,D 中无明显现象。
根据以上现象,回答下列问题:
(1)试剂①②的名称分别是:①
(2)待测溶液 A、B、C、D 的化学式分别是:A:
(3)写出步骤三中生成白色沉淀的化学方程式:
(4)为了证明步骤二 C 溶液中也发生了化学反应,向反应后的溶液中加入氯化钙溶液进行检验,请写出该检验反应的化学方程式:
步骤一:取适量 A、B、C、D 四种试液于试管中,分别加入试剂①,观察到 A、C 溶液变为红色,B、D 溶液仍为无色;
步骤二:另取适量 A、C 试液于洁净试管中,分别通入无色气体②,A 中出现白色沉淀,C 中无明显现象;
步骤三:另取适量 B、D 试液于洁净试管中,分别加入氯化钡溶液,B 中出现白色沉淀,D 中无明显现象。
根据以上现象,回答下列问题:
(1)试剂①②的名称分别是:①
无色酚酞试液
;②二氧化碳
。(2)待测溶液 A、B、C、D 的化学式分别是:A:
$Ca(OH)_{2}$
;B:$H_{2}SO_{4}$
;C:$NaOH$
;D:$NaCl$
。(3)写出步骤三中生成白色沉淀的化学方程式:
$H_{2}SO_{4}+BaCl_{2}=BaSO_{4}\downarrow +2HCl$
。(4)为了证明步骤二 C 溶液中也发生了化学反应,向反应后的溶液中加入氯化钙溶液进行检验,请写出该检验反应的化学方程式:
$Na_{2}CO_{3}+CaCl_{2}=CaCO_{3}\downarrow +2NaCl$
。
答案:
(1)①无色酚酞试液;②二氧化碳。
(2)A:$Ca(OH)_{2}$;B:$H_{2}SO_{4}$;C:$NaOH$;D:$NaCl$。
(3)$H_{2}SO_{4}+BaCl_{2}=BaSO_{4}\downarrow +2HCl$。
(4)$Na_{2}CO_{3}+CaCl_{2}=CaCO_{3}\downarrow +2NaCl$。
(2)A:$Ca(OH)_{2}$;B:$H_{2}SO_{4}$;C:$NaOH$;D:$NaCl$。
(3)$H_{2}SO_{4}+BaCl_{2}=BaSO_{4}\downarrow +2HCl$。
(4)$Na_{2}CO_{3}+CaCl_{2}=CaCO_{3}\downarrow +2NaCl$。
典例 5 现有 HCl 与 CaCl₂的混合溶液,为了分析混合溶液中 HCl 和 CaCl₂的质量分数,设计了如图实验方案:

【实验数据】实验共记录了两组数据:
第①组:气体吸收完全后,NaOH 溶液质量增加 4.4g;
第②组:沉淀完全后,经过滤、洗涤、烘干后得到固体的质量为 10g。
根据实验设计及有关数据进行分析与计算:
(1)混合溶液中 HCl 的质量分数为________。
(2)混合溶液中 CaCl₂的质量分数(写出计算过程)。
(3)实验中混合溶液与 Na₂CO₃溶液恰好完全反应,经过滤后所得“滤液”中溶质的质量分数为.3%(不考虑过滤中的损失,计算结果保留一位小数)。
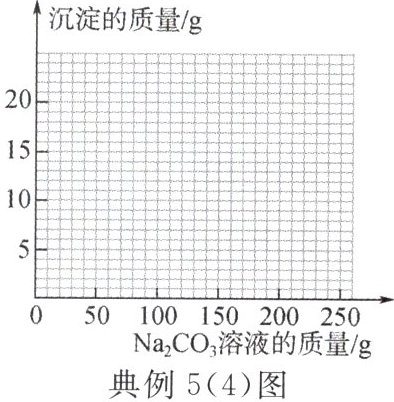
(4)若在 100g 混合溶液中不断加入 10.6%的 Na₂CO₃溶液,请你画出加入 Na₂CO₃溶液的质量与产生沉淀的质量的关系图。

【实验数据】实验共记录了两组数据:
第①组:气体吸收完全后,NaOH 溶液质量增加 4.4g;
第②组:沉淀完全后,经过滤、洗涤、烘干后得到固体的质量为 10g。
根据实验设计及有关数据进行分析与计算:
(1)混合溶液中 HCl 的质量分数为________。
(2)混合溶液中 CaCl₂的质量分数(写出计算过程)。
(3)实验中混合溶液与 Na₂CO₃溶液恰好完全反应,经过滤后所得“滤液”中溶质的质量分数为.3%(不考虑过滤中的损失,计算结果保留一位小数)。
(4)若在 100g 混合溶液中不断加入 10.6%的 Na₂CO₃溶液,请你画出加入 Na₂CO₃溶液的质量与产生沉淀的质量的关系图。

答案:
(1)7.3%
(2)设混合溶液中CaCl₂的质量为y。
CaCl₂ + Na₂CO₃ = CaCO₃↓ + 2NaCl
111 100
y 10g
111/100 = y/10g
y=11.1g
CaCl₂的质量分数=11.1g/100g×100%=11.1%
(3)8.2%
(4)
沉淀的质量/g
20|
15|
10| ●
5| /
0|____●_______
0 50 100 150 200 250
Na₂CO₃溶液的质量/g
(注:图中●为(100,0)和(200,10),线段从(100,0)到(200,10),200g后水平延伸)
(2)设混合溶液中CaCl₂的质量为y。
CaCl₂ + Na₂CO₃ = CaCO₃↓ + 2NaCl
111 100
y 10g
111/100 = y/10g
y=11.1g
CaCl₂的质量分数=11.1g/100g×100%=11.1%
(3)8.2%
(4)
沉淀的质量/g
20|
15|
10| ●
5| /
0|____●_______
0 50 100 150 200 250
Na₂CO₃溶液的质量/g
(注:图中●为(100,0)和(200,10),线段从(100,0)到(200,10),200g后水平延伸)
查看更多完整答案,请扫码查看


