第71页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
- 第107页
- 第108页
3 中考新考法 实验创新 实验小组用如图所示装置完成电解水实验并收集产生的气体,下列说法错误的是(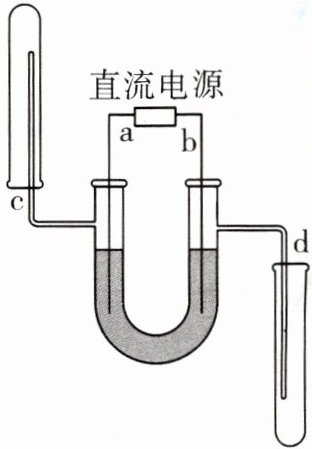
A.a端应连接电源的负极
B.c管与d管收集到的气体总质量之比为1:8
C.c管收集的气体是氢气
D.d管中的气体先收集满
D
)。
A.a端应连接电源的负极
B.c管与d管收集到的气体总质量之比为1:8
C.c管收集的气体是氢气
D.d管中的气体先收集满
答案:
D
4 (2025·黑龙江绥化绥棱六中月考)图中 “○”“●”分别表示不同的原子,其中可能表示氧化物的是(
“○”“●”分别表示不同的原子,其中可能表示氧化物的是(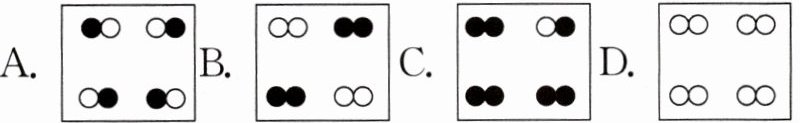
 “○”“●”分别表示不同的原子,其中可能表示氧化物的是(
“○”“●”分别表示不同的原子,其中可能表示氧化物的是(A
)。
答案:
A
5 (2024·内江中考)硝酸$(HNO_3)$中氮元素的化合价为(
A.+1
B.+2
C.+3
D.+5
D
)。A.+1
B.+2
C.+3
D.+5
答案:
D
(1)葡萄糖酸锌的相对分子质量是455,则葡萄糖酸锌化学式中氧原子右下角的数字为
(2)葡萄糖酸锌中碳、氢元素的质量比为
(3)该葡萄糖酸锌口服液中葡萄糖酸锌的质量分数为多少?(写出计算过程)
解:葡萄糖酸锌口服液中葡萄糖酸锌的质量为$\frac{5.0\ \text{mg}}{\frac{65}{455}×100\%}=35\ \text{mg}$,则该葡萄糖酸锌口服液中葡萄糖酸锌的质量分数为$\frac{35\ \text{mg}}{10.0\ \text{g}×1000\ \text{mg/g}}×100\%=0.35\%$
答:该葡萄糖酸锌口服液中葡萄糖酸锌的质量分数为0.35%。
14
。(2)葡萄糖酸锌中碳、氢元素的质量比为
72:11
。(3)该葡萄糖酸锌口服液中葡萄糖酸锌的质量分数为多少?(写出计算过程)
解:葡萄糖酸锌口服液中葡萄糖酸锌的质量为$\frac{5.0\ \text{mg}}{\frac{65}{455}×100\%}=35\ \text{mg}$,则该葡萄糖酸锌口服液中葡萄糖酸锌的质量分数为$\frac{35\ \text{mg}}{10.0\ \text{g}×1000\ \text{mg/g}}×100\%=0.35\%$
答:该葡萄糖酸锌口服液中葡萄糖酸锌的质量分数为0.35%。
答案:
(1)14
(2)72:11
(3)解:葡萄糖酸锌口服液中葡萄糖酸锌的质量为$\frac{5.0\ \text{mg}}{\frac{65}{455}×100\%}=35\ \text{mg}$,则该葡萄糖酸锌口服液中葡萄糖酸锌的质量分数为$\frac{35\ \text{mg}}{10.0\ \text{g}×1000\ \text{mg/g}}×100\%=0.35\%$
答:该葡萄糖酸锌口服液中葡萄糖酸锌的质量分数为0.35%。
(1)14
(2)72:11
(3)解:葡萄糖酸锌口服液中葡萄糖酸锌的质量为$\frac{5.0\ \text{mg}}{\frac{65}{455}×100\%}=35\ \text{mg}$,则该葡萄糖酸锌口服液中葡萄糖酸锌的质量分数为$\frac{35\ \text{mg}}{10.0\ \text{g}×1000\ \text{mg/g}}×100\%=0.35\%$
答:该葡萄糖酸锌口服液中葡萄糖酸锌的质量分数为0.35%。
7 (2024·贵州六盘水期末)2023年11月30日,同济大学许维教授团队利用十氯代蒽$(C_1_4Cl_1₀)$成功合成了芳香性环形碳C_1_4。C_1_4在新型半导体材料、分子电子器件中有着广阔的应用前景。下列有关说法正确的是(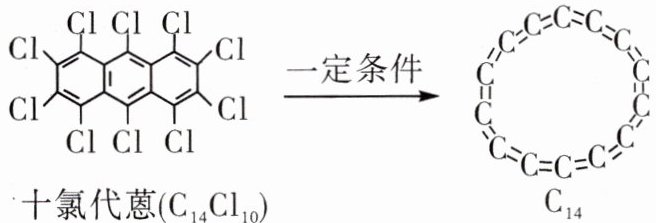
A.十氯代蒽分子中含有C_1_4分子
B.十氯代蒽的相对分子质量为523g
C.十氯代蒽分子由碳原子和氯原子构成
D.十氯代蒽中碳元素与氯元素的质量比为14:10
C
)。
A.十氯代蒽分子中含有C_1_4分子
B.十氯代蒽的相对分子质量为523g
C.十氯代蒽分子由碳原子和氯原子构成
D.十氯代蒽中碳元素与氯元素的质量比为14:10
答案:
C
(1)实验1:1766年,英国科学家卡文迪许通过实验发现“易燃空气”在纯氧中燃烧只生成水,该“易燃空气”的元素组成为
(2)实验2:1785年拉瓦锡通过让水蒸气通过高温的铁制枪管,将水转化为氢气,同时生成四氧化三铁(如图)。反应的符号表达式为
(3)实验3:1800年,尼科尔森利用新发明的伏打电池并使用银币和锌片作为正极和负极,进行电解水实验(如图)。
①该实验证明了水由
②测得V(甲):V(乙)= 1:2,要确定水分子中氢、氧原子个数之比,还需要的数据有
H
(填元素符号),该反应的符号表达式为H₂+O₂$\xrightarrow{\text{点燃}}$H₂O
。(2)实验2:1785年拉瓦锡通过让水蒸气通过高温的铁制枪管,将水转化为氢气,同时生成四氧化三铁(如图)。反应的符号表达式为
Fe+H₂O$\xrightarrow{\text{高温}}$Fe₃O₄+H₂
,该实验能
(填“能”或“不能”)得出结论“水不是一种元素”。(3)实验3:1800年,尼科尔森利用新发明的伏打电池并使用银币和锌片作为正极和负极,进行电解水实验(如图)。
①该实验证明了水由
氢、氧
元素组成。写出水电解反应的符号表达式:H₂O$\xrightarrow{\text{通电}}$H₂+O₂
。除此以外水参与的反应还有很多,请写出一个有水生成的分解反应的符号表达式:H₂O₂$\xrightarrow{\text{MnO₂}}$H₂O+O₂
(合理即可)。②测得V(甲):V(乙)= 1:2,要确定水分子中氢、氧原子个数之比,还需要的数据有
BC
(填字母)。
答案:
(1)$\text{H}$ $\text{H}_{2}+\text{O}_{2}\xrightarrow{\text{点燃}}\text{H}_{2}\text{O}$
(2)$\text{Fe}+\text{H}_{2}\text{O}\xrightarrow{\text{高温}}\text{Fe}_{3}\text{O}_{4}+\text{H}_{2}$ 能
(3)①氢、氧 $\text{H}_{2}\text{O}\xrightarrow{\text{通电}}\text{H}_{2}+\text{O}_{2}$ $\text{H}_{2}\text{O}_{2}\xrightarrow{\text{MnO}_{2}}\text{H}_{2}\text{O}+\text{O}_{2}$(合理即可) ②BC
(1)$\text{H}$ $\text{H}_{2}+\text{O}_{2}\xrightarrow{\text{点燃}}\text{H}_{2}\text{O}$
(2)$\text{Fe}+\text{H}_{2}\text{O}\xrightarrow{\text{高温}}\text{Fe}_{3}\text{O}_{4}+\text{H}_{2}$ 能
(3)①氢、氧 $\text{H}_{2}\text{O}\xrightarrow{\text{通电}}\text{H}_{2}+\text{O}_{2}$ $\text{H}_{2}\text{O}_{2}\xrightarrow{\text{MnO}_{2}}\text{H}_{2}\text{O}+\text{O}_{2}$(合理即可) ②BC
查看更多完整答案,请扫码查看


