第80页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
- 第107页
- 第108页
- 第109页
- 第110页
- 第111页
- 第112页
- 第113页
- 第114页
- 第115页
- 第116页
- 第117页
- 第118页
- 第119页
- 第120页
- 第121页
- 第122页
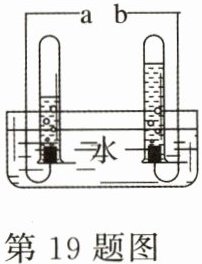
19.如图是同学们在实验室进行电解水的实验装置图,根据图示回答下列问题:
(1)判断a是电源的 极;
(2)接通电源后,发现正、负极上出现气泡,一段时间后,正、负极产生气体的体积之比接近 ;
(3)该反应的文字表达式是 ;
(4)通过该实验,同学们得到的结论是 。
(1)判断a是电源的 极;
(2)接通电源后,发现正、负极上出现气泡,一段时间后,正、负极产生气体的体积之比接近 ;
(3)该反应的文字表达式是 ;
(4)通过该实验,同学们得到的结论是 。

答案:
(1)负
(2)1:2
(3)水$\stackrel{通电}{→}$氢气 + 氧气
(4)水由氢元素和氧元素组成
[解析]
(1)由电解水的实验装置图可知,接通直流电源后,a端收集到的气体较多,是氢气,则a端电极是电源的负极;
(2)由电解水的实验装置图可知,接通直流电源后,a端收集到的气体较多,是氢气,b端收集到的气体较少,是氧气,氧气和氢气的体积之比是1:2;
(3)水在通电的条件下分解生成氢气和氧气,该反应的文字表达式是水$\stackrel{通电}{→}$氢气 + 氧气;
(4)通过该实验可得出的结论是水由氢元素和氧元素组成。
(1)负
(2)1:2
(3)水$\stackrel{通电}{→}$氢气 + 氧气
(4)水由氢元素和氧元素组成
[解析]
(1)由电解水的实验装置图可知,接通直流电源后,a端收集到的气体较多,是氢气,则a端电极是电源的负极;
(2)由电解水的实验装置图可知,接通直流电源后,a端收集到的气体较多,是氢气,b端收集到的气体较少,是氧气,氧气和氢气的体积之比是1:2;
(3)水在通电的条件下分解生成氢气和氧气,该反应的文字表达式是水$\stackrel{通电}{→}$氢气 + 氧气;
(4)通过该实验可得出的结论是水由氢元素和氧元素组成。
五、计算题(共6分)
20.目前市场上的补钙药品很多,如图是某品牌补钙药品的部分说明书。列式计算求解:
(1)碳酸钙(CaCO₃)的相对分子质量;
(2)碳酸钙中各元素的质量比;
(3)碳酸钙中钙元素的质量分数;
(4)如果按用量服用,则每天补充钙元素的质量是多少?

20.目前市场上的补钙药品很多,如图是某品牌补钙药品的部分说明书。列式计算求解:
(1)碳酸钙(CaCO₃)的相对分子质量;
(2)碳酸钙中各元素的质量比;
(3)碳酸钙中钙元素的质量分数;
(4)如果按用量服用,则每天补充钙元素的质量是多少?

答案:
解:
(1)CaCO₃的相对分子质量是40 + 12 + 16×3 = 100;
(2)CaCO₃中钙、碳、氧三种元素的质量比是40:12:(16×3) = 10:3:12;
(3)CaCO₃中钙元素的质量分数是$\frac{40}{100}$×100% = 40%;
(4)每片含碳酸钙0.75g,口服每次1片,每天2次,则每天补充钙元素的质量是0.75g×2×40% = 0.6g。
(1)CaCO₃的相对分子质量是40 + 12 + 16×3 = 100;
(2)CaCO₃中钙、碳、氧三种元素的质量比是40:12:(16×3) = 10:3:12;
(3)CaCO₃中钙元素的质量分数是$\frac{40}{100}$×100% = 40%;
(4)每片含碳酸钙0.75g,口服每次1片,每天2次,则每天补充钙元素的质量是0.75g×2×40% = 0.6g。
查看更多完整答案,请扫码查看


