第79页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
- 第107页
- 第108页
- 第109页
- 第110页
- 第111页
- 第112页
- 第113页
- 第114页
- 第115页
- 第116页
- 第117页
- 第118页
- 第119页
- 第120页
- 第121页
- 第122页
15.化合价是元素在形成化合物时表现出的一种性质,通常是根据元素在化合时原子得失电子的数目规定的。比如在化学反应中,钠原子失去一个电子,钠元素的化合价为+1价,氯原子得到一个电子,氯元素的化合价为−1价。
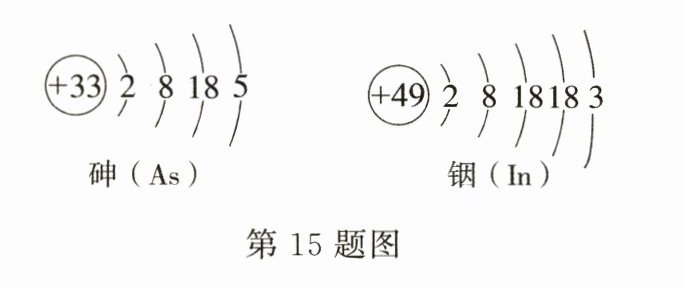
已知砷和铟的原子结构示意图如图,根据此规律,回答下列问题:
(1)铟在化学反应中容易 (填“得到”或“失去”)电子;
(2)砷化铟有优异的电学性能,可替代硅制造电子设备。砷化铟的化学式是 。

已知砷和铟的原子结构示意图如图,根据此规律,回答下列问题:
(1)铟在化学反应中容易 (填“得到”或“失去”)电子;
(2)砷化铟有优异的电学性能,可替代硅制造电子设备。砷化铟的化学式是 。
答案:
(1)失去
(2)InAs
[解析]
(1)铟原子的最外层电子数是3,小于4,在化学反应中容易失去电子;
(2)砷原子的最外层电子数是5,容易得到3个电子形成As³⁻,砷化铟的化学式是InAs。
(1)失去
(2)InAs
[解析]
(1)铟原子的最外层电子数是3,小于4,在化学反应中容易失去电子;
(2)砷原子的最外层电子数是5,容易得到3个电子形成As³⁻,砷化铟的化学式是InAs。
16.中国在南海成功试采可燃冰,它将推动世界能源利用格局的改变。已知某种可燃冰的化学式是CH₄·8H₂O。请回答下列问题:
(1)这种可燃冰中碳、氢、氧元素的原子个数之比是 ;
(2)这种可燃冰中质量分数最高的元素是 ;
(3)这种可燃冰的相对分子质量是 。
(1)这种可燃冰中碳、氢、氧元素的原子个数之比是 ;
(2)这种可燃冰中质量分数最高的元素是 ;
(3)这种可燃冰的相对分子质量是 。
答案:
(1)1:20:8
(2)氧元素(或O)
(3)160
[解析]
(1)由可燃冰的化学式CH₄·8H₂O可知,碳、氢、氧元素的原子个数之比是1:20:8;
(2)可燃冰中碳、氢、氧元素的质量比是12:(1×20):(16×8) = 12:20:128 = 3:5:32,则可燃冰中质量分数最高的元素是氧元素;
(3)由可燃冰的化学式CH₄·8H₂O可知,相对分子质量是12 + 1×4 + 8×(1×2 + 16) = 160。
(1)1:20:8
(2)氧元素(或O)
(3)160
[解析]
(1)由可燃冰的化学式CH₄·8H₂O可知,碳、氢、氧元素的原子个数之比是1:20:8;
(2)可燃冰中碳、氢、氧元素的质量比是12:(1×20):(16×8) = 12:20:128 = 3:5:32,则可燃冰中质量分数最高的元素是氧元素;
(3)由可燃冰的化学式CH₄·8H₂O可知,相对分子质量是12 + 1×4 + 8×(1×2 + 16) = 160。
17.氢气是初中常见的气体之一,实验室可通过锌粒与稀硫酸反应制得。
(1)收集氢气时可采用排水法,推知氢气有 的性质;
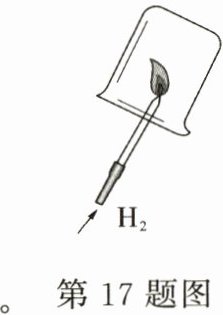
(2)如图所示,在点燃氢气前一定先检验 ;
(3)在空气中点燃纯净的氢气,该反应的符号表达式为
(1)收集氢气时可采用排水法,推知氢气有 的性质;
(2)如图所示,在点燃氢气前一定先检验 ;
(3)在空气中点燃纯净的氢气,该反应的符号表达式为

答案:
(1)难溶于水且不与水反应
(2)氢气的纯度
(3)H₂+O₂$\stackrel{点燃}{→}$H₂O
[解析]
(1)氢气难溶于水且不与水反应,所以可以用排水法收集;
(2)氢气是可燃性气体,与空气混合达到一定的程度,遇明火有爆炸的危险,所以在点燃氢气前一定先检验氢气的纯度;
(3)氢气在空气中燃烧生成水,该反应的符号表达式为H₂+O₂$\stackrel{点燃}{→}$H₂O。
(1)难溶于水且不与水反应
(2)氢气的纯度
(3)H₂+O₂$\stackrel{点燃}{→}$H₂O
[解析]
(1)氢气难溶于水且不与水反应,所以可以用排水法收集;
(2)氢气是可燃性气体,与空气混合达到一定的程度,遇明火有爆炸的危险,所以在点燃氢气前一定先检验氢气的纯度;
(3)氢气在空气中燃烧生成水,该反应的符号表达式为H₂+O₂$\stackrel{点燃}{→}$H₂O。
18.某化学兴趣小组在实验室中对浑浊的湖水进行了如下简单的净化,请回答有关问题:
(1)先向烧杯中加入适量混凝剂,混凝剂可以选择 。
(2)过滤液体:
①过滤时所必需的仪器有 (填字母,下同);
A.试管 B.酒精灯 C.玻璃棒 D.烧杯 E.铁架台(带铁圈)
F.托盘天平 G.漏斗
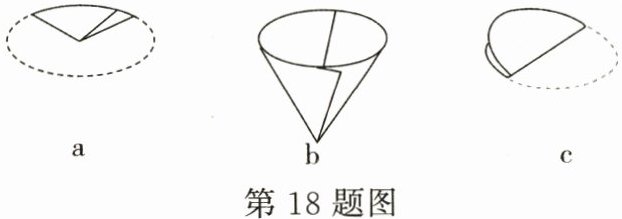
②制作过滤器的过程如图所示,正确操作顺序是 ;
③在过滤时,小明发现过滤速率较慢,可能的原因是滤纸没有紧贴漏斗内壁;
④若过滤两次以后滤液仍然浑浊,其原因可能是滤纸破损、漏斗内液面高于滤纸边缘等。
(3)再用活性炭除去水中的异味,这是利用了活性炭的吸附性。
(4)为了检验净化后的水是软水还是硬水,可向水中加入肥皂水。
(1)先向烧杯中加入适量混凝剂,混凝剂可以选择 。
(2)过滤液体:
①过滤时所必需的仪器有 (填字母,下同);
A.试管 B.酒精灯 C.玻璃棒 D.烧杯 E.铁架台(带铁圈)
F.托盘天平 G.漏斗
②制作过滤器的过程如图所示,正确操作顺序是 ;
③在过滤时,小明发现过滤速率较慢,可能的原因是滤纸没有紧贴漏斗内壁;
④若过滤两次以后滤液仍然浑浊,其原因可能是滤纸破损、漏斗内液面高于滤纸边缘等。
(3)再用活性炭除去水中的异味,这是利用了活性炭的吸附性。
(4)为了检验净化后的水是软水还是硬水,可向水中加入肥皂水。

答案:
(1)明矾
(2)①CDEG ②cab
③漏斗下端管口没有紧靠烧杯内壁(或滤纸与漏斗之间有气泡)
④滤纸破损(或漏斗内液面高于滤纸边缘等合理即可)
(3)吸附
(4)肥皂水
[解析]
(1)明矾可以使水中悬浮的杂质较快沉降,常用作混凝剂。
(2)①过滤用到的仪器有玻璃棒、烧杯、铁架台(带铁圈)、漏斗,故填:CDEG。
②首先将滤纸对折两次成一个扇形,即c→a,然后撑开中间,使其中一边是3层,另一边是1层,即b,所以正确操作顺序是cab。
③滤纸湿润后要紧贴漏斗内壁,不能留有空隙,若滤纸与漏斗内壁留有空隙,则过滤速率会比较慢;漏斗下端管口要紧靠烧杯内壁,若漏斗下端管口没有紧靠烧杯内壁,也会一定程度上影响过滤速率。
④滤纸破损、漏斗内液面高于滤纸边缘、仪器不干净都会造成过滤后滤液仍然浑浊。
(3)活性炭能够吸附水中的色素和异味,这是利用了活性炭的吸附性。
(4)为了检验净化后的水是软水还是硬水,可向水中加入肥皂水。
(1)明矾
(2)①CDEG ②cab
③漏斗下端管口没有紧靠烧杯内壁(或滤纸与漏斗之间有气泡)
④滤纸破损(或漏斗内液面高于滤纸边缘等合理即可)
(3)吸附
(4)肥皂水
[解析]
(1)明矾可以使水中悬浮的杂质较快沉降,常用作混凝剂。
(2)①过滤用到的仪器有玻璃棒、烧杯、铁架台(带铁圈)、漏斗,故填:CDEG。
②首先将滤纸对折两次成一个扇形,即c→a,然后撑开中间,使其中一边是3层,另一边是1层,即b,所以正确操作顺序是cab。
③滤纸湿润后要紧贴漏斗内壁,不能留有空隙,若滤纸与漏斗内壁留有空隙,则过滤速率会比较慢;漏斗下端管口要紧靠烧杯内壁,若漏斗下端管口没有紧靠烧杯内壁,也会一定程度上影响过滤速率。
④滤纸破损、漏斗内液面高于滤纸边缘、仪器不干净都会造成过滤后滤液仍然浑浊。
(3)活性炭能够吸附水中的色素和异味,这是利用了活性炭的吸附性。
(4)为了检验净化后的水是软水还是硬水,可向水中加入肥皂水。
查看更多完整答案,请扫码查看


