第102页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
- 第107页
- 第108页
- 第109页
- 第110页
- 第111页
- 第112页
- 第113页
- 第114页
- 第115页
- 第116页
- 第117页
- 第118页
- 第119页
- 第120页
- 第121页
- 第122页
8.(2024.广元中考)乙醇(C2H5OH)是常用的燃料。现有4.6g乙醇与一定量氧气混合于密闭容器内,在一定条件下反应物全部转化为一氧化碳、二氧化碳和水,恢复到室温,测得所得气体中氧元素的质量分数为70%,则参加反应的氧气的质量为( )
A.6.4g B.8.0g C.8.8g D.9.6g
A.6.4g B.8.0g C.8.8g D.9.6g
答案:
C [解析]现有4.6g乙醇与一定量氧气混合于密闭容器内,在一定条件下反应物全部转化为一氧化碳、二氧化碳和水,4.6g乙醇(C₂H₅OH)中碳元素的质量为:4.6g×$\frac{24}{46}$×100% = 2.4g,氢元素的质量为:4.6g×$\frac{6}{46}$×100% = 0.6g,恢复到室温,测得所得气体是一氧化碳和二氧化碳的混合气体,其中氧元素的质量分数为70%,则碳元素的质量分数为:100% - 70% = 30%,所以混合气体的质量为:2.4g÷30% = 8g,乙醇燃烧生成水的质量为:0.6g÷$\frac{2}{18}$ = 5.4g,根据质量守恒定律可知,参加反应的氧气的质量为:8g + 5.4g - 4.6g = 8.8g。故选:C。
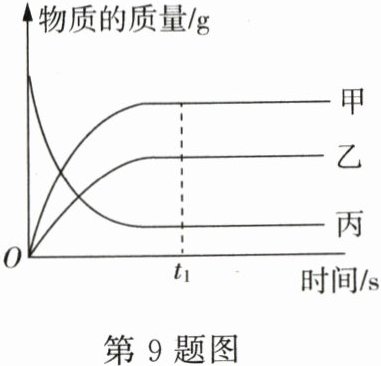
9.易错题如图是某个化学反应中各物质的质量与时间的变化关系,下列对此变化的描述中,正确的是( )
A.充分反应后,乙的质量 + 丙的质量 = 甲的质量
B.物质甲的相对分子质量比物质乙的大
C.此化学反应不遵守质量守恒定律
D.此化学反应是分解反应
A.充分反应后,乙的质量 + 丙的质量 = 甲的质量
B.物质甲的相对分子质量比物质乙的大
C.此化学反应不遵守质量守恒定律
D.此化学反应是分解反应

答案:
D [解析]A. 充分反应后应该是丙减小的质量等于甲和乙的质量之和,故选项A说法错误,不符合题意;
B. 不能确定物质甲的相对分子质量比物质乙的大,故选项B说法错误,不符合题意;
C. 只要是化学反应,就遵守质量守恒定律,故选项C说法错误,不符合题意;
D. 由图中信息可知,反应过程中,丙的质量减小,是反应物,甲和乙的质量都增大,都是生成物,此化学反应符合“多变一”的特征,是分解反应,故选项D说法正确,符合题意。
故选:D。
B. 不能确定物质甲的相对分子质量比物质乙的大,故选项B说法错误,不符合题意;
C. 只要是化学反应,就遵守质量守恒定律,故选项C说法错误,不符合题意;
D. 由图中信息可知,反应过程中,丙的质量减小,是反应物,甲和乙的质量都增大,都是生成物,此化学反应符合“多变一”的特征,是分解反应,故选项D说法正确,符合题意。
故选:D。
10.在一个密闭容器内有X、Y、Z、Q四种物质,在一定条件下充分反应,测得反应前后各物质的质量如下:

下列说法中不正确的是( )
A.X中未测值为零
B.该反应遵守质量守恒定律
C.该反应为分解反应
D.若Q为氧气,则该反应为氧化反应

下列说法中不正确的是( )
A.X中未测值为零
B.该反应遵守质量守恒定律
C.该反应为分解反应
D.若Q为氧气,则该反应为氧化反应
答案:
C [解析]由表中数据分析可知,反应前后Y的质量增加了21g - 10g = 11g,故Y是生成物,生成的Y的质量为11g;同理可以确定Z是生成物,生成的Z的质量为10g - 1g = 9g;Q是反应物,参加反应的Q的质量为25g - 9g = 16g。
A. 由质量守恒定律可知,X应是反应物,且参加反应的X的质量为11g + 9g - 16g = 4g,故未测值为4g - 4g = 0g,故选项A正确,不符合题意;
B. 该反应属于化学反应,遵守质量守恒定律,故选项B正确,不符合题意;
C. 该反应的反应物是X和Q,生成物是Y和Z,不符合“一变多”的特征,不属于分解反应,故选项C错误,符合题意;
D. 该反应的反应物是X和Q,若Q为氧气,则该反应为物质X与氧气的反应,属于氧化反应,故选项D正确,不符合题意。
故选:C。
A. 由质量守恒定律可知,X应是反应物,且参加反应的X的质量为11g + 9g - 16g = 4g,故未测值为4g - 4g = 0g,故选项A正确,不符合题意;
B. 该反应属于化学反应,遵守质量守恒定律,故选项B正确,不符合题意;
C. 该反应的反应物是X和Q,生成物是Y和Z,不符合“一变多”的特征,不属于分解反应,故选项C错误,符合题意;
D. 该反应的反应物是X和Q,若Q为氧气,则该反应为物质X与氧气的反应,属于氧化反应,故选项D正确,不符合题意。
故选:C。
11.用化学用语填空:
(1)2个氮分子:________; (2)m个铝离子:________;
(3)硫酸铁:________; (4)能保持氧气化学性质的最小粒子:________。
(1)2个氮分子:________; (2)m个铝离子:________;
(3)硫酸铁:________; (4)能保持氧气化学性质的最小粒子:________。
答案:
(1) 2N₂
(2) mAl³⁺
(3) Fe₂(SO₄)₃
(4) O₂
[解析]
(1) 氮气是双原子分子,故表示为N₂,2个氮分子则表示为2N₂;
(2) 铝离子表示为Al³⁺,m个铝离子则表示为mAl³⁺;
(3) 硫酸铁表示为Fe₂(SO₄)₃;
(4) 氧气由氧分子构成,保持氧气化学性质的最小粒子是氧分子,故表示为O₂。
(1) 2N₂
(2) mAl³⁺
(3) Fe₂(SO₄)₃
(4) O₂
[解析]
(1) 氮气是双原子分子,故表示为N₂,2个氮分子则表示为2N₂;
(2) 铝离子表示为Al³⁺,m个铝离子则表示为mAl³⁺;
(3) 硫酸铁表示为Fe₂(SO₄)₃;
(4) 氧气由氧分子构成,保持氧气化学性质的最小粒子是氧分子,故表示为O₂。
12.写出下列化学符号中数字“2”的含义:
(1)Fe²⁺:______________________________;
(2)$\stackrel{+2}{Mg}$O:______________________________。
(1)Fe²⁺:______________________________;
(2)$\stackrel{+2}{Mg}$O:______________________________。
答案:
(1) 一个亚铁离子带两个单位的正电荷
(2) 氧化镁中氧元素的化合价为 - 2价
[解析]
(1) 离子符号右上角的数字表示每个离子所带的电荷数,Fe²⁺中的“2”表示一个亚铁离子带两个单位的正电荷;
(2) 元素符号正上方的数字表示元素的化合价,MgO中氧元素上方的“ - 2”表示氧化镁中氧元素的化合价为 - 2价。
(1) 一个亚铁离子带两个单位的正电荷
(2) 氧化镁中氧元素的化合价为 - 2价
[解析]
(1) 离子符号右上角的数字表示每个离子所带的电荷数,Fe²⁺中的“2”表示一个亚铁离子带两个单位的正电荷;
(2) 元素符号正上方的数字表示元素的化合价,MgO中氧元素上方的“ - 2”表示氧化镁中氧元素的化合价为 - 2价。
13.根据下列反应事实写出相应的化学方程式:
(1)红磷在空气中燃烧:______________________________;
(2)实验室用双氧水和二氧化锰制取氧气:______________________________;
(3)铁在氧气中燃烧,火星四射:______________________________;
(4)加热高锰酸钾制取氧气:______________________________。
(1)红磷在空气中燃烧:______________________________;
(2)实验室用双氧水和二氧化锰制取氧气:______________________________;
(3)铁在氧气中燃烧,火星四射:______________________________;
(4)加热高锰酸钾制取氧气:______________________________。
答案:
(1) 4P + 5O₂$\stackrel{点燃}{=\!=\!=}$2P₂O₅
(2) 2H₂O₂$\stackrel{MnO₂}{=\!=\!=}$2H₂O + O₂↑
(3) 3Fe + 2O₂$\stackrel{点燃}{=\!=\!=}$Fe₃O₄
(4) 2KMnO₄$\stackrel{\triangle}{=\!=\!=}$K₂MnO₄ + MnO₂ + O₂↑
(1) 4P + 5O₂$\stackrel{点燃}{=\!=\!=}$2P₂O₅
(2) 2H₂O₂$\stackrel{MnO₂}{=\!=\!=}$2H₂O + O₂↑
(3) 3Fe + 2O₂$\stackrel{点燃}{=\!=\!=}$Fe₃O₄
(4) 2KMnO₄$\stackrel{\triangle}{=\!=\!=}$K₂MnO₄ + MnO₂ + O₂↑
14.一定质量的丙醇(C3H8O)和氧气在密闭容器中充分燃烧,生成的CO2和CO的质量比为22:7。该反应的化学方程式为________________,生成的二氧化碳和水的质量比为________。
答案:
C₃H₈O + 4O₂$\stackrel{点燃}{=\!=\!=}$2CO₂ + CO + 4H₂O 11:9
[解析]生成的CO₂和CO的质量比为22:7,二氧化碳和一氧化碳的化学计量数之比为$\frac{22}{44}$:$\frac{7}{28}$ = 2:1,该反应的化学方程式为C₃H₈O + 4O₂$\stackrel{点燃}{=\!=\!=}$2CO₂ + CO + 4H₂O,生成的二氧化碳和水的质量比为(44×2):(18×4) = 11:9。
[解析]生成的CO₂和CO的质量比为22:7,二氧化碳和一氧化碳的化学计量数之比为$\frac{22}{44}$:$\frac{7}{28}$ = 2:1,该反应的化学方程式为C₃H₈O + 4O₂$\stackrel{点燃}{=\!=\!=}$2CO₂ + CO + 4H₂O,生成的二氧化碳和水的质量比为(44×2):(18×4) = 11:9。
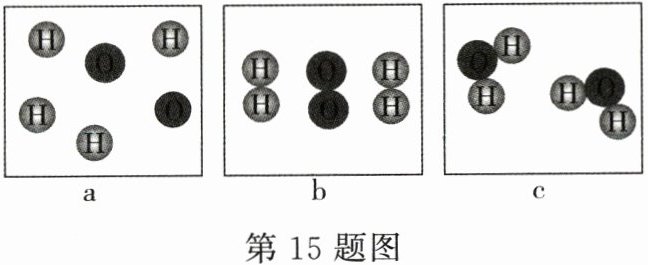
15.2400℃时水能分解,其微观过程可用以下示意图表示,请按要求回答下列问题:
(1)水分解过程示意图正确的排列顺序是________(填字母);
(2)2400℃时水分解的客观事实说明________(填序号)。
①通常情况下水的性质稳定
②水是一种元素
③化学变化需要一定条件
(1)水分解过程示意图正确的排列顺序是________(填字母);
(2)2400℃时水分解的客观事实说明________(填序号)。
①通常情况下水的性质稳定
②水是一种元素
③化学变化需要一定条件

答案:
(1) cab
(2) ①③
[解析]
(1) 由化学变化的实质可知,水分解的过程是:水分子分成氢原子和氧原子,然后每两个氢原子构成一个氢分子,每两个氧原子构成一个氧分子,故填:cab。
(2) ①通常情况下水的性质稳定,温度达到2400℃时才会分解,选项说法正确;②水是一种物质,而不是一种元素,选项说法错误;③通常情况下水的性质稳定,温度达到2400℃时才会分解,说明化学变化需要一定条件,选项说法正确。故填:①③。
(1) cab
(2) ①③
[解析]
(1) 由化学变化的实质可知,水分解的过程是:水分子分成氢原子和氧原子,然后每两个氢原子构成一个氢分子,每两个氧原子构成一个氧分子,故填:cab。
(2) ①通常情况下水的性质稳定,温度达到2400℃时才会分解,选项说法正确;②水是一种物质,而不是一种元素,选项说法错误;③通常情况下水的性质稳定,温度达到2400℃时才会分解,说明化学变化需要一定条件,选项说法正确。故填:①③。
查看更多完整答案,请扫码查看


