第112页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
- 第107页
- 第108页
- 第109页
- 第110页
- 第111页
- 第112页
- 第113页
- 第114页
- 第115页
- 第116页
- 第117页
- 第118页
- 第119页
1. 如图甲是天宫课堂中航天员王亚平给我们演示的“冰雪球”实验,通过航天员的介绍,小科同学知道了这里所用的溶液是过饱和的乙酸钠溶液(一定温度、压力下,当溶液中溶质的质量已经超过该温度、压力下该溶质的溶解度,而溶质不析出的现象叫过饱和现象)。在这种溶液中只要有点结晶核颗粒或振动,就能迅速打破原本的过饱和状态,析出大量的晶体,同时还会释放出大量的热量。请根据题干中的信息,回答下列问题:

(1) 由题可知,“冰雪球”是因为
(2) 市面上有一种掰掰热暖宝宝(里面装有过饱和的乙酸钠溶液)如图乙所示,只需要用力掰动袋中金属片,就能达到发热取暖的效果,掰动金属片的目的是
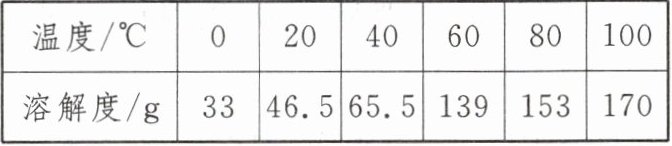
(3) 下表是乙酸钠的溶解度,小科先在 $100^{\circ}C$ 水中配制其饱和溶液,一定条件下,降温到 $40^{\circ}C$,此时没有晶体析出,此时溶液中溶质质量分数为

(1) 由题可知,“冰雪球”是因为
溶液结晶
(填“溶液结晶”或“溶液凝固”)而形成的。(2) 市面上有一种掰掰热暖宝宝(里面装有过饱和的乙酸钠溶液)如图乙所示,只需要用力掰动袋中金属片,就能达到发热取暖的效果,掰动金属片的目的是
产生振动,迅速打破原本的过饱和状态,析出大量的晶体,同时还会释放出大量的热量
。(3) 下表是乙酸钠的溶解度,小科先在 $100^{\circ}C$ 水中配制其饱和溶液,一定条件下,降温到 $40^{\circ}C$,此时没有晶体析出,此时溶液中溶质质量分数为
63.0%
(精确到 $0.1\%$)。
答案:
1.
(1)溶液结晶
(2)产生振动,迅速打破原本的过饱和状态,析出大量的晶体,同时还会释放出大量的热量
(3)63.0%
(1)溶液结晶
(2)产生振动,迅速打破原本的过饱和状态,析出大量的晶体,同时还会释放出大量的热量
(3)63.0%
2. 小组进行发热袋的模型制作,通过调查生活中的相关商品,提出了几种课本外的其他模型。
模型一 一种自热饮料的原理简图
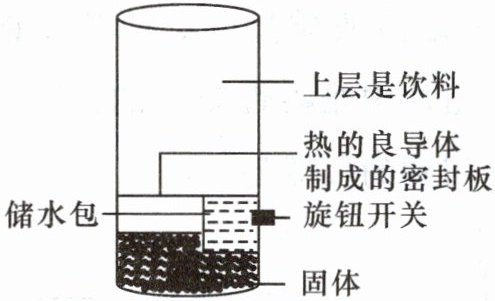
(1) 该装置的优点是可以通过更换瓶底固体的种类来实现对饮料的加热或降温,若想要在冬天对饮料进行加热,其罐底的固体可能是
A. 氢氧化钠 B. 硝酸铵 C. 氯化钠
模型二 自热火锅的原理简图
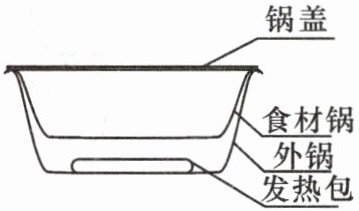
(2) 自热火锅的加热原理是利用发热包内的物质(生石灰等)与水接触,释放出热量,从而使上层食材锅内的食物吸收热量后温度升高。请写出该反应的化学方程式:
模型三 简单的铁粉发热包
(3) 简单的铁粉发热包中主要包括铁粉、活性炭、氯化钠和水,依靠铁的锈蚀放出热量。在阴凉干燥环境下密封保存,其保质期可达一年甚至更长,这说明铁的锈蚀必须要有水和
模型一 一种自热饮料的原理简图

(1) 该装置的优点是可以通过更换瓶底固体的种类来实现对饮料的加热或降温,若想要在冬天对饮料进行加热,其罐底的固体可能是
A
(填字母),可以用金属作为密封板,这是因为金属具有良好的导热性
。A. 氢氧化钠 B. 硝酸铵 C. 氯化钠
模型二 自热火锅的原理简图

(2) 自热火锅的加热原理是利用发热包内的物质(生石灰等)与水接触,释放出热量,从而使上层食材锅内的食物吸收热量后温度升高。请写出该反应的化学方程式:
CaO+H₂O=Ca(OH)₂
,外锅和食材锅几乎没有直接接触,但食材锅依旧可以被快速加热,这是因为外锅中的水因升温汽化为水蒸气,热的水蒸气遇到冷的食材锅液化放出热量,使得食材锅被加热
。模型三 简单的铁粉发热包
(3) 简单的铁粉发热包中主要包括铁粉、活性炭、氯化钠和水,依靠铁的锈蚀放出热量。在阴凉干燥环境下密封保存,其保质期可达一年甚至更长,这说明铁的锈蚀必须要有水和
氧气
参与。铁粉发热包的优点是可以根据调节其组成成分和成分占比来控制加热的时长和单位时间放热的多少,既可以制作长期发热但温度适宜的暖宝宝和蒸汽眼罩,也可以制作需要瞬间放出大量热来加热食品的加热包。
答案:
2.
(1)A 导热性
(2)CaO+H₂O=Ca(OH)₂ 外锅中的水因升温汽化为水蒸气,热的水蒸气遇到冷的食材锅液化放出热量,使得食材锅被加热
(3)氧气
(1)A 导热性
(2)CaO+H₂O=Ca(OH)₂ 外锅中的水因升温汽化为水蒸气,热的水蒸气遇到冷的食材锅液化放出热量,使得食材锅被加热
(3)氧气
查看更多完整答案,请扫码查看


