第6页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
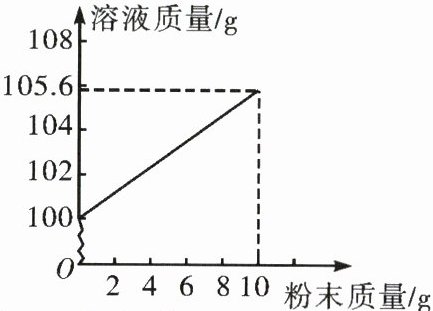
25.(9分)复方碳酸氢钠片是一种常用的抗酸剂药物,口服后能迅速中和胃酸,用于缓解胃酸过多引起的胃痛等症状。复方碳酸氢钠片的主要成分是碳酸氢钠(其他成分可溶于水但不参与反应),碳酸氢钠与盐酸反应的化学方程式为$NaHCO_3+HCl= NaCl+H_2O+CO_2↑。$某科学兴趣小组为了测定药片中碳酸氢钠的含量做了以下实验:先将复方碳酸氢钠片制成粉末,取10 g分多次放入盛有100 g稀盐酸的烧杯中充分反应。测出加入的粉末质量和反应后的溶液质量,两者质量关系如图所示。
(1)实验后,兴趣小组又往烧杯中加入少量粉末,观察到______,说明上述实验结束时稀盐酸过量。
(2)计算复方碳酸氢钠片中碳酸氢钠的含量。
(3)计算10 g粉末与稀盐酸反应后所得氯化钠溶液的溶质质量分数。(计算结果精确到0.1%)

(1)实验后,兴趣小组又往烧杯中加入少量粉末,观察到______,说明上述实验结束时稀盐酸过量。
(2)计算复方碳酸氢钠片中碳酸氢钠的含量。
(3)计算10 g粉末与稀盐酸反应后所得氯化钠溶液的溶质质量分数。(计算结果精确到0.1%)
答案:
(1)有气泡产生
(2)解:由图可知,加入10g粉末后溶液质量为105.6g,根据质量守恒定律,生成二氧化碳质量为10g+100g-105.6g=4.4g。
设10g粉末中碳酸氢钠质量为x,生成氯化钠质量为y。
$NaHCO_3+HCl=NaCl+H_2O+CO_2↑$
84 58.5 44
x y 4.4g
$\frac{84}{x}=\frac{44}{4.4g}$,解得x=8.4g
碳酸氢钠含量为$\frac{8.4g}{10g}×100\%=84\%$
(3)$\frac{58.5}{y}=\frac{44}{4.4g}$,解得y=5.85g
反应后溶液质量为105.6g,溶质质量分数为$\frac{5.85g}{105.6g}×100\%\approx5.5\%$
(2)复方碳酸氢钠片中碳酸氢钠的含量为84%;
(3)所得氯化钠溶液的溶质质量分数为5.5%。
(1)有气泡产生
(2)解:由图可知,加入10g粉末后溶液质量为105.6g,根据质量守恒定律,生成二氧化碳质量为10g+100g-105.6g=4.4g。
设10g粉末中碳酸氢钠质量为x,生成氯化钠质量为y。
$NaHCO_3+HCl=NaCl+H_2O+CO_2↑$
84 58.5 44
x y 4.4g
$\frac{84}{x}=\frac{44}{4.4g}$,解得x=8.4g
碳酸氢钠含量为$\frac{8.4g}{10g}×100\%=84\%$
(3)$\frac{58.5}{y}=\frac{44}{4.4g}$,解得y=5.85g
反应后溶液质量为105.6g,溶质质量分数为$\frac{5.85g}{105.6g}×100\%\approx5.5\%$
(2)复方碳酸氢钠片中碳酸氢钠的含量为84%;
(3)所得氯化钠溶液的溶质质量分数为5.5%。
查看更多完整答案,请扫码查看


