第12页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
25.(12分)市场上有碳酸氢钠片、铝碳酸镁片[化学式:$\mathrm{Al_2Mg_6(OH)_{16}CO_3 \cdot 4H_2O}$,相对分子质量为602]等治疗胃酸(主要成分为盐酸)过多症的药物。
[已知]碳酸氢钠与盐酸反应原理为$\mathrm{NaHCO_3} + \mathrm{HCl} \xlongequal{} \mathrm{NaCl} + \mathrm{H_2O} + \mathrm{CO_2}\uparrow$;铝碳酸镁片与盐酸反应原理为$\mathrm{Al_2Mg_6(OH)_{16}CO_3 \cdot 4H_2O} + 18\mathrm{HCl} \xlongequal{} 2\mathrm{AlCl_3} + 6\mathrm{MgCl_2} + \mathrm{CO_2}\uparrow + 21\mathrm{H_2O}$。
(1)结合上述化学方程式分析,铝碳酸镁片起到降低酸性效果的离子是碳酸根离子和______(填离子符号)。
(2)若上述两种药片各服用1 g,试通过计算分析哪种药片降低酸性能力更强。(结果保留2位小数)
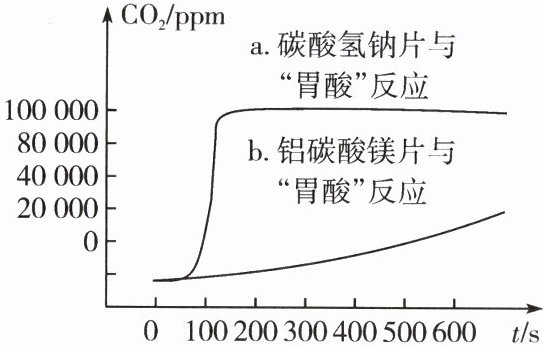
(3)在两份各120 mL相同的稀盐酸(模拟胃酸)中分别加入4 g碳酸氢钠片和铝碳酸镁片反应,得到产生二氧化碳的浓度与时间的关系如图所示。请你结合图像分析:若是胃溃疡患者要避免出现胃内气体过多导致胃胀,引起胃穿孔等症状,你认为医生会建议这位患者不宜过多服用上述哪种药物?说明你的理由。
[已知]碳酸氢钠与盐酸反应原理为$\mathrm{NaHCO_3} + \mathrm{HCl} \xlongequal{} \mathrm{NaCl} + \mathrm{H_2O} + \mathrm{CO_2}\uparrow$;铝碳酸镁片与盐酸反应原理为$\mathrm{Al_2Mg_6(OH)_{16}CO_3 \cdot 4H_2O} + 18\mathrm{HCl} \xlongequal{} 2\mathrm{AlCl_3} + 6\mathrm{MgCl_2} + \mathrm{CO_2}\uparrow + 21\mathrm{H_2O}$。
(1)结合上述化学方程式分析,铝碳酸镁片起到降低酸性效果的离子是碳酸根离子和______(填离子符号)。
(2)若上述两种药片各服用1 g,试通过计算分析哪种药片降低酸性能力更强。(结果保留2位小数)
(3)在两份各120 mL相同的稀盐酸(模拟胃酸)中分别加入4 g碳酸氢钠片和铝碳酸镁片反应,得到产生二氧化碳的浓度与时间的关系如图所示。请你结合图像分析:若是胃溃疡患者要避免出现胃内气体过多导致胃胀,引起胃穿孔等症状,你认为医生会建议这位患者不宜过多服用上述哪种药物?说明你的理由。

答案:
(1)OH⁻
(2)解:设1g碳酸氢钠能消耗HCl的质量为x
NaHCO₃ + HCl = NaCl + H₂O + CO₂↑
84 36.5
1g x
84/36.5 = 1g/x
x ≈ 0.43g
设1g铝碳酸镁能消耗HCl的质量为y
Al₂Mg₆(OH)₁₆CO₃·4H₂O + 18HCl = 2AlCl₃ + 6MgCl₂ + CO₂↑ + 21H₂O
602 657
1g y
602/657 = 1g/y
y ≈ 1.09g
1.09g > 0.43g,铝碳酸镁片降低酸性能力更强。
(3)碳酸氢钠片;由图像可知,相同时间内碳酸氢钠片反应产生CO₂的浓度远大于铝碳酸镁片,会导致胃内气体过多。
(1)OH⁻
(2)解:设1g碳酸氢钠能消耗HCl的质量为x
NaHCO₃ + HCl = NaCl + H₂O + CO₂↑
84 36.5
1g x
84/36.5 = 1g/x
x ≈ 0.43g
设1g铝碳酸镁能消耗HCl的质量为y
Al₂Mg₆(OH)₁₆CO₃·4H₂O + 18HCl = 2AlCl₃ + 6MgCl₂ + CO₂↑ + 21H₂O
602 657
1g y
602/657 = 1g/y
y ≈ 1.09g
1.09g > 0.43g,铝碳酸镁片降低酸性能力更强。
(3)碳酸氢钠片;由图像可知,相同时间内碳酸氢钠片反应产生CO₂的浓度远大于铝碳酸镁片,会导致胃内气体过多。
查看更多完整答案,请扫码查看


