2025年成才之路高中新课程学习指导高中化学选择性必修第三册人教版
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2025年成才之路高中新课程学习指导高中化学选择性必修第三册人教版 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
第43页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
- 第107页
- 第108页
- 第109页
- 第110页
- 第111页
- 第112页
- 第113页
- 第114页
- 第115页
- 第116页
- 第117页
- 第118页
- 第119页
- 第120页
- 第121页
- 第122页
- 第123页
- 第124页
- 第125页
- 第126页
- 第127页
- 第128页
- 第129页
- 第130页
- 第131页
- 第132页
- 第133页
- 第134页
- 第135页
- 第136页
- 第137页
- 第138页
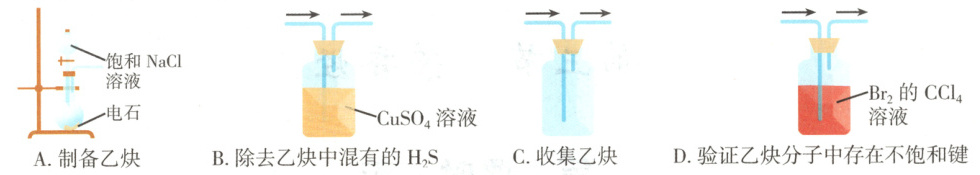
1.(2024·广东深圳高二期末)在实验室进行乙炔的制备、净化、收集及检验实验(“→”表示气流方向)。下列装置难以达到实验目的的是
(
(
C
)
答案:
1.C 实验室用电石和饱和食盐水反应制备乙炔,可以获得平稳的气流,故不选A;H₂S和硫酸铜反应生成硫化铜沉淀和硫酸,用硫酸铜溶液除去乙炔中混有的H₂S,故不选B;乙炔密度略小于空气,不能用向上排空气法收集乙炔,故选C;乙炔和溴发生加成反应,用溴的四氯化碳溶液验证乙炔分子中存在不饱和键,故不选D。
2.(2024·安徽马鞍山高二期中)如图是制备和研究乙炔性质的实验装置图,有关说法不正确的是
(
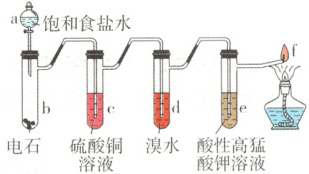
A.用蒸馏水替代a中饱和食盐水产生的乙炔更为纯净
B.c中溶液(过量)的作用是除去影响后续实验的杂质
C.d、e中溶液褪色的原理不同
D.f处产生明亮、伴有浓烟的火焰
(
A
)
A.用蒸馏水替代a中饱和食盐水产生的乙炔更为纯净
B.c中溶液(过量)的作用是除去影响后续实验的杂质
C.d、e中溶液褪色的原理不同
D.f处产生明亮、伴有浓烟的火焰
答案:
2.A 在试管b中饱和食盐水与电石发生反应CaC₂ + 2H₂O ⟶ Ca(OH)₂ + C₂H₂↑,蒸馏水代替饱和食盐水会使反应速率加快,不容易控制,故A错误;c中硫酸铜溶液除去杂质硫化氢,防止硫化氢对后续实验产生影响,故B正确;d中溴水与乙炔发生加成反应生成的有机产物为1,1,2,2-四溴乙烷,e中乙炔与高锰酸钾发生氧化反应,酸性高锰酸钾溶液褪色可说明乙炔能被氧化,反应原理不同,故C正确;e中已经排除杂质的干扰,f处若有剩余气体应为乙炔,燃烧放出明亮火焰,伴有浓烟,故D正确。
1.(2024·陕西高二期末)有5种物质:①甲烷 ②环己烯 ③聚乙炔 ④1,3-丁二烯 ⑤聚乙烯,既能使酸性高锰酸钾溶液褪色,又能使溴水因反应而褪色的是
(
A.①③④
B.②④⑤
C.②③④
D.①②③④
(
C
)A.①③④
B.②④⑤
C.②③④
D.①②③④
答案:
1.C ①甲烷属于饱和烃,既不能和酸性高锰酸钾溶液反应,也不和溴水反应;②环己烯分子中有碳碳双键,可以被酸性高锰酸钾溶液氧化使其褪色,也可以和溴水中的溴发生加成反应使溴水褪色;③乙炔聚合生成的聚乙炔含有碳碳双键,可以被酸性高锰酸钾溶液氧化使其褪色,也可以和溴水中的溴发生加成反应使溴水褪色;④1,3-丁二烯分子中有碳碳双键,可以被酸性高锰酸钾溶液氧化使其褪色,也可以和溴水中的溴发生加成反应使溴水褪色;⑤聚乙烯中没有碳碳双键,既不能和酸性高锰酸钾溶液反应,也不和溴水反应。故选C。
2.(2024·广东梅州高二期中)乙炔在氧气中燃烧时放出大量的热,氧炔焰的温度可达3 000 ℃以上,因此常用于焊接或切割金属。下列有关乙炔的说法错误的是
(
A.电子式为$\mathrm{H:C::C:H}$
B.含碳量约为92.3%
C.是最简单的炔烃
D.能使溴水褪色,原因是乙炔与溴发生了萃取
(
D
)A.电子式为$\mathrm{H:C::C:H}$
B.含碳量约为92.3%
C.是最简单的炔烃
D.能使溴水褪色,原因是乙炔与溴发生了萃取
答案:
2.D 乙炔电子式为H:C⋮⋮C:H,A正确;乙炔中含碳量:$\frac{12×2}{12×2 + 2}×100% ≈ 92.3%,$B正确;乙炔是最简单的炔烃,C正确;乙炔能使溴水褪色,是因为乙炔与溴水发生加成反应,D错误。
3.(2024·广东佛山高二期末)乙炔的实验室制备及性质检验装置如图所示。下列说法错误的是
(

A.饱和食盐水的作用是降低反应速率
B.可用酸性高锰酸钾溶液替换$\mathrm{CuSO_4}$溶液
C.溴的$\mathrm{CCl_4}$溶液褪色,发生加成反应
D.可采用点燃的方法除尾气,观察到有黑烟产生
(
B
)
A.饱和食盐水的作用是降低反应速率
B.可用酸性高锰酸钾溶液替换$\mathrm{CuSO_4}$溶液
C.溴的$\mathrm{CCl_4}$溶液褪色,发生加成反应
D.可采用点燃的方法除尾气,观察到有黑烟产生
答案:
3.B 碳化钙和水反应生成乙炔,生成的乙炔中含有硫化氢等杂质,利用硫酸铜溶液除去杂质,利用溴的四氯化碳溶液检验乙炔的性质,据此解答。碳化钙与水反应剧烈,分液漏斗中装的是饱和氯化钠溶液,可以减缓反应速率,故A正确;制备的乙炔中含有杂质硫化氢,制取纯净乙炔应除去杂质硫化氢,硫酸铜溶液与硫化氢反应生成硫化铜沉淀和硫酸,可以用于吸收硫化氢,但由于乙炔也能被酸性高锰酸钾溶液氧化,所以不能用酸性高锰酸钾溶液替换CuSO₄溶液,故B错误;乙炔含有碳碳三键,能与溴发生加成反应,从而使溴的CCl₄溶液褪色,故C正确;乙炔属于可燃性气体,含碳量高,所以可采用点燃的方法除尾气,观察到有黑烟产生,故D正确。
查看更多完整答案,请扫码查看


