第85页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
1. 除杂原则
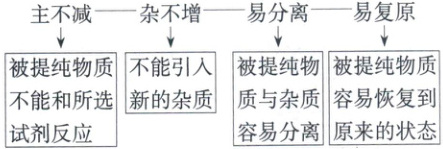
2. 常见物质的除杂
(1) 气体的除杂[(详见微专题(一) 气体的制取、检验与净化)]
(2) 固体的除杂
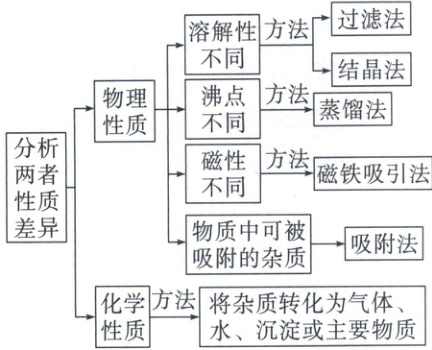
(3) 液体的除杂(以除去 NaCl 溶液中的 Na₂CO₃为例)
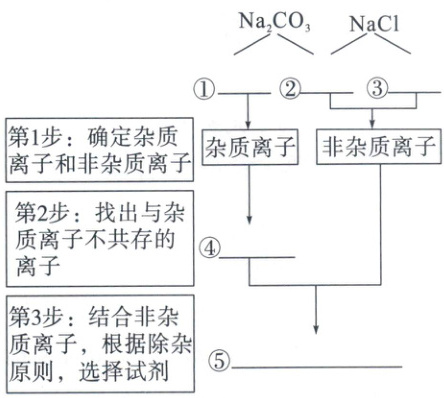

2. 常见物质的除杂
(1) 气体的除杂[(详见微专题(一) 气体的制取、检验与净化)]
(2) 固体的除杂

(3) 液体的除杂(以除去 NaCl 溶液中的 Na₂CO₃为例)

答案:
①$\text{CO}_{3}^{2-}$ ②$\text{Na}^{+}$ ③$\text{Cl}^{-}$ ④$\text{Ca}^{2+}$ ⑤$\text{CaCl}_{2}$ (或④$\text{Ba}^{2+}$ ⑤$\text{BaCl}_{2}$ 或④$\text{H}^{+}$ ⑤$\text{HCl}$)
1. (2025·烟台)物质的检验、鉴别、除杂是化学研究的重要方法。下列实验方案能达到目的的是(
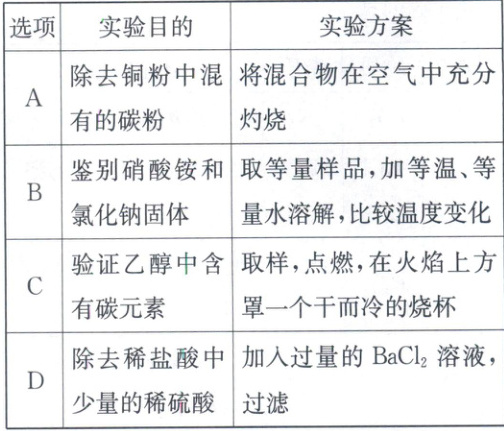
B
)
答案:
1.B [解析]碳粉、铜粉在空气中充分灼烧,分别生成二氧化碳氧化铜,不仅能把杂质除去,也会把原物质除去,不符合除杂
原则,故A错误;硝酸铵溶于水吸热,氯化钠溶于水无明显吸放热现象,取等量样品,加等温、等量水溶解,比较温度变化,温度降低的是硝酸铵固体,温度几乎不变的是氯化钠固体,实验方案能达到目的,故B正确;含碳物质充分燃烧生成二氧化碳,应该用澄清石灰水来检验二氧化碳;取样,点燃,在火焰上方罩一个干而冷的烧杯,烧杯内壁出现水雾,说明生成了水,证明乙醇中一定含有氢元素,无法确定是否含有碳元素,故C错误;稀硫酸能与过量的$BaCl_{2}$ 溶液反应生成硫酸钡沉淀和氯化氢,能除去杂质但引入了新的杂质氯化钡(过量),不符合除杂原则,故D错误。
原则,故A错误;硝酸铵溶于水吸热,氯化钠溶于水无明显吸放热现象,取等量样品,加等温、等量水溶解,比较温度变化,温度降低的是硝酸铵固体,温度几乎不变的是氯化钠固体,实验方案能达到目的,故B正确;含碳物质充分燃烧生成二氧化碳,应该用澄清石灰水来检验二氧化碳;取样,点燃,在火焰上方罩一个干而冷的烧杯,烧杯内壁出现水雾,说明生成了水,证明乙醇中一定含有氢元素,无法确定是否含有碳元素,故C错误;稀硫酸能与过量的$BaCl_{2}$ 溶液反应生成硫酸钡沉淀和氯化氢,能除去杂质但引入了新的杂质氯化钡(过量),不符合除杂原则,故D错误。
2. (2025·河北)下列实验方案不能达到实验目的的是(
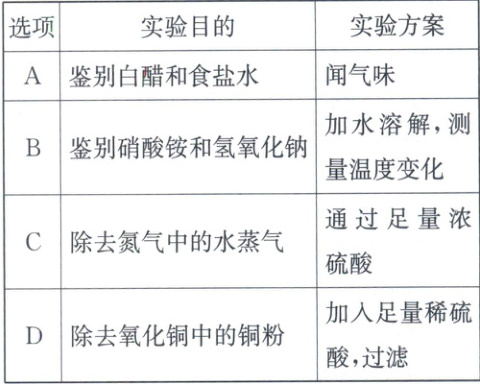
D
)
答案:
2.D [解析]白醋有特殊气味,食盐水无味,可通过闻气味鉴别,A不符合题意;硝酸铵溶于水吸热,温度降低,氢氧化钠溶于水放热,温度升高,通过加水溶解测量温度变化可鉴别,B不符合题意;浓硫酸具有吸水性,通过足量浓硫酸可除去氮气中的水蒸气,C不符合题意;加入足量稀硫酸,氧化铜能与稀硫酸反应,铜粉不与稀硫酸反应,不符合除杂原则,D符合题意。
3. (2025·云南)下列实验方案合理的是(
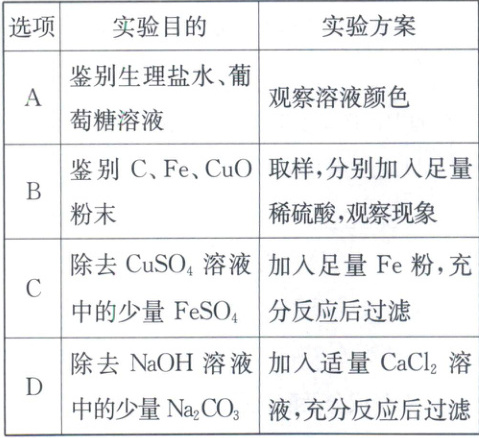
B
)
答案:
3.B [解析]生理盐水和葡萄糖溶液均为无色透明液体,不能通过观察溶液颜色的方法鉴别,故A不合理;取样,分别加入足量稀$H_{2}SO_{4}$,C与稀$H_{2}SO_{4}$ 不反应,无明显现象;Fe与稀$H_{2}SO_{4}$反应生成$FeSO_{4}$和$H_{2}$,有气泡产生,溶液由无色变为浅绿色;$CuO$与稀$H_{2}SO_{4}$反应生成$CuSO_{4}$和$H_{2}O$,固体逐渐溶解,溶液由无色变为蓝色,现象不同,能鉴别C、Fe、CuO粉末,故B合理;加入足量Fe粉,Fe与$CuSO_{4}$反应生成Cu和$FeSO_{4}$,除去了原物质$CuSO_{4}$,故C不合理;加入适量$CaCl_{2}$溶液,$Na_{2}CO_{3}$与$CaCl_{2}$反应生成$CaCO_{3}$沉淀和NaCl,充分反应后过滤除去$CaCO_{3}$,能除去杂质$Na_{2}CO_{3}$,但会引入新杂质NaCl,故D不合理。
查看更多完整答案,请扫码查看


