第84页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
3. 鉴别是重要的实验技能。分别鉴别两组物质:①C、CuO;②稀 H₂SO₄、Na₂CO₃ 溶液,都能选用的试剂是 (
A.O₂
B.NaOH 溶液
C.铁片
D.稀 H₂SO₄
D
)A.O₂
B.NaOH 溶液
C.铁片
D.稀 H₂SO₄
答案:
3.D
4. (2025·黑龙江龙东地区)下列实验方案能达到实验目的的是 (
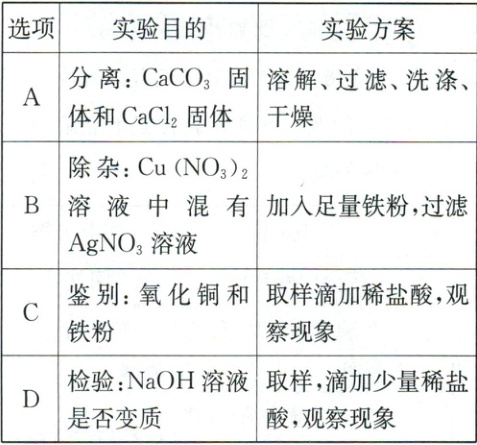
C
)
答案:
4.C [解析]A.碳酸钙难溶于水,氯化钙易溶于水,可通过溶解、过滤、洗涤、干燥得到碳酸钙固体,然后蒸发结晶才能得到氯化钙固体,题中方案达不到分离的目的,不符合题意;B.加入足量铁粉,铁和硝酸银溶液反应生成硝酸亚铁和银,铁与硝酸铜溶液反应生成硝酸亚铁和铜,不但除去了杂质,也除去了原物质,不符合题意;C.取样滴加稀盐酸,观察现象,氧化铜和稀盐酸反应生成氯化铜和水,黑色固体逐渐溶解,溶液由无色变为蓝色,铁和稀盐酸反应生成氯化亚铁和氢气,产生气泡,且得到浅绿色溶液,现象不同,可以鉴别,符合题意;D.氢氧化钠能与空气中的二氧化碳反应生成碳酸钠和水,从而变质,如果氢氧化钠部分变质,滴加少量稀盐酸,稀盐酸先与氢氧化钠反应生成氯化钠和水,待氢氧化钠完全反应后,碳酸钠和稀盐酸反应生成氯化钠、二氧化碳和水,因为稀盐酸的量太少,即使氢氧化钠溶液部分变质也不会有明显现象,应用足量的稀盐酸,不符合题意。
5. 九年级同学在化学实验操作训练中,进行了氢氧化钠和氢氧化钙溶液的鉴别实验。为进一步探究氢氧化钠的化学性质,做了以下实验。
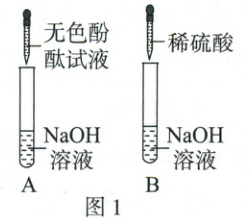
(1)A 试管中的现象是_。
为探究 B 试管中反应后溶液中溶质的成分,同学们进行了以下探究。
【猜想与假设】
(2)猜想一:Na₂SO₄;
猜想二:Na₂SO₄、H₂SO₄;
猜想三:_。
【设计并进行实验】
(3)完成并记录以下实验:

为探究氢氧化钠溶液与稀硫酸反应过程中pH 的变化,甲、乙两组同学按图 2 所示装置进行实验,测定出溶液 pH 变化如图3 所示。
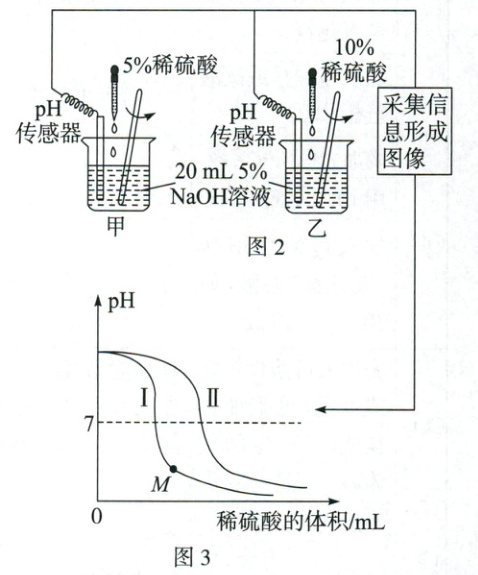
(4)甲组实验 pH变化对应的曲线是_(选填“Ⅰ”或“Ⅱ”)。若取 M 点对应溶液滴加紫色石蕊试液,现象是_。
(5)氢氧化钠溶液久置在空气中会变质,其原因是_(用化学方程式表示);向部分变质的氢氧化钠溶液中加入适量_溶液可除去杂质。

(1)A 试管中的现象是_。
为探究 B 试管中反应后溶液中溶质的成分,同学们进行了以下探究。
【猜想与假设】
(2)猜想一:Na₂SO₄;
猜想二:Na₂SO₄、H₂SO₄;
猜想三:_。
【设计并进行实验】
(3)完成并记录以下实验:

为探究氢氧化钠溶液与稀硫酸反应过程中pH 的变化,甲、乙两组同学按图 2 所示装置进行实验,测定出溶液 pH 变化如图3 所示。

(4)甲组实验 pH变化对应的曲线是_(选填“Ⅰ”或“Ⅱ”)。若取 M 点对应溶液滴加紫色石蕊试液,现象是_。
(5)氢氧化钠溶液久置在空气中会变质,其原因是_(用化学方程式表示);向部分变质的氢氧化钠溶液中加入适量_溶液可除去杂质。
答案:
5.
(1)溶液变红
(2)Na₂SO₄、NaOH
(3)产生白色沉淀
(4)Ⅱ 溶液变红
(5)CO₂+2NaOH=Na₂CO₃+H₂O 氢氧化钙(合理即可)
[解析]
(2)B试管中发生的反应为2NaOH+H₂SO₄=Na₂SO₄+2H₂O,如果恰好完全反应,则溶质为Na₂SO₄;如果H₂SO₄溶液过量,则溶质为Na₂SO₄、H₂SO₄;如果NaOH溶液过量,则溶质为Na₂SO₄、NaOH,故猜想三为Na₂SO₄、NaOH。
(3)由实验结论“猜想一不成立,猜想三成立”知一定存在NaOH,则加入硝酸镁溶液后发生反应:2NaOH+Mg(NO₃)₂=Mg(OH)₂↓+2NaNO₃,观察到有白色沉淀产生。
(4)不同溶质质量分数的稀硫酸与相同的氢氧化钠溶液反应,稀硫酸的溶质质量分数越大,恰好完全反应,即pH=7时,消耗稀硫酸的体积越小,故甲组实验pH变化对应的曲线是Ⅱ。M点pH<7,溶液显酸性,能使紫色石蕊溶液变红。
(1)溶液变红
(2)Na₂SO₄、NaOH
(3)产生白色沉淀
(4)Ⅱ 溶液变红
(5)CO₂+2NaOH=Na₂CO₃+H₂O 氢氧化钙(合理即可)
[解析]
(2)B试管中发生的反应为2NaOH+H₂SO₄=Na₂SO₄+2H₂O,如果恰好完全反应,则溶质为Na₂SO₄;如果H₂SO₄溶液过量,则溶质为Na₂SO₄、H₂SO₄;如果NaOH溶液过量,则溶质为Na₂SO₄、NaOH,故猜想三为Na₂SO₄、NaOH。
(3)由实验结论“猜想一不成立,猜想三成立”知一定存在NaOH,则加入硝酸镁溶液后发生反应:2NaOH+Mg(NO₃)₂=Mg(OH)₂↓+2NaNO₃,观察到有白色沉淀产生。
(4)不同溶质质量分数的稀硫酸与相同的氢氧化钠溶液反应,稀硫酸的溶质质量分数越大,恰好完全反应,即pH=7时,消耗稀硫酸的体积越小,故甲组实验pH变化对应的曲线是Ⅱ。M点pH<7,溶液显酸性,能使紫色石蕊溶液变红。
查看更多完整答案,请扫码查看


