第109页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
- 第107页
- 第108页
- 第109页
- 第110页
- 第111页
- 第112页
- 第113页
- 第114页
- 第115页
- 第116页
- 第117页
- 第118页
- 第119页
- 第120页
- 第121页
- 第122页
- 第123页
- 第124页
- 第125页
- 第126页
- 第127页
- 第128页
- 第129页
- 第130页
- 第131页
- 第132页
- 第133页
- 第134页
- 第135页
- 第136页
- 第137页
- 第138页
- 第139页
- 第140页
- 第141页
- 第142页
- 第143页
- 第144页
- 第145页
- 第146页
- 第147页
- 第148页
- 第149页
- 第150页
- 第151页
- 第152页
- 第153页
- 第154页
- 第155页
- 第156页
- 第157页
- 第158页
- 第159页
- 第160页
- 第161页
- 第162页
- 第163页
- 第164页
- 第165页
- 第166页
- 第167页
- 第168页
- 第169页
- 第170页
- 第171页
- 第172页
- 第173页
- 第174页
- 第175页
- 第176页
- 第177页
- 第178页
- 第179页
- 第180页
- 第181页
- 第182页
- 第183页
- 第184页
- 第185页
- 第186页
- 第187页
- 第188页
- 第189页
- 第190页
- 第191页
- 第192页
- 第193页
- 第194页
- 第195页
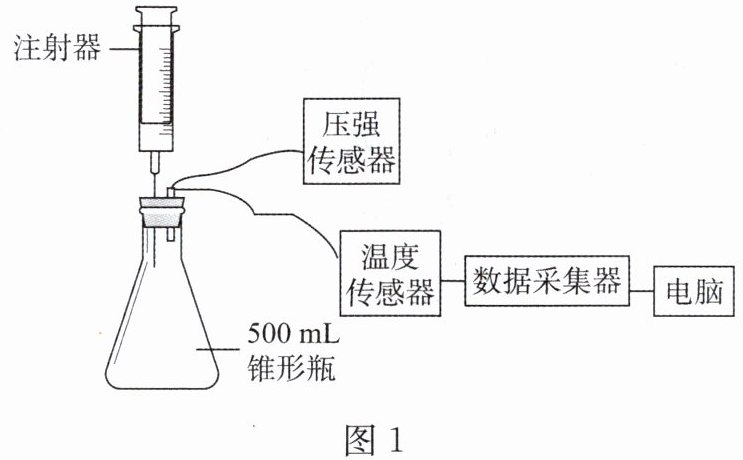
7. 某项目学习小组用传感器开展“影响铁锈蚀因素”的探究,设计如图1所示实验装置并完成实验。实验过程中,传感器采集数据绘制得到如图2所示的甲、乙两幅曲线图。
【资料1】在一定条件下,碳和氯化钠溶液可加快铁的锈蚀,但它们本身不参加反应。
【资料2】该实验步骤如下:
① 检查装置的气密性;
② 装药品,将5g铁粉和2g碳粉加入锥形瓶,并加入2mL饱和氯化钠溶液;
③ 立即塞紧橡皮塞,橡皮塞上已插有一支装有5mL稀盐酸的注射器及传感器;
④ 观察现象,采集数据。

用所学知识及以上资料信息完成下列问题。
(1)实验进行一段时间后,注射器中的盐酸会自动注入瓶内,原因是_________。
(2)图2甲、乙曲线图中$,0~t_1$段温度升高,瓶内压强减小;$t_2~t_3$段温度升高,瓶内压强增大。解释产生这两个不同现象的原因:_________。
【资料1】在一定条件下,碳和氯化钠溶液可加快铁的锈蚀,但它们本身不参加反应。
【资料2】该实验步骤如下:
① 检查装置的气密性;
② 装药品,将5g铁粉和2g碳粉加入锥形瓶,并加入2mL饱和氯化钠溶液;
③ 立即塞紧橡皮塞,橡皮塞上已插有一支装有5mL稀盐酸的注射器及传感器;
④ 观察现象,采集数据。


用所学知识及以上资料信息完成下列问题。
(1)实验进行一段时间后,注射器中的盐酸会自动注入瓶内,原因是_________。
(2)图2甲、乙曲线图中$,0~t_1$段温度升高,瓶内压强减小;$t_2~t_3$段温度升高,瓶内压强增大。解释产生这两个不同现象的原因:_________。
答案:
(1)铁生锈消耗瓶内氧气,瓶内压强减小,当瓶内气压减小到一定程度,大气压将注射器的活塞下压(或瓶内气压减小,盐酸被吸入瓶内,合理即可) (2)0~t₁段铁生锈消耗氧气,减小的压强大于温度升高增大的压强,瓶内压强减小;t₂~t₃段因瓶内气压减小,盐酸自动注入瓶内,与铁反应生成氢气并放出大量的热,生成的氢气和放出的热量都使压强增大
8. 金属铁和金属铜都是我们生活中非常熟悉的金属。
(1)炼铁可以选用磁铁矿,其主要成分是_________(填化学式)。
(2)炼铁的设备是_________;得到的主要产品是_________。
(3)写出炼铁时焦炭与二氧化碳反应的化学方程式:_________。
(4)晋葛洪《抱朴子内篇·黄白》中有“以曾青涂铁,铁赤色如铜”的记载。请写出表示该原理的化学方程式:_________。
(5)普通的铁制品在_________中容易生锈,除了制成不锈钢或保持表面的洁净干燥外,通常采用_________的原理来防止生锈。事实上,铜虽然不如铁活泼,在一定条件下也会生锈。
【查阅资料】铜锈的主要成分可以看成是$aCu(OH)_2·bCuCO_3;$
$Cu(OH)_2、$$CuCO_3$受热易分解,各生成对应的两种氧化物;
$Cu(OH)_2$的分解温度为$66℃~68℃,CuCO_3$的分解温度为200℃~220℃。
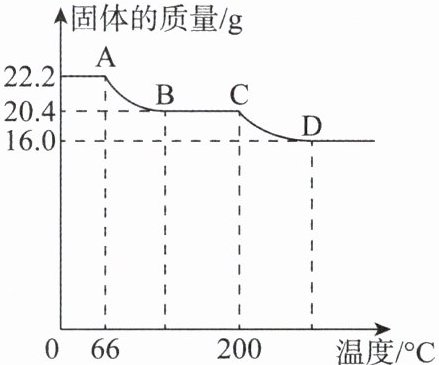
研究小组的同学用热分析仪对$aCu(OH)_2·bCuCO_3$固体进行热分解,获得相关数据,绘成固体质量变化与分解温度的关系如右图所示,请根据图示回答下列问题。
① 写出AB、CD段发生反应的化学方程式。
AB段:_________。
CD段:_________。
② BC段固体为_________。
③ 通过计算可得a:b= _________。
(1)炼铁可以选用磁铁矿,其主要成分是_________(填化学式)。
(2)炼铁的设备是_________;得到的主要产品是_________。
(3)写出炼铁时焦炭与二氧化碳反应的化学方程式:_________。
(4)晋葛洪《抱朴子内篇·黄白》中有“以曾青涂铁,铁赤色如铜”的记载。请写出表示该原理的化学方程式:_________。
(5)普通的铁制品在_________中容易生锈,除了制成不锈钢或保持表面的洁净干燥外,通常采用_________的原理来防止生锈。事实上,铜虽然不如铁活泼,在一定条件下也会生锈。
【查阅资料】铜锈的主要成分可以看成是$aCu(OH)_2·bCuCO_3;$
$Cu(OH)_2、$$CuCO_3$受热易分解,各生成对应的两种氧化物;
$Cu(OH)_2$的分解温度为$66℃~68℃,CuCO_3$的分解温度为200℃~220℃。
研究小组的同学用热分析仪对$aCu(OH)_2·bCuCO_3$固体进行热分解,获得相关数据,绘成固体质量变化与分解温度的关系如右图所示,请根据图示回答下列问题。
① 写出AB、CD段发生反应的化学方程式。
AB段:_________。
CD段:_________。
② BC段固体为_________。
③ 通过计算可得a:b= _________。

答案:
(1) Fe₃O₄
(2) 高炉;生铁
(3) C + CO₂ =高温= 2CO
(4) Fe + CuSO₄ = FeSO₄ + Cu
(5) 潮湿的空气中(或与氧气、水接触的环境中);隔绝氧气和水(或隔绝空气和水)
① AB段:Cu(OH)₂ =△= CuO + H₂O↑
CD段:CuCO₃ =△= CuO + CO₂↑
② CuO和CuCO₃(或氧化铜和碳酸铜)
③ 1:1
(1) Fe₃O₄
(2) 高炉;生铁
(3) C + CO₂ =高温= 2CO
(4) Fe + CuSO₄ = FeSO₄ + Cu
(5) 潮湿的空气中(或与氧气、水接触的环境中);隔绝氧气和水(或隔绝空气和水)
① AB段:Cu(OH)₂ =△= CuO + H₂O↑
CD段:CuCO₃ =△= CuO + CO₂↑
② CuO和CuCO₃(或氧化铜和碳酸铜)
③ 1:1
查看更多完整答案,请扫码查看


