第74页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
- 第107页
- 第108页
- 第109页
- 第110页
- 第111页
- 第112页
- 第113页
- 第114页
- 第115页
- 第116页
- 第117页
- 第118页
- 第119页
- 第120页
- 第121页
- 第122页
- 第123页
- 第124页
- 第125页
- 第126页
- 第127页
- 第128页
- 第129页
- 第130页
- 第131页
- 第132页
- 第133页
- 第134页
- 第135页
- 第136页
5. (2024·昆明西山区一模)“液态阳光”是指生产过程中碳排放极低或为零时制得的甲醇。我国科学家分别攻克了两大催化技术,使合成“液态阳光”(甲醇$CH_{3}OH$)的两个生产环节效率大幅提高。如图一为“液态阳光”的合成示意图,图二所示为图一中环节2的反应原理。下列说法不正确的是(


A.据图一分析:环节1中发生的是分解反应
B.据图一分析:环节2的反应涉及两种氧化物
C.据图二分析:参加反应的两物质的分子个数比为$3:1$
D.据图二分析:参加反应的甲和生成的丁物质的质量比为$1:9$
D
)

A.据图一分析:环节1中发生的是分解反应
B.据图一分析:环节2的反应涉及两种氧化物
C.据图二分析:参加反应的两物质的分子个数比为$3:1$
D.据图二分析:参加反应的甲和生成的丁物质的质量比为$1:9$
答案:
5.D
6. 新考向 跨学科融合 四冲程汽油机的工作冲程由吸气、压缩、做功、排气四个冲程组成,燃料为汽油、天然气等。气缸中微观粒子变化示意图如图:
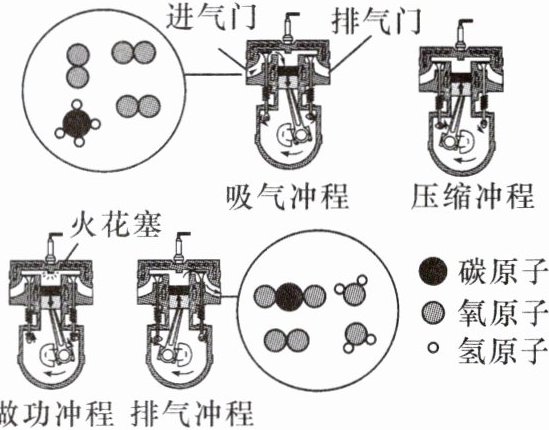
(1) 从微观角度解释压缩冲程中气缸内气体发生的变化:
(2) 做功冲程中化学能转变为
(3) 上述化学反应中,参加反应的和分子个数比为

(1) 从微观角度解释压缩冲程中气缸内气体发生的变化:
分子间的间隔变小
。(2) 做功冲程中化学能转变为
机械能
。(3) 上述化学反应中,参加反应的和分子个数比为
1:2
。
答案:
6.
(1)分子间的间隔变小
(2)机械能
(3)$1:2$
(1)分子间的间隔变小
(2)机械能
(3)$1:2$
7. (2024·昆明盘龙区期末)为测定某过氧化钠样品的纯度,用40g该样品与足量水发生如下反应(杂质不参与反应):$2Na_{2}O_{2} + 2H_{2}O = 4NaOH + O_{2}↑$,生成的气体质量和时间的关系如图所示。
(1) 生成氧气的质量为
(2) 求该样品中过氧化钠($Na_{2}O_{2}$)的质量分数。

(1) 生成氧气的质量为
6.4
g;(2) 求该样品中过氧化钠($Na_{2}O_{2}$)的质量分数。

答案:
7.
(1)6.4
(2)解:设该样品中过氧化钠的质量为x。
$2\mathrm{N}{\mathrm{a}}_{2}{\mathrm{O}}_{2}+2{\mathrm{H}}_{2}\mathrm{O}\xlongequal{}4\mathrm{N}\mathrm{a}\mathrm{O}\mathrm{H}+{\mathrm{O}}_{2}\uparrow$
156 32
x 6.4 g
$\frac{156}{32}=\frac{x}{6.4\mathrm{g}}$ $x=31.2\mathrm{g}$
则该样品中过氧化钠的质量分数为$\frac{31.2\mathrm{g}}{40\mathrm{g}}× 100\%=78\%$
答:该样品中过氧化钠的质量分数为78%。
(1)6.4
(2)解:设该样品中过氧化钠的质量为x。
$2\mathrm{N}{\mathrm{a}}_{2}{\mathrm{O}}_{2}+2{\mathrm{H}}_{2}\mathrm{O}\xlongequal{}4\mathrm{N}\mathrm{a}\mathrm{O}\mathrm{H}+{\mathrm{O}}_{2}\uparrow$
156 32
x 6.4 g
$\frac{156}{32}=\frac{x}{6.4\mathrm{g}}$ $x=31.2\mathrm{g}$
则该样品中过氧化钠的质量分数为$\frac{31.2\mathrm{g}}{40\mathrm{g}}× 100\%=78\%$
答:该样品中过氧化钠的质量分数为78%。
8. 化学观念 变化与转化 $N_{2}O$、$CO$在复合催化剂$M_{2}O$($M$代表一种金属)表面进行两步反应后转化为无毒气体,其转化关系如图所示。下列说法错误的是(

A.$N_{2}$是空气中含量最多的气体
B.“过程2”说明$CO$在一定条件下可以转化为$CO_{2}$
C.“过程1”中$N$元素化合价升高
D.转化的总反应为$N_{2}O + CO \xlongequal{M_{2}O} N_{2} + CO_{2}$
C
)
A.$N_{2}$是空气中含量最多的气体
B.“过程2”说明$CO$在一定条件下可以转化为$CO_{2}$
C.“过程1”中$N$元素化合价升高
D.转化的总反应为$N_{2}O + CO \xlongequal{M_{2}O} N_{2} + CO_{2}$
答案:
8.C
1. 根据质量守恒定律解释,细铁丝在氧气中燃烧后,生成物的质量比原来细铁丝的质量大:
2. 从微观的角度解释质量守恒的原因:
根据质量守恒定律,参加反应的铁和氧气的质量之和一定等于生成的四氧化三铁的质量,故生成物的质量比原来细铁丝的质量大
。2. 从微观的角度解释质量守恒的原因:
化学反应前后,原子的种类、质量、数目都没有改变
。
答案:
1. 根据质量守恒定律,参加反应的铁和氧气的质量之和一定等于生成的四氧化三铁的质量,故生成物的质量比原来细铁丝的质量大
2. 从微观的角度解释质量守恒的原因:化学反应前后,原子的种类、质量、数目都没有改变
2. 从微观的角度解释质量守恒的原因:化学反应前后,原子的种类、质量、数目都没有改变
查看更多完整答案,请扫码查看


