2026年金考卷中考试题汇编45套化学山东专版
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2026年金考卷中考试题汇编45套化学山东专版 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
第94页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
- 第107页
- 第108页
- 第109页
- 第110页
- 第111页
- 第112页
- 第113页
- 第114页
- 第115页
- 第116页
- 第117页
- 第118页
- 第119页
- 第120页
- 第121页
- 第122页
- 第123页
- 第124页
- 第125页
- 第126页
- 第127页
- 第128页
- 第129页
- 第130页
- 第131页
- 第132页
- 第133页
- 第134页
- 第135页
- 第136页
- 第137页
- 第138页
26.(11分)铁是日常生活中应用最广泛的金属。
(1)铁的认识:铁块可以拉成铁丝是利用铁的
(2)铁的冶炼:赤铁矿的主要成分为氧化铁,请写出用一氧化碳还原赤铁矿发生反应的化学方程式:
(3)铁的锈蚀:为探究铁制品锈蚀的条件,兴趣小组同学设计如下实验。

①一周后,观察 A、B、C 中的铁钉,只有 A 中的铁钉出现了明显锈蚀现象,由此得出铁生锈的条件是
②取出生锈的铁钉,将其放置在稀盐酸中,一段时间后发现溶液变黄,铁钉表面有少量气泡产生。产生气泡的原因是
(4)金属的回收:现有一份废铜料(含有金属铜及少量铁和银),化学兴趣小组欲回收其中的铜,设计并进行了如下实验。

已知:Cu + 2FeCl₃ ══ CuCl₂ + 2FeCl₂;Ag + FeCl₃ ══ AgCl + FeCl₂。
①溶液 A 中的溶质是
②滤渣 B 的成分是
③写出步骤4中反应的化学方程式:
(1)铁的认识:铁块可以拉成铁丝是利用铁的
延展性
。生铁和钢都属于合金
(选填“金属单质”或“合金”)。(2)铁的冶炼:赤铁矿的主要成分为氧化铁,请写出用一氧化碳还原赤铁矿发生反应的化学方程式:
$\mathrm{Fe_2O_3+3CO\xlongequal{高温}2Fe+3CO_2}$
。(3)铁的锈蚀:为探究铁制品锈蚀的条件,兴趣小组同学设计如下实验。

①一周后,观察 A、B、C 中的铁钉,只有 A 中的铁钉出现了明显锈蚀现象,由此得出铁生锈的条件是
与水和氧气同时接触
。②取出生锈的铁钉,将其放置在稀盐酸中,一段时间后发现溶液变黄,铁钉表面有少量气泡产生。产生气泡的原因是
$\mathrm{Fe+2HCl=FeCl_2+H_2\uparrow}$
(用化学方程式表示)。(4)金属的回收:现有一份废铜料(含有金属铜及少量铁和银),化学兴趣小组欲回收其中的铜,设计并进行了如下实验。

已知:Cu + 2FeCl₃ ══ CuCl₂ + 2FeCl₂;Ag + FeCl₃ ══ AgCl + FeCl₂。
①溶液 A 中的溶质是
$\mathrm{FeSO_4}$、$\mathrm{H_2SO_4}$
(填化学式)。②滤渣 B 的成分是
$\mathrm{AgCl}$
(填化学式)。③写出步骤4中反应的化学方程式:
$\mathrm{Fe+CuCl_2=FeCl_2+Cu}$
。
答案:
26
(1)延展性 合金
(2)$\mathrm{Fe_2O_3+3CO\xlongequal{高温}2Fe+3CO_2}$
(3)①与水和氧气同时接触
②$\mathrm{Fe+2HCl=FeCl_2+H_2\uparrow}$ ③$\mathrm{Fe+CuCl_2=FeCl_2+Cu}$
【解题思路】
(3)①对比A、B可知,铁钉锈蚀需要与氧气接触;对比A、C可知,铁钉锈蚀需要与水接触;综上所述,该实验能得出铁生锈的条件是与水和氧气同时接触。②将生锈的铁钉放置在稀盐酸中,根据题述实验现象知发生两个反应:$\mathrm{Fe_2O_3+6HCl=2FeCl_3+3H_2O}$、$\mathrm{Fe+2HCl=FeCl_2+H_2\uparrow}$,产生气泡的反应是后者。
(4)①向废铜料(含有金属铜及少量铁和银)粉末中加入过量稀硫酸,铜、银与稀硫酸不反应,铁与稀硫酸反应生成硫酸亚铁和氢气,则滤渣A的成分为铜、银,溶液A中的溶质为$\mathrm{FeSO_4}$、$\mathrm{H_2SO_4}$。②向滤渣A中加入适量$\mathrm{FeCl_3}$溶液,发生反应$\mathrm{Cu+2FeCl_3=CuCl_2+2FeCl_2}$、$\mathrm{Ag+FeCl_3=AgCl+FeCl_2}$,则滤渣B的成分为$\mathrm{AgCl}$。③由②的分析可知,向滤渣A中加入适量$\mathrm{FeCl_3}$溶液,反应后溶液中的溶质是氯化亚铁和氯化铜,此时加入适量试剂X,得到氯化亚铁和铜,则试剂X为铁,反应的化学方程式为$\mathrm{Fe+CuCl_2=FeCl_2+Cu}$。
(1)延展性 合金
(2)$\mathrm{Fe_2O_3+3CO\xlongequal{高温}2Fe+3CO_2}$
(3)①与水和氧气同时接触
②$\mathrm{Fe+2HCl=FeCl_2+H_2\uparrow}$ ③$\mathrm{Fe+CuCl_2=FeCl_2+Cu}$
【解题思路】
(3)①对比A、B可知,铁钉锈蚀需要与氧气接触;对比A、C可知,铁钉锈蚀需要与水接触;综上所述,该实验能得出铁生锈的条件是与水和氧气同时接触。②将生锈的铁钉放置在稀盐酸中,根据题述实验现象知发生两个反应:$\mathrm{Fe_2O_3+6HCl=2FeCl_3+3H_2O}$、$\mathrm{Fe+2HCl=FeCl_2+H_2\uparrow}$,产生气泡的反应是后者。
(4)①向废铜料(含有金属铜及少量铁和银)粉末中加入过量稀硫酸,铜、银与稀硫酸不反应,铁与稀硫酸反应生成硫酸亚铁和氢气,则滤渣A的成分为铜、银,溶液A中的溶质为$\mathrm{FeSO_4}$、$\mathrm{H_2SO_4}$。②向滤渣A中加入适量$\mathrm{FeCl_3}$溶液,发生反应$\mathrm{Cu+2FeCl_3=CuCl_2+2FeCl_2}$、$\mathrm{Ag+FeCl_3=AgCl+FeCl_2}$,则滤渣B的成分为$\mathrm{AgCl}$。③由②的分析可知,向滤渣A中加入适量$\mathrm{FeCl_3}$溶液,反应后溶液中的溶质是氯化亚铁和氯化铜,此时加入适量试剂X,得到氯化亚铁和铜,则试剂X为铁,反应的化学方程式为$\mathrm{Fe+CuCl_2=FeCl_2+Cu}$。
27.(6分)某复习课上兴趣小组同学设计如图所示实验探究酸碱盐的性质。请你回答下列问题。
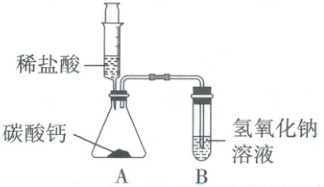
(1)组装好实验装置后,首先检查装置 A 的气密性良好。将稀盐酸全部推入锥形瓶中,固体全部溶解,得到无色透明溶液,还可以观察到 A 装置中的实验现象有
写出装置 B 中发生反应的化学方程式:
(2)待反应完全结束后,冷却至常温常压下,向上拉注射器活塞,发现装置 A 中产生白色沉淀。此时 A 装置中可能含有的阳离子是

(1)组装好实验装置后,首先检查装置 A 的气密性良好。将稀盐酸全部推入锥形瓶中,固体全部溶解,得到无色透明溶液,还可以观察到 A 装置中的实验现象有
有气泡产生
,写出装置 B 中发生反应的化学方程式:
$\mathrm{CO_2+2NaOH=Na_2CO_3+H_2O}$
。(2)待反应完全结束后,冷却至常温常压下,向上拉注射器活塞,发现装置 A 中产生白色沉淀。此时 A 装置中可能含有的阳离子是
$\mathrm{Ca^{2+}}$
(填离子符号),写出产生白色沉淀的化学方程式:$\mathrm{CaCl_2+Na_2CO_3=CaCO_3\downarrow+2NaCl}$
。
答案:
27
(1)有气泡产生 $\mathrm{CO_2+2NaOH=Na_2CO_3+H_2O}$
(2)$\mathrm{Ca^{2+}}$ $\mathrm{CaCl_2+Na_2CO_3=CaCO_3\downarrow+2NaCl}$
【解题思路】
(2)待反应完全结束后,冷却至常温常压下,向上拉注射器活塞,B中的溶液进入A中,与A中的物质反应生成白色沉淀,则说明A中的稀盐酸完全反应,B中生成的碳酸钠与A中氯化钙反应生成碳酸钙沉淀和氯化钠($\mathrm{CaCl_2+Na_2CO_3=CaCO_3\downarrow+2NaCl}$),则此时A装置中一定含有钠离子,可能含有钙离子($\mathrm{Ca^{2+}}$)。
(1)有气泡产生 $\mathrm{CO_2+2NaOH=Na_2CO_3+H_2O}$
(2)$\mathrm{Ca^{2+}}$ $\mathrm{CaCl_2+Na_2CO_3=CaCO_3\downarrow+2NaCl}$
【解题思路】
(2)待反应完全结束后,冷却至常温常压下,向上拉注射器活塞,B中的溶液进入A中,与A中的物质反应生成白色沉淀,则说明A中的稀盐酸完全反应,B中生成的碳酸钠与A中氯化钙反应生成碳酸钙沉淀和氯化钠($\mathrm{CaCl_2+Na_2CO_3=CaCO_3\downarrow+2NaCl}$),则此时A装置中一定含有钠离子,可能含有钙离子($\mathrm{Ca^{2+}}$)。
查看更多完整答案,请扫码查看


