2026年金考卷中考试题汇编45套化学山东专版
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2026年金考卷中考试题汇编45套化学山东专版 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
第7页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
- 第107页
- 第108页
- 第109页
- 第110页
- 第111页
- 第112页
- 第113页
- 第114页
- 第115页
- 第116页
- 第117页
- 第118页
- 第119页
- 第120页
- 第121页
- 第122页
- 第123页
- 第124页
- 第125页
- 第126页
- 第127页
- 第128页
- 第129页
- 第130页
- 第131页
- 第132页
- 第133页
- 第134页
- 第135页
- 第136页
- 第137页
- 第138页
21. (20分)我国的铜矿产资源比较丰富,需要根据矿石种类的不同选用适当的方法冶炼。
(1)我国古代即有湿法炼铜的技术,南北朝时期又将湿法炼铜中铜盐的范围扩大到所有的可溶性铜盐(如CuCl₂),铁与氯化铜溶液反应的化学方程式为
(2)蓝铜矿的主要成分Cu₃(CO₃)₂(OH)₂可溶于稀硫酸。先用稀硫酸浸取矿石,再电解浸取液使铜沉积。电解时能量的主要转化形式为
(3)黄铜矿的主要成分为CuFeS₂,其冶炼过程大致如下:
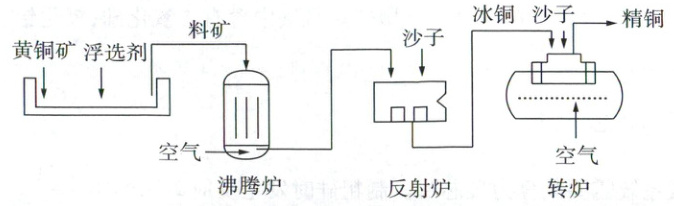
①为了增强浮选剂对矿石的富集效果,提高沸腾炉中化学反应的反应速率和原料利用率,需预先对矿石进行的操作为
②沸腾炉中,发生反应2CuFeS₂ + O₂ $\xlongequal{高温}$ 2FeS + Cu₂S + X,X的化学式为
③反射炉中,沙子与杂质形成熔渣浮于上层,Cu₂S和FeS熔融生成的“冰铜”沉于下层。Cu₂S中硫元素的化合价为-2,则铜元素的化合价为
④转炉中,沙子与杂质形成炉渣,Cu₂S在高温条件下发生的反应过程如下:
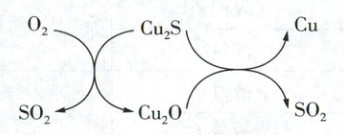
判断生成的气体能否直接排放并说明原因
(4)兴趣小组利用如图装置(夹持装置已略去)对我国古代“竖炉炼铜”进行模拟实验,实验原理为C + 2CuO $\xlongequal{高温}$ 2Cu + CO₂↑
①依据上述化学方程式计算C与CuO的质量比为
②为获得最佳实验效果,控制C与CuO的总质量一定,按不同质量比进行实验所得反应后物质状态如表。由实验知C和CuO质量比为1:10时实验效果最佳,判断依据是


(1)我国古代即有湿法炼铜的技术,南北朝时期又将湿法炼铜中铜盐的范围扩大到所有的可溶性铜盐(如CuCl₂),铁与氯化铜溶液反应的化学方程式为
Fe + CuCl₂ ══ FeCl₂ + Cu
。(2)蓝铜矿的主要成分Cu₃(CO₃)₂(OH)₂可溶于稀硫酸。先用稀硫酸浸取矿石,再电解浸取液使铜沉积。电解时能量的主要转化形式为
电能转化为化学能
。(3)黄铜矿的主要成分为CuFeS₂,其冶炼过程大致如下:

①为了增强浮选剂对矿石的富集效果,提高沸腾炉中化学反应的反应速率和原料利用率,需预先对矿石进行的操作为
将矿石粉碎为碎石块,增大接触面积
。②沸腾炉中,发生反应2CuFeS₂ + O₂ $\xlongequal{高温}$ 2FeS + Cu₂S + X,X的化学式为
SO₂
。③反射炉中,沙子与杂质形成熔渣浮于上层,Cu₂S和FeS熔融生成的“冰铜”沉于下层。Cu₂S中硫元素的化合价为-2,则铜元素的化合价为
+1
。④转炉中,沙子与杂质形成炉渣,Cu₂S在高温条件下发生的反应过程如下:

判断生成的气体能否直接排放并说明原因
不能,生成的 SO₂为污染性气体,会危害人体健康
;Cu₂O→Cu的化学方程式为2Cu₂O + Cu₂S\overset{高温}{=}6Cu + SO₂↑
。(4)兴趣小组利用如图装置(夹持装置已略去)对我国古代“竖炉炼铜”进行模拟实验,实验原理为C + 2CuO $\xlongequal{高温}$ 2Cu + CO₂↑
①依据上述化学方程式计算C与CuO的质量比为
3:40
(填最简整数比)。烘干CuO粉末和木炭后,将木炭在研钵中研磨,按此质量比进行实验,效果不佳。②为获得最佳实验效果,控制C与CuO的总质量一定,按不同质量比进行实验所得反应后物质状态如表。由实验知C和CuO质量比为1:10时实验效果最佳,判断依据是
比例 1:10时,既有金属光泽又有红色块状金属产生,说明铜产量较大,几乎无黑色物质,说明反应物 C 与 Cu₂O 残留少,即原料利用率高
,利用数据分析其原因可能是碳过少时无法将 Cu₂O 完全反应而有残留,碳过量时,碳与产物 CO₂会生成 CO,同时装置内残留的 O₂也会消耗碳从而生成 CO₂,导致 C 的额外损耗
。

答案:
21
(1)Fe + CuCl₂ ══ FeCl₂ + Cu
(2)电能转化为化学能
(3)①将矿石粉碎为碎石块,增大接触面积 ②SO₂ ③ + 1
④不能,生成的 SO₂为污染性气体,会危害人体健康
$2Cu₂O + Cu₂S\overset{高温}{=}6Cu + SO₂↑ (4)①3:40 ②$比例 1:10时,既有金属光泽又有红色块状金属产生,说明铜产量较大,几乎无黑色物质,说明反应物 C 与 Cu₂O 残留少,即原料利用率高 碳过少时无法将 Cu₂O 完全反应而有残留,碳过量时,碳与产物 CO₂会生成 CO,同时装置内残留的 O₂也会消耗碳从而生成 CO₂,导致 C 的额外损耗
【解题思路】
(3)①对矿石进行粉碎,以增大反应物间的接触面积,可有效提高化学反应速率和原料的利用率。
②根据反应前后原子的种类、数目不变。可知 X 的化学式为 SO₂。
③根据化合物中各元素正、负化合价的代数和为0的原则,设 Cu₂S 中 Cu 的化合价为 x,有 2x + (-2) = 0,解得 x = +1。
④由图可知,反应会生成 SO₂等污染性气体,若直接排放会造成空气污染,危害人体健康;Cu₂S→Cu 的反应:反应物为 Cu₂S 和 Cu₂O,生成物为 Cu 和 SO₂,所以化学方程式为$2Cu₂O + Cu₂S\overset{高温}{=}6Cu + SO₂↑。$
(4)①根据化学方程式,反应中 C 与 Cu₂O 的质量比为 12:160 = 3:40。
(1)Fe + CuCl₂ ══ FeCl₂ + Cu
(2)电能转化为化学能
(3)①将矿石粉碎为碎石块,增大接触面积 ②SO₂ ③ + 1
④不能,生成的 SO₂为污染性气体,会危害人体健康
$2Cu₂O + Cu₂S\overset{高温}{=}6Cu + SO₂↑ (4)①3:40 ②$比例 1:10时,既有金属光泽又有红色块状金属产生,说明铜产量较大,几乎无黑色物质,说明反应物 C 与 Cu₂O 残留少,即原料利用率高 碳过少时无法将 Cu₂O 完全反应而有残留,碳过量时,碳与产物 CO₂会生成 CO,同时装置内残留的 O₂也会消耗碳从而生成 CO₂,导致 C 的额外损耗
【解题思路】
(3)①对矿石进行粉碎,以增大反应物间的接触面积,可有效提高化学反应速率和原料的利用率。
②根据反应前后原子的种类、数目不变。可知 X 的化学式为 SO₂。
③根据化合物中各元素正、负化合价的代数和为0的原则,设 Cu₂S 中 Cu 的化合价为 x,有 2x + (-2) = 0,解得 x = +1。
④由图可知,反应会生成 SO₂等污染性气体,若直接排放会造成空气污染,危害人体健康;Cu₂S→Cu 的反应:反应物为 Cu₂S 和 Cu₂O,生成物为 Cu 和 SO₂,所以化学方程式为$2Cu₂O + Cu₂S\overset{高温}{=}6Cu + SO₂↑。$
(4)①根据化学方程式,反应中 C 与 Cu₂O 的质量比为 12:160 = 3:40。
查看更多完整答案,请扫码查看


