第27页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
3. 某化学兴趣小组以金属为主题进行项目式探究,然后将知识应用于生活和学习。
【活动一】探究金属与氧气的反应
(1)按如图1进行铁丝在氧气中燃烧的实验,反应的化学方程式为
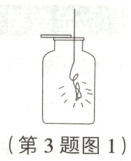
【活动二】探究金属与酸溶液的反应
如图2,取大小、表面积相同的金属片,分别加入等体积、等浓度的三份稀硫酸中。

(2)【实验分析】试管①中气泡快速产生,放出热量,反应的化学方程式为
【活动三】探究金属与盐溶液的反应
某同学为探究Cu和Al两种金属的活动性顺序,设计了如下实验:
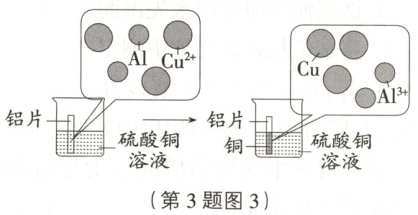
(3)铝和硫酸铜溶液反应的化学方程式为
【得出结论】(4)Cu和Al两种金属的活动性顺序为Al
【活动一】探究金属与氧气的反应
(1)按如图1进行铁丝在氧气中燃烧的实验,反应的化学方程式为
3Fe + 2O2 =点燃= Fe3O4
。该实验装置存在明显不足,改进的措施是瓶底要放少量的水(或铺一层细沙)
。对比铁丝在空气中不能燃烧、在氧气中剧烈燃烧的现象,说明化学反应的剧烈程度与氧气的浓度
有关。
【活动二】探究金属与酸溶液的反应
如图2,取大小、表面积相同的金属片,分别加入等体积、等浓度的三份稀硫酸中。

(2)【实验分析】试管①中气泡快速产生,放出热量,反应的化学方程式为
Zn + H2SO4 = ZnSO4 + H2↑
;试管②中气泡缓慢产生,溶液由无色变为浅绿
色,放出热量;试管③中无明显现象
。【活动三】探究金属与盐溶液的反应
某同学为探究Cu和Al两种金属的活动性顺序,设计了如下实验:

(3)铝和硫酸铜溶液反应的化学方程式为
2Al + 3CuSO4 = Al2(SO4)3 + 3Cu
。【得出结论】(4)Cu和Al两种金属的活动性顺序为Al
>
(选填“>”“<”或“=”)Cu。
答案:
3.(1)$\mathrm{3Fe + 2O_2 \xlongequal{点燃} Fe_3O_4}$ 瓶底要放少量的水(或铺一层细沙) 氧气的浓度
(2)$\mathrm{Zn + H_2SO_4 \xlongequal{ } ZnSO_4 + H_2 \uparrow}$ 浅绿 无明显现象
(3)$\mathrm{2Al + 3CuSO_4 \xlongequal{ } Al_2(SO_4)_3 + 3Cu}$
(4)>
(2)$\mathrm{Zn + H_2SO_4 \xlongequal{ } ZnSO_4 + H_2 \uparrow}$ 浅绿 无明显现象
(3)$\mathrm{2Al + 3CuSO_4 \xlongequal{ } Al_2(SO_4)_3 + 3Cu}$
(4)>
查看更多完整答案,请扫码查看


