第98页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
- 第107页
- 第108页
- 第109页
- 第110页
- 第111页
- 第112页
- 第113页
- 第114页
- 第115页
- 第116页
- 第117页
- 第118页
- 第119页
- 第120页
- 第121页
- 第122页
- 第123页
- 第124页
- 第125页
- 第126页
- 第127页
- 第128页
- 第129页
- 第130页
- 第131页
- 第132页
8. (2025·石家庄期中)如图所示是碳与氧化铜反应的实验装置,下列说法错误的是
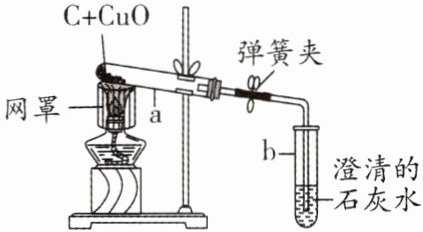
A.网罩的作用:集中火焰并提高温度
B.试管b的作用是检验有二氧化碳生成
C.试管a中黑色粉末变红,说明碳具有还原性
D.反应结束后立即把试管a中的物质倒出来观察现象
D

A.网罩的作用:集中火焰并提高温度
B.试管b的作用是检验有二氧化碳生成
C.试管a中黑色粉末变红,说明碳具有还原性
D.反应结束后立即把试管a中的物质倒出来观察现象
答案:
D 解析:反应结束后立即把试管 a 中的物质倒出来,其中的铜可能在较高温度下与空气中的氧气发生反应生成氧化铜,D 错误。
9. 新趋势 传统文化 我国明代宋应星所著的《天工开物》已记载有炼锡(锡的元素符号为Sn)的方法,用化学方程式可表示为$SnO_{2}+2C\xlongequal {高温}Sn+2CO\uparrow $。下列关于该反应的描述不正确的是
A.该炼锡方法会污染环境
B.CO在该反应中表现出了还原性
C.$SnO_{2}$在反应中提供氧,发生了还原反应
D.该化学反应后,固体质量减小
B
A.该炼锡方法会污染环境
B.CO在该反应中表现出了还原性
C.$SnO_{2}$在反应中提供氧,发生了还原反应
D.该化学反应后,固体质量减小
答案:
B 解析:该炼锡方法生成了一氧化碳,其有毒,能污染空气,A 正确;碳夺取了 ${SnO_{2}}$ 中的氧,碳在该反应中表现出了还原性,并且被氧化成 ${CO}$,即 ${CO}$ 在该反应中只是碳被氧化后的生成物,B 不正确;${SnO_{2}}$ 在反应中提供氧,被还原,发生了还原反应,C 正确;根据质量守恒定律,参与反应的各物质的质量总和等于反应后生成的各物质的质量总和,由于反应后有气体生成,所以该化学反应后固体质量减小,D 正确。
10. 新趋势 数字化实验 (2024·长春二模)将一定质量碳粉在密闭容器中引燃(如图1),一段时间后碳粉消失。实验过程测得容器内气体压强(同温下,容器内压强与气体分子数成正比)随时间的变化关系如图2。下列分析正确的是
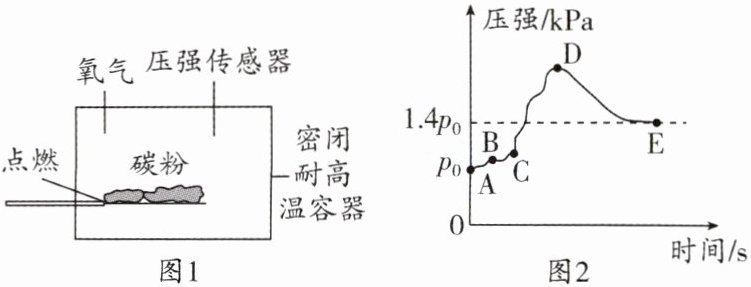
A.AB段碳粉开始燃烧
B.反应生成的$CO_{2}$导致CD段压强增大
C.E点气体的成分是$CO_{2}$和CO
D.燃烧放出的热量减少导致DE段压强下降
C

A.AB段碳粉开始燃烧
B.反应生成的$CO_{2}$导致CD段压强增大
C.E点气体的成分是$CO_{2}$和CO
D.燃烧放出的热量减少导致DE段压强下降
答案:
C 解析:由题意分析,碳粉燃烧生成二氧化碳,也能生成一氧化碳,根据化学方程式:${C + O_{2}\xlongequal{点燃}CO_{2}}$,${2C + O_{2}\xlongequal{点燃}2CO}$ 可知,一定温度和体积下气体的压强与分子数成正比,生成二氧化碳的过程中氧分子和二氧化碳分子的分子个数比为 $1:1$,生成一氧化碳的过程中氧分子和一氧化碳的分子个数比为 $1:2$。若完全转化为一氧化碳,气体分子个数变为原来的 2 倍,压强也变为原来的 2 倍,图示中显示压强为原来的 1.4 倍,所以没有完全生成一氧化碳,即反应后的气体应该为一氧化碳和二氧化碳的混合物。AB 段压强变化不明显,无法确定碳粉是否开始燃烧,A 错误;生成二氧化碳的过程中氧分子和二氧化碳分子的分子个数比为 $1:1$,所以生成二氧化碳的过程中气体体积不变,CD 段压强增大,是由于反应放热和生成一氧化碳造成的,B 错误;根据分析可知,C 正确;燃烧结束后,温度下降至室温,气体体积减小,压强减小,所以 DE 段压强下降,D 错误。
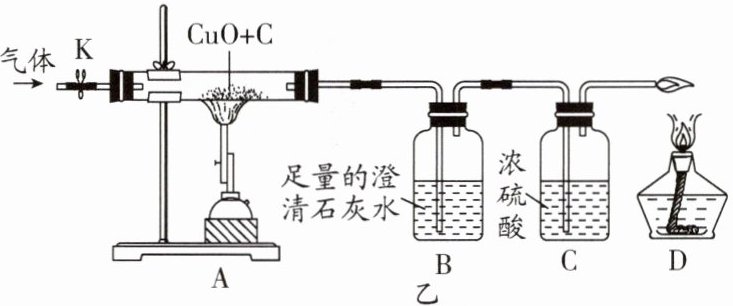
11. 碳还原氧化铜的实验装置如图甲、乙所示。
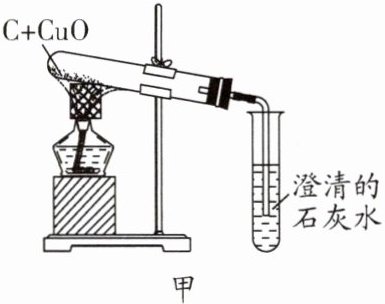
【提出问题】碳燃烧时可能生成$CO_{2}$也可能生成CO,那么碳与氧化铜反应生成的气体是否也有多种可能?
【作出猜想】猜想Ⅰ:CO;
猜想Ⅱ:$CO_{2}$;
猜想Ⅲ:
【设计方案】实验装置如图乙所示。打开K,缓缓通入干燥的氮气一段时间,关闭K,点燃酒精喷灯和酒精灯,充分反应后,熄灭酒精喷灯和酒精灯,打开K,再通入一段时间氮气。
方案一:从定性观察角度判断
(1)实验时装置A处的现象是
(2)若B中无明显现象,D处的气体能点燃,则猜想
方案二:从定量计算角度判断
取一定量碳粉和4g氧化铜的混合物进行实验,并测定表格中的四个数据:
| |反应前的质量|反应后的质量|
|A(玻璃管+固体)|$m_{1}$|$m_{2}$|
|B+C(广口瓶+混合液)|$m_{3}$|$m_{4}$|
(3)若猜想Ⅱ成立,则理论上$(m_{4}-m_{3})$
(4)若猜想Ⅲ成立且CuO全部转化成Cu,则参加反应的碳粉的质量m的取值范围是
【交流反思】实验开始前缓缓通入氮气的目的是


【提出问题】碳燃烧时可能生成$CO_{2}$也可能生成CO,那么碳与氧化铜反应生成的气体是否也有多种可能?
【作出猜想】猜想Ⅰ:CO;
猜想Ⅱ:$CO_{2}$;
猜想Ⅲ:
${CO}$ 和 ${CO_{2}}$
。【设计方案】实验装置如图乙所示。打开K,缓缓通入干燥的氮气一段时间,关闭K,点燃酒精喷灯和酒精灯,充分反应后,熄灭酒精喷灯和酒精灯,打开K,再通入一段时间氮气。
方案一:从定性观察角度判断
(1)实验时装置A处的现象是
黑色粉末变为(光亮的)红色
。(2)若B中无明显现象,D处的气体能点燃,则猜想
Ⅰ
(填序号)成立。方案二:从定量计算角度判断
取一定量碳粉和4g氧化铜的混合物进行实验,并测定表格中的四个数据:
| |反应前的质量|反应后的质量|
|A(玻璃管+固体)|$m_{1}$|$m_{2}$|
|B+C(广口瓶+混合液)|$m_{3}$|$m_{4}$|
(3)若猜想Ⅱ成立,则理论上$(m_{4}-m_{3})$
=
(填“>”“<”或“=”)$(m_{1}-m_{2})$。(4)若猜想Ⅲ成立且CuO全部转化成Cu,则参加反应的碳粉的质量m的取值范围是
$0.3\ \text{g} < m < 0.6\ \text{g}$
。【交流反思】实验开始前缓缓通入氮气的目的是
排尽装置内的空气,防止加热时发生爆炸,防止空气中的成分干扰实验
。
答案:
【作出猜想】${CO}$ 和 ${CO_{2}}$ 【设计方案】
(1) 黑色粉末变为(光亮的)红色
(2) Ⅰ
(3) =
(4) $0.3\ \text{g} < m < 0.6\ \text{g}$ 【交流反思】排尽装置内的空气,防止加热时发生爆炸,防止空气中的成分干扰实验 解析:【作出猜想】碳与氧化铜在高温条件下反应生成二氧化碳,如果碳过量,碳会与二氧化碳在高温条件下反应生成一氧化碳,故碳与氧化铜反应生成的气体可能是一氧化碳,还可能是二氧化碳,也可能是一氧化碳和二氧化碳的混合物,故猜想Ⅲ:${CO}$ 和 ${CO_{2}}$。【设计方案】方案一:
(1) 碳与氧化铜在高温条件下反应生成铜和二氧化碳,碳和氧化铜是黑色的,铜是红色的,故实验时装置 A 处的现象是黑色粉末变为(光亮的)红色。
(2) 二氧化碳能使澄清石灰水变浑浊,若 B 中无明显现象,说明无二氧化碳生成,一氧化碳具有可燃性,D 处的气体能点燃,说明生成了一氧化碳,故猜想Ⅰ成立。方案二:
(3) 若猜想Ⅱ成立,说明反应生成的气体是二氧化碳,相关化学方程式为 ${C + 2CuO\xlongequal{高温}2Cu + CO_{2}\uparrow}$,玻璃管中,反应后减少的质量就是反应生成的二氧化碳的质量,二氧化碳能被澄清石灰水吸收,$(m_{4}-m_{3})$ 即吸收的二氧化碳的质量,即碳与氧化铜在高温条件下反应生成二氧化碳的质量,故理论上 $(m_{4}-m_{3})=(m_{1}-m_{2})$。
(4) 假设 $4\ \text{g}$ 氧化铜与碳粉反应生成的气体全部是二氧化碳,则设这时消耗碳粉的质量为 $x$。${2CuO + C\xlongequal{高温}2Cu + CO_{2}\uparrow}$ $160\ \ \ 12$ $4\ \text{g}\ \ \ x$ $\dfrac{160}{12}=\dfrac{4\ \text{g}}{x}$,解得 $x = 0.3\ \text{g}$ 假设 $4\ \text{g}$ 氧化铜与碳粉反应生成的气体全部是一氧化碳,则设这时消耗碳粉的质量为 $y$。${CuO + C\xlongequal{高温}Cu + CO\uparrow}$ $80\ \ \ 12$ $4\ \text{g}\ \ \ y$ $\dfrac{80}{12}=\dfrac{4\ \text{g}}{y}$,解得 $y = 0.6\ \text{g}$ 若猜想Ⅲ成立,说明生成的气体是一氧化碳和二氧化碳的混合物,故参加反应的碳粉的质量 $m$ 的取值范围是 $0.3\ \text{g} < m < 0.6\ \text{g}$。【交流反思】该反应可能生成一氧化碳,一氧化碳具有可燃性,混有一定量的空气,遇高温容易发生爆炸,故实验开始前缓缓通入氮气的目的是排尽装置内的空气,防止加热时发生爆炸,防止空气中的成分干扰实验。
(1) 黑色粉末变为(光亮的)红色
(2) Ⅰ
(3) =
(4) $0.3\ \text{g} < m < 0.6\ \text{g}$ 【交流反思】排尽装置内的空气,防止加热时发生爆炸,防止空气中的成分干扰实验 解析:【作出猜想】碳与氧化铜在高温条件下反应生成二氧化碳,如果碳过量,碳会与二氧化碳在高温条件下反应生成一氧化碳,故碳与氧化铜反应生成的气体可能是一氧化碳,还可能是二氧化碳,也可能是一氧化碳和二氧化碳的混合物,故猜想Ⅲ:${CO}$ 和 ${CO_{2}}$。【设计方案】方案一:
(1) 碳与氧化铜在高温条件下反应生成铜和二氧化碳,碳和氧化铜是黑色的,铜是红色的,故实验时装置 A 处的现象是黑色粉末变为(光亮的)红色。
(2) 二氧化碳能使澄清石灰水变浑浊,若 B 中无明显现象,说明无二氧化碳生成,一氧化碳具有可燃性,D 处的气体能点燃,说明生成了一氧化碳,故猜想Ⅰ成立。方案二:
(3) 若猜想Ⅱ成立,说明反应生成的气体是二氧化碳,相关化学方程式为 ${C + 2CuO\xlongequal{高温}2Cu + CO_{2}\uparrow}$,玻璃管中,反应后减少的质量就是反应生成的二氧化碳的质量,二氧化碳能被澄清石灰水吸收,$(m_{4}-m_{3})$ 即吸收的二氧化碳的质量,即碳与氧化铜在高温条件下反应生成二氧化碳的质量,故理论上 $(m_{4}-m_{3})=(m_{1}-m_{2})$。
(4) 假设 $4\ \text{g}$ 氧化铜与碳粉反应生成的气体全部是二氧化碳,则设这时消耗碳粉的质量为 $x$。${2CuO + C\xlongequal{高温}2Cu + CO_{2}\uparrow}$ $160\ \ \ 12$ $4\ \text{g}\ \ \ x$ $\dfrac{160}{12}=\dfrac{4\ \text{g}}{x}$,解得 $x = 0.3\ \text{g}$ 假设 $4\ \text{g}$ 氧化铜与碳粉反应生成的气体全部是一氧化碳,则设这时消耗碳粉的质量为 $y$。${CuO + C\xlongequal{高温}Cu + CO\uparrow}$ $80\ \ \ 12$ $4\ \text{g}\ \ \ y$ $\dfrac{80}{12}=\dfrac{4\ \text{g}}{y}$,解得 $y = 0.6\ \text{g}$ 若猜想Ⅲ成立,说明生成的气体是一氧化碳和二氧化碳的混合物,故参加反应的碳粉的质量 $m$ 的取值范围是 $0.3\ \text{g} < m < 0.6\ \text{g}$。【交流反思】该反应可能生成一氧化碳,一氧化碳具有可燃性,混有一定量的空气,遇高温容易发生爆炸,故实验开始前缓缓通入氮气的目的是排尽装置内的空气,防止加热时发生爆炸,防止空气中的成分干扰实验。
查看更多完整答案,请扫码查看


