第59页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
- 第107页
- 第108页
- 第109页
- 第110页
- 第111页
- 第112页
- 第113页
- 第114页
- 第115页
- 第116页
- 第117页
- 第118页
- 第119页
- 第120页
- 第121页
- 第122页
- 第123页
- 第124页
- 第125页
- 第126页
- 第127页
- 第128页
- 第129页
- 第130页
- 第131页
- 第132页
12. (2025·钦州期中)元素周期表是学习和研究化学的重要工具。如图是元素周期表的一部分,X、Y、Z、M分别代表四种不同的元素。下列说法正确的是 (
A.X、Z的最外层电子数相同
B.X和Z处于同一周期
C.原子序数:Z<Y<M<X
D.原子核外电子数:X= M
A
)A.X、Z的最外层电子数相同
B.X和Z处于同一周期
C.原子序数:Z<Y<M<X
D.原子核外电子数:X= M
答案:
A 解析:X、Z位于同一族,则X、Z的最外层电子数相同,A正确;由图示可知,He是第一周期的元素,则X位于第二周期,Z位于第三周期,因此X和Z位于不同周期,B错误;图中X、M位于第二周期,且M位于X右侧,Y、Z位于第三周期,且Z位于Y右侧,可知X、M、Y、Z的原子序数大小关系为$Z>Y>M>X$,C错误;X、M处于同一周期,且M位于X右侧,所以原子序数:$X<M$,在原子中,原子序数=核外电子数,则原子核外电子数:$X<M$,D错误。
13. (11分)在宏观、微观和符号之间建立联系是化学学科的特点。下图是某物质发生反应的微观示意图。

(1)丙图中所示物质都是由
(2)结合上图分析,化学变化中最小的粒子是
(3)画出氧原子的结构示意图:
(4)该反应的基本类型为

(1)丙图中所示物质都是由
分子
(填“分子”“原子”或“离子”)构成的。(2)结合上图分析,化学变化中最小的粒子是
原子
。(3)画出氧原子的结构示意图:
$\enclose{circle}{+8}\begin{array}{l}2\\ \end{array}\begin{array}{l}6\\ \end{array}$
。(4)该反应的基本类型为
分解反应
。
答案:
(1)分子
(2)原子
(3)$\enclose{circle}{+8}\begin{array}{l}2\\ \end{array}\begin{array}{l}6\\ \end{array}$
(4)分解反应
解析:
(1)从微观角度看,丙图中所示物质是水和氧气,都是由分子构成的。
(2)结合题图分析,化学变化中分子可以分解为原子,原子不能再分,只能重新组合,化学变化中最小的粒子是原子。
(3)氧原子的质子数为8,电子数也为8,第一层为2个电子,第二层为6个电子,故氧原子的结构示意图为$\enclose{circle}{+8}\begin{array}{l}2\\ \end{array}\begin{array}{l}6\\ \end{array}$ 。
(4)该反应为一种物质生成两种物质的反应,属于分解反应
(1)分子
(2)原子
(3)$\enclose{circle}{+8}\begin{array}{l}2\\ \end{array}\begin{array}{l}6\\ \end{array}$
(4)分解反应
解析:
(1)从微观角度看,丙图中所示物质是水和氧气,都是由分子构成的。
(2)结合题图分析,化学变化中分子可以分解为原子,原子不能再分,只能重新组合,化学变化中最小的粒子是原子。
(3)氧原子的质子数为8,电子数也为8,第一层为2个电子,第二层为6个电子,故氧原子的结构示意图为$\enclose{circle}{+8}\begin{array}{l}2\\ \end{array}\begin{array}{l}6\\ \end{array}$ 。
(4)该反应为一种物质生成两种物质的反应,属于分解反应
14. (10分)(2025·滨州月考)对原子结构模型的形成,汤姆孙、卢瑟福和玻尔等科学家做出了突出贡献。请根据所学完成下列有关问题。
(1)汤姆孙发现了原子中存在一种带负电荷的粒子,证明了原子是可以再分的。汤姆孙发现的粒子是______
(2)1911年,卢瑟福等人进行了α粒子(α粒子是带两个单位正电荷的氦原子核)散射实验,为建立现代原子理论打下了基础。如图a、b、c、d四条线中,不可能是α粒子在该实验中的运动轨迹的是______
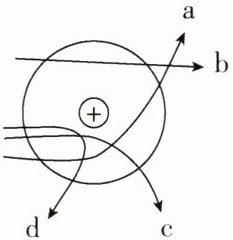
(3)从原子结构模型建立的过程中,我们发现______(填字母)
A. 科学模型的建立是一个不断完善、不断修正的过程
B. 模型在科学研究中起着很重要的作用
C. 卢瑟福原子模型的建立,使人们对原子结构的认识达到了完美的境界
D. 人类借助模型建立,对原子的认识逐渐接近本质
(1)汤姆孙发现了原子中存在一种带负电荷的粒子,证明了原子是可以再分的。汤姆孙发现的粒子是______
电子
。(2)1911年,卢瑟福等人进行了α粒子(α粒子是带两个单位正电荷的氦原子核)散射实验,为建立现代原子理论打下了基础。如图a、b、c、d四条线中,不可能是α粒子在该实验中的运动轨迹的是______
a
。
(3)从原子结构模型建立的过程中,我们发现______(填字母)
ABD
。A. 科学模型的建立是一个不断完善、不断修正的过程
B. 模型在科学研究中起着很重要的作用
C. 卢瑟福原子模型的建立,使人们对原子结构的认识达到了完美的境界
D. 人类借助模型建立,对原子的认识逐渐接近本质
答案:
(1)电子
(2)a
(3)ABD
(1)电子
(2)a
(3)ABD
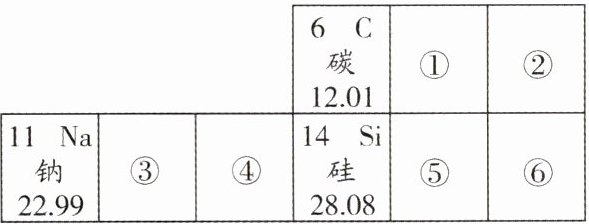
15. (15分)如图是几种元素的原子结构示意图及元素周期表的一部分。根据图中信息回答:
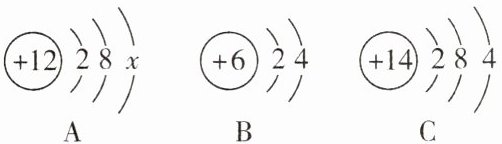
(1)A原子中,x=
(2)钠原子的相对原子质量为
(3)原子序数为12、8的两种元素组成物质的化学式为
(4)不同种元素最本质的区别是


(1)A原子中,x=
2
,所对应元素在元素周期表中的位置是③
(填序号)。(2)钠原子的相对原子质量为
22.99
,核外电子数是11
,它属于金属
(填“金属”或“非金属”)元素,在化学反应中容易失去
(填“得到”或“失去”)电子。(3)原子序数为12、8的两种元素组成物质的化学式为
MgO
。(4)不同种元素最本质的区别是
质子数
不同。
答案:
(1)2 ③
(2)22.99 11 金属 失去
(3)MgO
(4)质子数
解析:
(3)原子序数为12、8的两种元素分别是镁和氧,二者组成的化合物是氧化镁,其化学式是MgO。
(4)元素的概念是质子数(即核电荷数)相同的一类原子的总称,故不同种元素最本质的区别是核内质子数不同
(1)2 ③
(2)22.99 11 金属 失去
(3)MgO
(4)质子数
解析:
(3)原子序数为12、8的两种元素分别是镁和氧,二者组成的化合物是氧化镁,其化学式是MgO。
(4)元素的概念是质子数(即核电荷数)相同的一类原子的总称,故不同种元素最本质的区别是核内质子数不同
16. (13分)元素周期表是学习化学的重要工具,如图为元素周期表中部分元素的相关信息,利用如图回答相关问题。

(1)原子序数为4的元素符号为
(2)锂离子核外电子排布与
(3)一个磷原子含有
(4)第8号元素的原子在化学反应中易
(5)我国科学家张青莲教授主持测定的铟等多种元素的相对原子质量数据被确认为国际标准。关于相对原子质量,下列叙述错误的是
A. 相对原子质量与原子质量没有什么差别
B. 由于原子的质量太小,使用不方便,所以采用相对原子质量
C. 两种原子的质量之比等于它们的相对原子质量之比
D. 采用相对原子质量后,就增大了原子的质量

(1)原子序数为4的元素符号为
Be
。(2)锂离子核外电子排布与
He
(填元素符号)原子核外电子排布相同。(3)一个磷原子含有
15
个质子,一个$NH_4⁺$含有10
个电子。(4)第8号元素的原子在化学反应中易
得到
(填“得到”或“失去”)电子。(5)我国科学家张青莲教授主持测定的铟等多种元素的相对原子质量数据被确认为国际标准。关于相对原子质量,下列叙述错误的是
AD
(填字母)。A. 相对原子质量与原子质量没有什么差别
B. 由于原子的质量太小,使用不方便,所以采用相对原子质量
C. 两种原子的质量之比等于它们的相对原子质量之比
D. 采用相对原子质量后,就增大了原子的质量
答案:
(1)Be
(2)He
(3)15 10
(4)得到
(5)AD
解析:
(3)磷元素的原子序数为15,即磷原子中含有15个质子;1个氮原子含有7个电子,1个氢原子含有1个电子,所以一个$NH_{4}^{+}$含有$7+1×4−1=10$个电子。
(4)第8号元素的原子是氧原子,其最外层电子数为6,在化学反应中易得到电子。
(5)A.相对原子质量是根据统一的标准,用原子的实际质量与标准相比较得到的数值,而原子质量是原子的实际质量,二者之间有差别,说法错误;
B.由于原子的质量太小,使用不方便,所以采用相对原子质量,说法正确;C.相对原子质量是根据统一的标准,用原子的实际质量与标准相比较得到的数值,因此两种原子的质量之比等于它们的相对原子质量之比,说法正确;
D.采用相对原子质量后,原子的质量不会发生变化,说法错误;故选AD
(1)Be
(2)He
(3)15 10
(4)得到
(5)AD
解析:
(3)磷元素的原子序数为15,即磷原子中含有15个质子;1个氮原子含有7个电子,1个氢原子含有1个电子,所以一个$NH_{4}^{+}$含有$7+1×4−1=10$个电子。
(4)第8号元素的原子是氧原子,其最外层电子数为6,在化学反应中易得到电子。
(5)A.相对原子质量是根据统一的标准,用原子的实际质量与标准相比较得到的数值,而原子质量是原子的实际质量,二者之间有差别,说法错误;
B.由于原子的质量太小,使用不方便,所以采用相对原子质量,说法正确;C.相对原子质量是根据统一的标准,用原子的实际质量与标准相比较得到的数值,因此两种原子的质量之比等于它们的相对原子质量之比,说法正确;
D.采用相对原子质量后,原子的质量不会发生变化,说法错误;故选AD
查看更多完整答案,请扫码查看


