2025年中考备考课时练九年级化学全一册人教版
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2025年中考备考课时练九年级化学全一册人教版 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
第68页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
- 第107页
- 第108页
- 第109页
- 第110页
- 第111页
- 第112页
- 第113页
- 第114页
- 第115页
- 第116页
- 第117页
- 第118页
- 第119页
- 第120页
- 第121页
- 第122页
- 第123页
- 第124页
- 第125页
- 第126页
- 第127页
- 第128页
- 第129页
- 第130页
- 第131页
- 第132页
- 第133页
- 第134页
- 第135页
- 第136页
- 第137页
- 第138页
- 第139页
- 第140页
- 第141页
- 第142页
- 第143页
- 第144页
- 第145页
- 第146页
- 第147页
- 第148页
- 第149页
- 第150页
- 第151页
- 第152页
- 第153页
- 第154页
- 第155页
- 第156页
- 第157页
- 第158页
- 第159页
- 第160页
- 第161页
- 第162页
- 第163页
- 第164页
- 第165页
- 第166页
- 第167页
- 第168页
- 第169页
- 第170页
- 第171页
- 第172页
- 第173页
- 第174页
- 第175页
- 第176页
- 第177页
- 第178页
- 第179页
- 第180页
1.下列属于化学变化的是( )
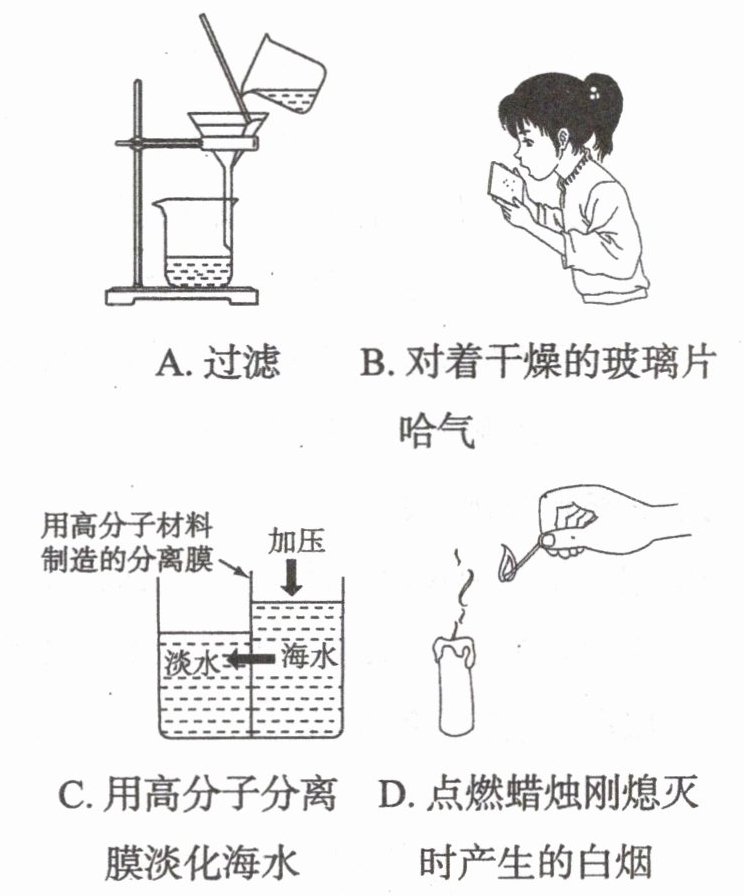

答案:
D
2.如图所示的化学实验基本操作中,正确的是( )
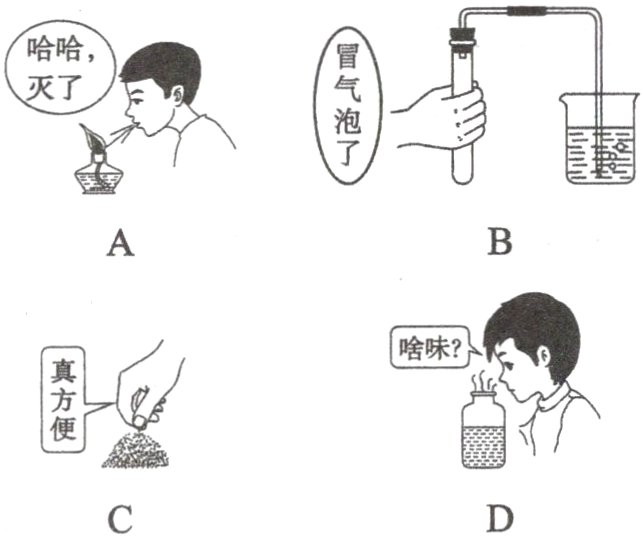

答案:
B
3.空气是一种宝贵的自然资源。下列有关说法中不正确的是( )
A.法国化学家拉瓦锡研究了空气的成分,并得出氧气约占空气总体积$\frac{4}{5}$的结论
B.空气是由氮气、氧气、稀有气体、二氧化碳等物质组成的混合物
C.氮气是制造硝酸和氮肥的重要原料
D.稀有气体都没有颜色、没有气味,在通电时能发出不同颜色的光
A.法国化学家拉瓦锡研究了空气的成分,并得出氧气约占空气总体积$\frac{4}{5}$的结论
B.空气是由氮气、氧气、稀有气体、二氧化碳等物质组成的混合物
C.氮气是制造硝酸和氮肥的重要原料
D.稀有气体都没有颜色、没有气味,在通电时能发出不同颜色的光
答案:
A
4.下列说法不正确的是( )
A.用红磷测定空气中氧气含量时,红磷一定要过量
B.用排水法收集氧气时,导管口刚有气泡冒出就收集气体
C.硫粉在氧气中燃烧时,集气瓶中放少量水可吸收二氧化硫
D.实验室用过氧化氢制氧气的反应中,二氧化锰起催化作用
A.用红磷测定空气中氧气含量时,红磷一定要过量
B.用排水法收集氧气时,导管口刚有气泡冒出就收集气体
C.硫粉在氧气中燃烧时,集气瓶中放少量水可吸收二氧化硫
D.实验室用过氧化氢制氧气的反应中,二氧化锰起催化作用
答案:
B
5.从微观角度解释下列现象,正确的是( )
A.“破镜不能重圆”说明分子间有斥力
B.温度越高,分子运动得越剧烈
C.汽油要密闭保存,主要是防止其泄漏引起火灾
D.冰吸热变成水,水吸热变成水蒸气,都说明分子可以再分
A.“破镜不能重圆”说明分子间有斥力
B.温度越高,分子运动得越剧烈
C.汽油要密闭保存,主要是防止其泄漏引起火灾
D.冰吸热变成水,水吸热变成水蒸气,都说明分子可以再分
答案:
B
6.水是生命之源。下列有关水的说法错误的是( )
A.明矾能吸附水中的悬浮颗粒而沉降
B.自然界中的水都是纯净物
C.食盐水中混有泥沙,利用过滤的方法可以除去泥沙
D.电解水生成氢气和氧气,说明水是由氢元素和氧元素组成的
A.明矾能吸附水中的悬浮颗粒而沉降
B.自然界中的水都是纯净物
C.食盐水中混有泥沙,利用过滤的方法可以除去泥沙
D.电解水生成氢气和氧气,说明水是由氢元素和氧元素组成的
答案:
B
7.(Sc)是“工业的维生素”,如图为钪在元素周期表中的相关信息及其原子结构示意图,下列说法正确的是( )

A.原子核外有四个电子层
B.钪的相对原子质量是21
C.原子结构示意图中x = 10
D.钪属于非金属元素

A.原子核外有四个电子层
B.钪的相对原子质量是21
C.原子结构示意图中x = 10
D.钪属于非金属元素
答案:
A
8.铈(Ce)是一种常见的稀土元素,已知铈原子的原子核内有58个质子和82个中子,该原子的核外电子数为( )
A.24
B.58
C.82
D.140
A.24
B.58
C.82
D.140
答案:
B
9.如图中“○”和“●”分别表示不同的原子,下列判断不正确的是( )

A.①可能是氧化物
B.②可能是金属
C.③一定是混合物
D.④包含组成元素相同的不同物质

A.①可能是氧化物
B.②可能是金属
C.③一定是混合物
D.④包含组成元素相同的不同物质
答案:
B
10.某种毒品的主要成分是MDMA(化学式为C₁₁H₁₅NO₂),吸食后对身体有严重的危害,下列说法错误的是( )
A.MDMA由4种元素组成
B.一个MDMA分子中含有29个原子
C.MDMA的相对分子质量为193g
D.MDMA中氢、氮元素的质量比为15:14
A.MDMA由4种元素组成
B.一个MDMA分子中含有29个原子
C.MDMA的相对分子质量为193g
D.MDMA中氢、氮元素的质量比为15:14
答案:
C
11.(6分)I.用化学用语填空:
(1)2个镁离子____________;
(2)氖气__________________;
(3)氢氧化钙______________;
(4)+6价硫元素的氧化物____________。
II.写出下列物质的名称:
(5)NaNO₂____________________;
(6)Fe₂O₃______________________。
(1)2个镁离子____________;
(2)氖气__________________;
(3)氢氧化钙______________;
(4)+6价硫元素的氧化物____________。
II.写出下列物质的名称:
(5)NaNO₂____________________;
(6)Fe₂O₃______________________。
答案:
(1)$2Mg^{2+}$ (2)$Ne$ (3)$Ca(OH)_{2}$ (4)$SO_{3}$ (5)硝酸钠 (6)三氧化二铁(或氧化铁)
12.(6分)在宏观、微观和符号之间建立联系是化学学科的特点。结合下图回答问题:
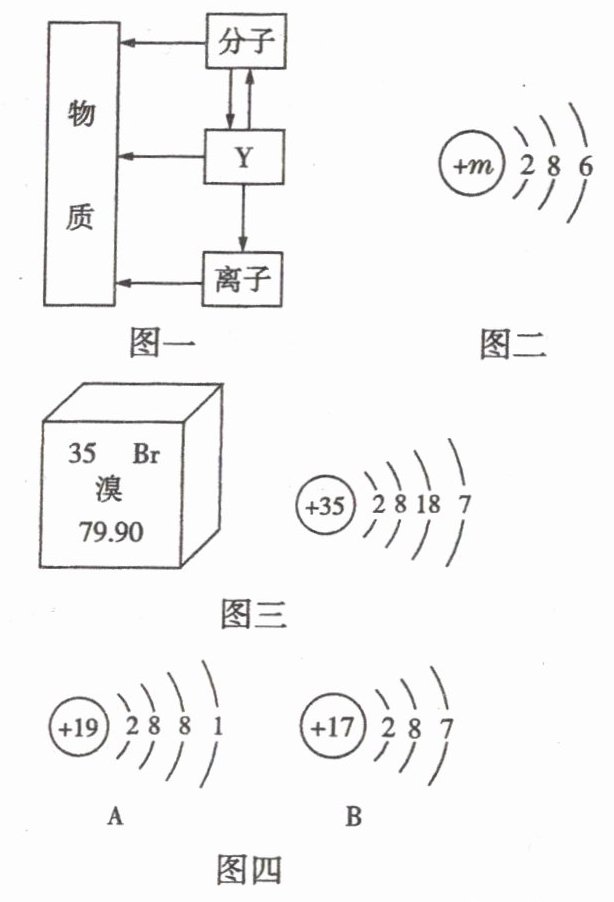
(1)图一中Y表示的是______________。
(2)图二为某原子结构示意图,其中m的值为__________,该粒子在化学反应中易____________(填“得到”或“失去”)电子。
(3)图三中溴元素属于__________(填“金属”或“非金属”)元素。
(4)溴元素的化学性质与图四中________(填字母)元素的化学性质相似。
(5)图四中A表示钾元素处于元素周期表的第________周期。

(1)图一中Y表示的是______________。
(2)图二为某原子结构示意图,其中m的值为__________,该粒子在化学反应中易____________(填“得到”或“失去”)电子。
(3)图三中溴元素属于__________(填“金属”或“非金属”)元素。
(4)溴元素的化学性质与图四中________(填字母)元素的化学性质相似。
(5)图四中A表示钾元素处于元素周期表的第________周期。
答案:
(1)原子
(2)16 得到
(3)非金属
(4)B
(5)4(或四)
(1)原子
(2)16 得到
(3)非金属
(4)B
(5)4(或四)
13.(4分)化学在生活、生产、医疗、科技等领域发挥着重要的作用。
(1)薯片是年轻人爱吃的食物。薯片包装袋总是鼓鼓的,猜测薯片包装袋内常用的填充气是__________,空气中该气体的体积分数约为__________。
(2)“打铁花”有着悠久的历史,其表演方式独特、文化内涵丰富,被列为国家级非物质文化遗产。铁燃烧时发生的反应是__________________________(用符号表达式表示)。
(3)我国自主研发出−271℃超流氦大型低温制冷装备,打破了发达国家的技术垄断。目前我国已掌握在−269℃下加压,将氦气转化为液氦的技术,从微观角度解释该过程发生改变的是______________。
(1)薯片是年轻人爱吃的食物。薯片包装袋总是鼓鼓的,猜测薯片包装袋内常用的填充气是__________,空气中该气体的体积分数约为__________。
(2)“打铁花”有着悠久的历史,其表演方式独特、文化内涵丰富,被列为国家级非物质文化遗产。铁燃烧时发生的反应是__________________________(用符号表达式表示)。
(3)我国自主研发出−271℃超流氦大型低温制冷装备,打破了发达国家的技术垄断。目前我国已掌握在−269℃下加压,将氦气转化为液氦的技术,从微观角度解释该过程发生改变的是______________。
答案:
(1)氮气 78%
(2)3Fe + 2O₂$\stackrel{点燃}{=\!=\!=}$Fe₃O₄
(3)氦原子间的间隔
(1)氮气 78%
(2)3Fe + 2O₂$\stackrel{点燃}{=\!=\!=}$Fe₃O₄
(3)氦原子间的间隔
14.(5分)空气是由多种气体组成的混合物,是一种宝贵的自然资源。
(1)空气中稀有气体的体积分数大约为________________。
(2)鱼虾能在水中生存是因为氧气易溶于水,这种说法____________(填“正确”或“不正确”)。
(3)因为氮气具有____________________的性质,所以充入食品包装袋内用于防腐。
(4)用微粒的观点解释:
①气态二氧化碳能被压缩成液态贮存在钢瓶中的原因是______________________。
②气态二氧化碳和液态二氧化碳的化学性质相同的原因是____________________。
(1)空气中稀有气体的体积分数大约为________________。
(2)鱼虾能在水中生存是因为氧气易溶于水,这种说法____________(填“正确”或“不正确”)。
(3)因为氮气具有____________________的性质,所以充入食品包装袋内用于防腐。
(4)用微粒的观点解释:
①气态二氧化碳能被压缩成液态贮存在钢瓶中的原因是______________________。
②气态二氧化碳和液态二氧化碳的化学性质相同的原因是____________________。
答案:
(1)0.94%
(2)不正确
(3)常温下化学性质稳定且无毒
(4)①分子之间有间隔 ②构成它们的分子相同
(1)0.94%
(2)不正确
(3)常温下化学性质稳定且无毒
(4)①分子之间有间隔 ②构成它们的分子相同
15.(5分)下面是自来水厂利用水库中的水生产自来水的主要流程:

(1)水库中的水属于________________(填“纯净物”或“混合物”)。
(2)①A池中通过________________(填操作名称)除去水中的固体杂质;②二氧化氯(ClO₂)是一种高效的消毒剂,其中氯元素的化合价为________。
(3)把自来水进一步净化为蒸馏水的实验方法是________________,实验室制取蒸馏水的蒸馏烧瓶里,通常要加入几粒沸石或碎瓷片,作用是____________________。

(1)水库中的水属于________________(填“纯净物”或“混合物”)。
(2)①A池中通过________________(填操作名称)除去水中的固体杂质;②二氧化氯(ClO₂)是一种高效的消毒剂,其中氯元素的化合价为________。
(3)把自来水进一步净化为蒸馏水的实验方法是________________,实验室制取蒸馏水的蒸馏烧瓶里,通常要加入几粒沸石或碎瓷片,作用是____________________。
答案:
(1)混合物
(2)①过滤 ②+4
(3)蒸馏 防止暴沸
(1)混合物
(2)①过滤 ②+4
(3)蒸馏 防止暴沸
16.(6分)下列A~D是初中化学中的四个实验装置。
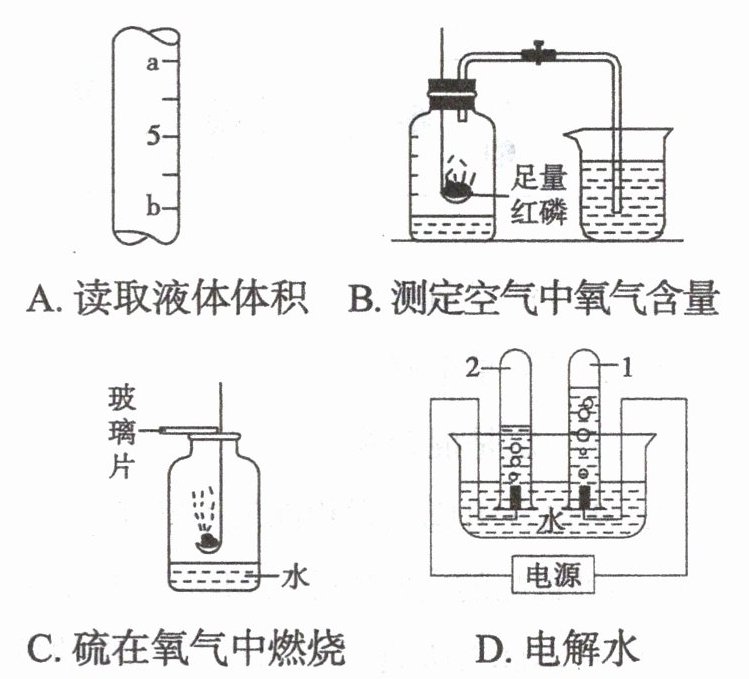
(1)A实验中用10mL量筒量取6mL蒸馏水,读数时量筒内的液体凹液面最低处应与A图中________(填“a”或“b”)处的刻度线保持水平。
(2)B实验成功的关键是______(填序号)。
①装置气密性好
②实验前夹紧止水夹
③红磷过量或足量
④冷却至室温后再打开止水夹
⑤选用教室内的空气
(3)C实验中水的作用是______________。
(4)D实验试管2中产生的气体是______(填化学式)。电解所发生反应的文字表达式为______________________________;该反应的基本反应类型为______________。

(1)A实验中用10mL量筒量取6mL蒸馏水,读数时量筒内的液体凹液面最低处应与A图中________(填“a”或“b”)处的刻度线保持水平。
(2)B实验成功的关键是______(填序号)。
①装置气密性好
②实验前夹紧止水夹
③红磷过量或足量
④冷却至室温后再打开止水夹
⑤选用教室内的空气
(3)C实验中水的作用是______________。
(4)D实验试管2中产生的气体是______(填化学式)。电解所发生反应的文字表达式为______________________________;该反应的基本反应类型为______________。
答案:
(1)a
(2)①②③④
(3)吸收反应生成的二氧化硫
(4)水$\stackrel{通电}{=\!=\!=}$氢气 + 氧气 分解反应
(1)a
(2)①②③④
(3)吸收反应生成的二氧化硫
(4)水$\stackrel{通电}{=\!=\!=}$氢气 + 氧气 分解反应
17.(5分)某校化学兴趣小组的同学根据实验室提供的仪器和试剂,在老师的指导下从图中选择装置进行了氧气的制备实验。

回答下列问题。
(1)写出仪器a的名称:________。
(2)甲同学从图中选择B、E装置制取氧气,收集氧气还可选用的装置是____________。
(3)乙同学称取一定质量的KMnO₄固体放入大试管中,将温度控制在250℃加热制取O₂。
写出该反应的文字表达式______________。实验结束时,乙同学发现用排水法收集到的O₂大于理论产量。针对这一现象,同学们进行了如下探究:
[提出猜想]
猜想I:反应生成的MnO₂分解放出O₂;
猜想II:反应生成的K₂MnO₄分解放出O₂;
猜想III:反应生成的K₂MnO₄和MnO₂分解都放出O₂。
[实验验证]
同学们分成两组,分别进行下列实验:
第一组同学取一定质量的MnO₂,在250℃条件下加热一段时间,冷却后测得MnO₂ 的质量不变,则猜想________错误;第二组同学取K₂MnO₄在250℃条件下加热,没有用测定质量的方法便得出了猜想II 正确的结论。该组同学选择的实验方法是______________________________。

回答下列问题。
(1)写出仪器a的名称:________。
(2)甲同学从图中选择B、E装置制取氧气,收集氧气还可选用的装置是____________。
(3)乙同学称取一定质量的KMnO₄固体放入大试管中,将温度控制在250℃加热制取O₂。
写出该反应的文字表达式______________。实验结束时,乙同学发现用排水法收集到的O₂大于理论产量。针对这一现象,同学们进行了如下探究:
[提出猜想]
猜想I:反应生成的MnO₂分解放出O₂;
猜想II:反应生成的K₂MnO₄分解放出O₂;
猜想III:反应生成的K₂MnO₄和MnO₂分解都放出O₂。
[实验验证]
同学们分成两组,分别进行下列实验:
第一组同学取一定质量的MnO₂,在250℃条件下加热一段时间,冷却后测得MnO₂ 的质量不变,则猜想________错误;第二组同学取K₂MnO₄在250℃条件下加热,没有用测定质量的方法便得出了猜想II 正确的结论。该组同学选择的实验方法是______________________________。
答案:
(1)锥形瓶
(2)C
(3)高锰酸钾$\stackrel{加热}{=\!=\!=}$锰酸钾 + 二氧化锰 + 氧气 I、III 用带火星的木条检验
(1)锥形瓶
(2)C
(3)高锰酸钾$\stackrel{加热}{=\!=\!=}$锰酸钾 + 二氧化锰 + 氧气 I、III 用带火星的木条检验
四、分析计算题(共3分)
18.山梨酸钾是常用的食品防腐剂,化学式为C₆H₇O₂K,相对分子质量为150。
(1)山梨酸钾由________种元素组成。
(2)求60g山梨酸钾中含钾元素的质量。
18.山梨酸钾是常用的食品防腐剂,化学式为C₆H₇O₂K,相对分子质量为150。
(1)山梨酸钾由________种元素组成。
(2)求60g山梨酸钾中含钾元素的质量。
答案:
(1)4(或四)
(2)解:60g山梨酸钾中含钾元素的质量为60g×($\frac{39}{150}$×100%) = 15.6g
答:60g山梨酸钾中含钾元素的质量为15.6g。
(1)4(或四)
(2)解:60g山梨酸钾中含钾元素的质量为60g×($\frac{39}{150}$×100%) = 15.6g
答:60g山梨酸钾中含钾元素的质量为15.6g。
1.下列验证质量守恒定律的实验中,能得出正确结论的是( )
(提示:锌和稀硫酸反应生成氢气。)
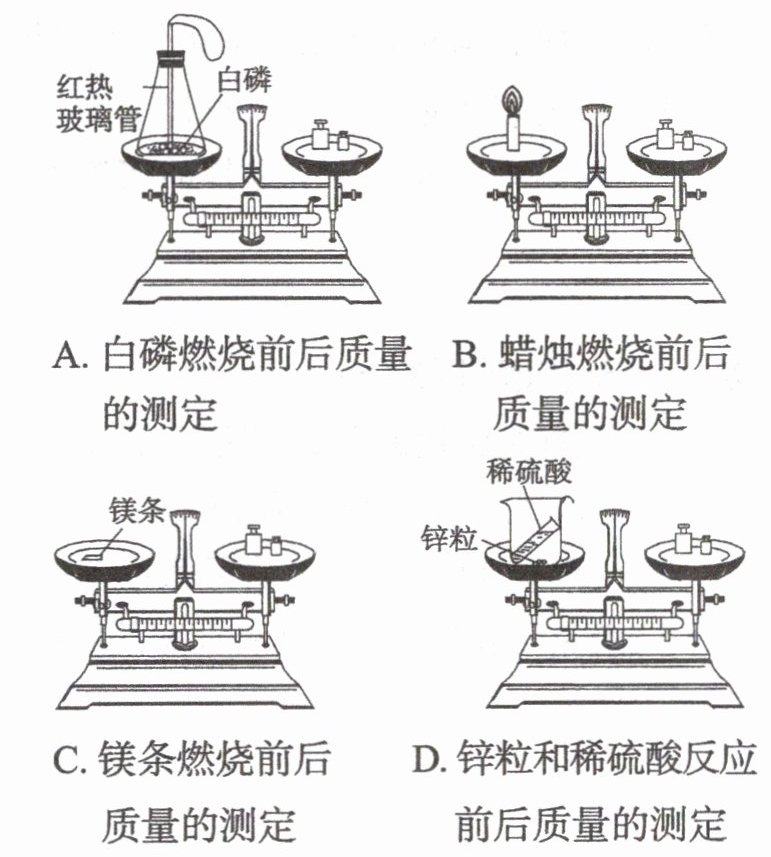
(提示:锌和稀硫酸反应生成氢气。)

答案:
A
2.如图是探究质量守恒定律的实验装置图,回答下列问题:
(提示:碳酸钙与稀盐酸反应的文字表达式为碳酸钙+盐酸−→氯化钙+水+二氧化碳。)

(1)该实验________(填“能”或“不能”)
探究质量守恒定律,原因是______________。
(2)用如图所示装置继续探究质量守恒定律,若试剂不变,改变装置的方法是________________________;若装置不变,改变试剂,可选用的一组试剂是________(举一例)。
(提示:碳酸钙与稀盐酸反应的文字表达式为碳酸钙+盐酸−→氯化钙+水+二氧化碳。)

(1)该实验________(填“能”或“不能”)
探究质量守恒定律,原因是______________。
(2)用如图所示装置继续探究质量守恒定律,若试剂不变,改变装置的方法是________________________;若装置不变,改变试剂,可选用的一组试剂是________(举一例)。
答案:
(1)不能 反应生成的二氧化碳气体会逸散到空气中
(2)反应在密闭容器中进行 铁钉与硫酸铜溶液(合理即可)
(1)不能 反应生成的二氧化碳气体会逸散到空气中
(2)反应在密闭容器中进行 铁钉与硫酸铜溶液(合理即可)
3.下列对化学反应前后质量变化的解释,不符合质量守恒定律的是(( )
A.高锰酸钾受热分解后固体剩余物的质量减小,是因为放出了氧气
B.蜡烛燃烧后质量变小,是因为蜡烛受热形成了石蜡蒸气
C.细铁丝在氧气中燃烧后,质量增大,是因为生成物中含有氧的质量
D.白磷在密闭容器中燃烧,反应前后总质量不变,是因为生成物都没有逸散
A.高锰酸钾受热分解后固体剩余物的质量减小,是因为放出了氧气
B.蜡烛燃烧后质量变小,是因为蜡烛受热形成了石蜡蒸气
C.细铁丝在氧气中燃烧后,质量增大,是因为生成物中含有氧的质量
D.白磷在密闭容器中燃烧,反应前后总质量不变,是因为生成物都没有逸散
答案:
B
4.在一密闭容器中,有甲、乙、丙、丁四种物质,一定条件下充分反应,测得反应前后各物质的质量如下表所示:

请根据质量守恒定律判断x的值为( )
A.50
B.40
C.10
D.70

请根据质量守恒定律判断x的值为( )
A.50
B.40
C.10
D.70
答案:
D
5.下列对“化学反应前后”的叙述不正确的是( )
A.物质的质量总和相同
B.元素的种类相同
C.物质的分子个数相同
D.原子的个数相同
A.物质的质量总和相同
B.元素的种类相同
C.物质的分子个数相同
D.原子的个数相同
答案:
C
查看更多完整答案,请扫码查看


