第77页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
- 第107页
- 第108页
三、实验探究题(共10分)
答案:
15.(2024山东淄博高青期末)(10分)碘(I₂)单质是一种由碘分子构成的非金属单质,碘单质能使淀粉变蓝色,小明同学利用碘进行了如图所示的实验,A中用湿润的馒头蘸取少量的固体碘,B中把湿润的馒头放在碘蒸气氛围中。碘蒸气在空气中呈紫红色,有刺激性气味,会对环境造成污染。
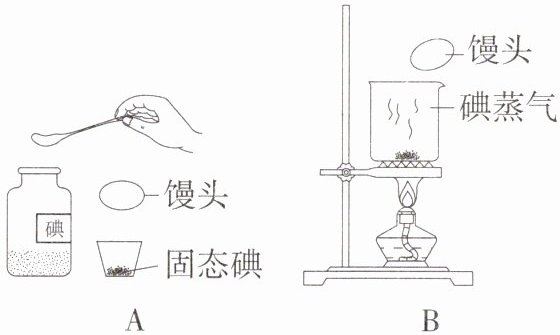
(1)A中,从广口瓶中取出固体碘,所用的仪器名称是______。B中,烧杯底部应垫上________。
(2)A和B中,湿润的馒头都显蓝色,原因是____________________。
(3)小芳同学认为B装置设计有不合理之处,原因是______________________________。

(1)A中,从广口瓶中取出固体碘,所用的仪器名称是______。B中,烧杯底部应垫上________。
(2)A和B中,湿润的馒头都显蓝色,原因是____________________。
(3)小芳同学认为B装置设计有不合理之处,原因是______________________________。
答案:
药匙@@陶土网@@碘单质能使淀粉变蓝色,固体碘、碘蒸气都是由碘分子构成的,同种分子的化学性质相同@@烧杯是敞口的,碘蒸气有刺激性气味,逸散到空气中会对环境造成污染 +5
四、计算题(共16分)
答案:
16.(2023四川内江中考)(8分)钙是人体必需的常量元素,人体缺钙时可适当使用补钙剂。碳酸钙(CaCO₃)、乳酸钙(C₆H₁₀O₆Ca)是补钙剂中常用的含钙物质。
(1)乳酸钙分子中氢原子和氧原子的个数比为______(填最简整数比,下同),乳酸钙中碳元素和钙元素的质量比为______。
(2)碳酸钙中钙元素的质量分数为______;从元素质量分数的角度推断,用______(填物质名称)作补钙剂中的含钙物质更好。
(1)乳酸钙分子中氢原子和氧原子的个数比为______(填最简整数比,下同),乳酸钙中碳元素和钙元素的质量比为______。
(2)碳酸钙中钙元素的质量分数为______;从元素质量分数的角度推断,用______(填物质名称)作补钙剂中的含钙物质更好。
答案:
$5:3$@@$9:5$@@40%@@碳酸钙
17.情境素材·健康教育(2023福建中考)(8分)为求证“喝反复烧开的饮用水会造成亚硝酸盐中毒”的真伪,学习小组以煮沸52次的桶装水为水样,利用下述反应测定亚硝酸盐的含量(以NaNO₂计):
2NaNO₂ + 2KI + 2H₂SO₄ === 2NO↑ + I₂ + 2H₂O + K₂SO₄ + Na₂SO₄
结果表明,1 L水样反应时产生了5.08×10⁻³ mg的I₂。
(1)计算1 L水样中NaNO₂的质量。
(2)查阅《食品安全国家标准(GB 2762 - 2022)》,经换算,合格饮用水中NaNO₂的含量应低于7.50×10⁻³ mg·L⁻¹。结合计算结果,得出的结论是:喝反复烧开的饮用水________(填“会”或“不会”)造成亚硝酸盐中毒。
2NaNO₂ + 2KI + 2H₂SO₄ === 2NO↑ + I₂ + 2H₂O + K₂SO₄ + Na₂SO₄
结果表明,1 L水样反应时产生了5.08×10⁻³ mg的I₂。
(1)计算1 L水样中NaNO₂的质量。
(2)查阅《食品安全国家标准(GB 2762 - 2022)》,经换算,合格饮用水中NaNO₂的含量应低于7.50×10⁻³ mg·L⁻¹。结合计算结果,得出的结论是:喝反复烧开的饮用水________(填“会”或“不会”)造成亚硝酸盐中毒。
答案:
(1)解:设 1 L 水样中NaNO₂的质量为$x$。
2NaNO₂ + 2KI + 2H₂SO₄ === 2NO↑ + I₂ + 2H₂O + K₂SO₄ + Na₂SO₄
138 254
x $5.08×10^{-3}\ mg$
$\frac{138}{254} = \frac{x}{5.08×10^{-3}\ mg}$
$x = 2.76×10^{-3}\ mg$
答:1 L 水样中 NaNO₂的质量为$2.76×10^{-3}\ mg$。
(2)不会
2NaNO₂ + 2KI + 2H₂SO₄ === 2NO↑ + I₂ + 2H₂O + K₂SO₄ + Na₂SO₄
138 254
x $5.08×10^{-3}\ mg$
$\frac{138}{254} = \frac{x}{5.08×10^{-3}\ mg}$
$x = 2.76×10^{-3}\ mg$
答:1 L 水样中 NaNO₂的质量为$2.76×10^{-3}\ mg$。
(2)不会
查看更多完整答案,请扫码查看


