第30页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
- 第107页
- 第108页
8.(2023 山东泰安岱岳期末改编)海洋中蕴含着丰富的资源,人们可以从海水中获取很多物质。海水制镁:从海水或卤水中制备金属镁流程如图所示。
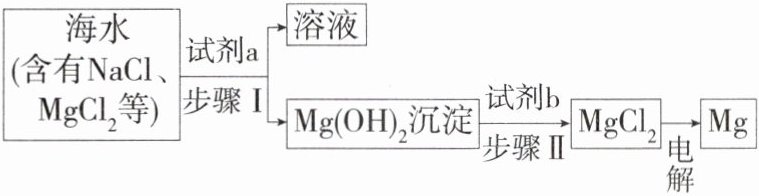
(1)为了使海水中含量较低的镁元素富集,加入的试剂 a 为__________,该反应的化学方程式为________________________,此过程富集镁元素的同时也达到了__________的目的。
(2)加入试剂 b 发生反应的化学方程式为____________________。
(3)步骤Ⅰ的实验操作为__________,该操作中使用的玻璃仪器有____________________。

(1)为了使海水中含量较低的镁元素富集,加入的试剂 a 为__________,该反应的化学方程式为________________________,此过程富集镁元素的同时也达到了__________的目的。
(2)加入试剂 b 发生反应的化学方程式为____________________。
(3)步骤Ⅰ的实验操作为__________,该操作中使用的玻璃仪器有____________________。
答案:
氢氧化钙(或石灰乳)@@$Ca(OH)_{2}+MgCl_{2}=Mg(OH)_{2}\downarrow +CaCl_{2}$@@提纯@@$Mg(OH)_{2}+2HCl=MgCl_{2}+2H_{2}O$@@过滤@@烧杯、玻璃棒、漏斗
9.(2023 四川德阳中考,7,★★☆)粗盐提纯过程中,除去难溶性杂质后的食盐水中,还含有 SO₄²⁻、Ca²⁺和 Mg²⁺等杂质离子。在实验室中去除这些杂质离子的实验步骤如下:
(1)取 100 mL 除去难溶性杂质的食盐水于烧杯中,依次加入过量的 BaCl₂溶液、NaOH 溶液和 Na₂CO₃溶液,将杂质离子转化为沉淀;
(2)过滤,得沉淀和滤液;
(3)向滤液中加入适量盐酸,得到精盐;
(4)将精盐水蒸发结晶,得到较纯净的氯化钠晶体。
依据以上实验步骤分析,下列说法正确的是 ( )
A. 步骤(1)中将 NaOH 溶液放在 Na₂CO₃溶液之后加入,不影响除杂效果
B. 步骤(2)过滤得到的沉淀中含有 3 种物质
C. 步骤(3)加入的盐酸若过量,会导致蒸发结晶得到的 NaCl 中含 HCl
D. 步骤(4)中需要加热至水分完全消失,再停止加热
(1)取 100 mL 除去难溶性杂质的食盐水于烧杯中,依次加入过量的 BaCl₂溶液、NaOH 溶液和 Na₂CO₃溶液,将杂质离子转化为沉淀;
(2)过滤,得沉淀和滤液;
(3)向滤液中加入适量盐酸,得到精盐;
(4)将精盐水蒸发结晶,得到较纯净的氯化钠晶体。
依据以上实验步骤分析,下列说法正确的是 ( )
A. 步骤(1)中将 NaOH 溶液放在 Na₂CO₃溶液之后加入,不影响除杂效果
B. 步骤(2)过滤得到的沉淀中含有 3 种物质
C. 步骤(3)加入的盐酸若过量,会导致蒸发结晶得到的 NaCl 中含 HCl
D. 步骤(4)中需要加热至水分完全消失,再停止加热
答案:
A
10.(2024 四川达州中考,48,★★☆)海水中含有丰富的化学资源,可提取食盐。如图是粗盐提纯的部分流程,粗盐中的杂质有泥沙、氯化钙、氯化镁,回答下列问题。(C9208002)
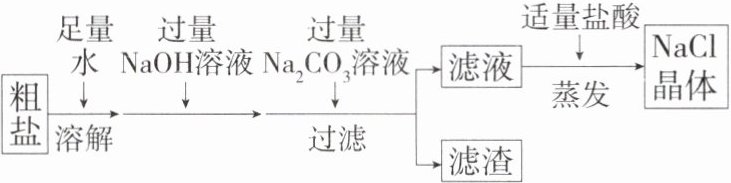
(1)粗盐溶解时,玻璃棒的作用是____________________。
(2)过滤后,滤渣中除泥沙外,还含有__________(填化学式);若滤液仍然浑浊,原因可能是______________(任写一条)。
(3)蒸发时,当蒸发皿中出现__________时即停止加热。

(1)粗盐溶解时,玻璃棒的作用是____________________。
(2)过滤后,滤渣中除泥沙外,还含有__________(填化学式);若滤液仍然浑浊,原因可能是______________(任写一条)。
(3)蒸发时,当蒸发皿中出现__________时即停止加热。
答案:
搅拌,加快溶解速率@@$Mg(OH)_{2}$、$CaCO_{3}$@@滤纸破损(或漏斗中液体液面高于滤纸的边缘等)@@较多固体
11.(2023 山东枣庄峄城期中,24,★★☆)氯碱工业以粗盐(主要成分是 NaCl,含少量泥沙和 CaCl₂、MgCl₂)为原料,生产氯气和氢氧化钠,模拟流程如图所示:
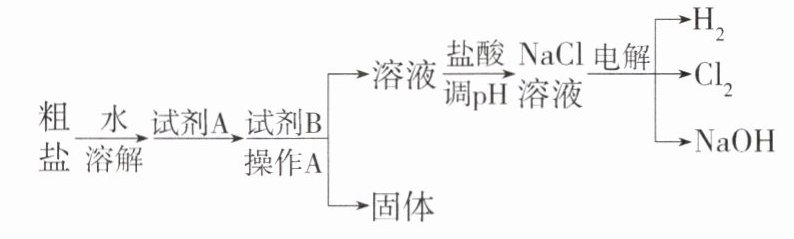
(1)试剂 A 与试剂 B 的组合为________(填序号)。
①KOH ②NaOH ③ $K_{2}C O_{3}$ ④$N a_{2}C O_{3}$
(2)操作 A 需使用玻璃棒,玻璃棒的作用是__________。
(3)流程中镁离子必须转化成______(填化学式)才能完全被除去。
(4)写出电解 NaCl 溶液的化学方程式:______________________________。
(5)该工业副产品 H₂目前还不能作为燃料被广泛应用,其理由是____________________(答一条)。

(1)试剂 A 与试剂 B 的组合为________(填序号)。
①KOH ②NaOH ③ $K_{2}C O_{3}$ ④$N a_{2}C O_{3}$
(2)操作 A 需使用玻璃棒,玻璃棒的作用是__________。
(3)流程中镁离子必须转化成______(填化学式)才能完全被除去。
(4)写出电解 NaCl 溶液的化学方程式:______________________________。
(5)该工业副产品 H₂目前还不能作为燃料被广泛应用,其理由是____________________(答一条)。
答案:
②④@@引流@@$Mg(OH)_{2}$@@$2NaCl + 2H_{2}O\xlongequal{通电}2NaOH + H_{2}\uparrow + Cl_{2}\uparrow$@@不易储存(合理即可)
查看更多完整答案,请扫码查看


