2025年优化探究同步导学案高中化学必修第一册人教版
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2025年优化探究同步导学案高中化学必修第一册人教版 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
第42页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
2.(2023·合肥三中高一段考)下列离子方程式书写正确的是 (
A.碳酸钙和 $\mathrm{CO}_2$ 反应:$\mathrm{CO}_3^{2-} + \mathrm{H}_2\mathrm{O} + \mathrm{CO}_2 = 2\mathrm{HCO}_3^-$
B.钠与水反应:$\mathrm{Na} + 2\mathrm{H}_2\mathrm{O} = \mathrm{Na}^+ + 2\mathrm{OH}^- + \mathrm{H}_2\uparrow$
C.硫酸铜溶液与氢氧化钡溶液反应:$\mathrm{SO}_4^{2-} + \mathrm{Ba}^{2+} = \mathrm{BaSO}_4\downarrow$
D.向小苏打溶液中加入过量的澄清石灰水:$\mathrm{HCO}_3^- + \mathrm{Ca}^{2+} + \mathrm{OH}^- = \mathrm{CaCO}_3\downarrow + \mathrm{H}_2\mathrm{O}$
D
)A.碳酸钙和 $\mathrm{CO}_2$ 反应:$\mathrm{CO}_3^{2-} + \mathrm{H}_2\mathrm{O} + \mathrm{CO}_2 = 2\mathrm{HCO}_3^-$
B.钠与水反应:$\mathrm{Na} + 2\mathrm{H}_2\mathrm{O} = \mathrm{Na}^+ + 2\mathrm{OH}^- + \mathrm{H}_2\uparrow$
C.硫酸铜溶液与氢氧化钡溶液反应:$\mathrm{SO}_4^{2-} + \mathrm{Ba}^{2+} = \mathrm{BaSO}_4\downarrow$
D.向小苏打溶液中加入过量的澄清石灰水:$\mathrm{HCO}_3^- + \mathrm{Ca}^{2+} + \mathrm{OH}^- = \mathrm{CaCO}_3\downarrow + \mathrm{H}_2\mathrm{O}$
答案:
2.D A.碳酸钙是固体不能拆,碳酸钙和$\mathrm{CO_2}$反应:$\mathrm{CaCO_3 +}$
$\mathrm{H_2O + CO_2 = 2HCO_3^- + Ca^{2+}}$,故A错误;B.电荷不守恒,
钠与水反应:$\mathrm{2Na + 2H_2O = 2Na^+ + 2OH^- + H_2\uparrow}$,故B
错误;C.硫酸铜溶液与氢氧化钡溶液反应生成氢氧化铜沉
淀和硫酸钡沉淀,$\mathrm{Cu^{2+} + 2OH^- + SO_4^{2-} + Ba^{2+} =}$
$\mathrm{BaSO_4\downarrow + Cu(OH)_2\downarrow}$,故C错误;D.按少量的物质定系
数,$\mathrm{HCO_3^- + Ca^{2+} + OH^- = CaCO_3\downarrow + H_2O}$,故D正确。
$\mathrm{H_2O + CO_2 = 2HCO_3^- + Ca^{2+}}$,故A错误;B.电荷不守恒,
钠与水反应:$\mathrm{2Na + 2H_2O = 2Na^+ + 2OH^- + H_2\uparrow}$,故B
错误;C.硫酸铜溶液与氢氧化钡溶液反应生成氢氧化铜沉
淀和硫酸钡沉淀,$\mathrm{Cu^{2+} + 2OH^- + SO_4^{2-} + Ba^{2+} =}$
$\mathrm{BaSO_4\downarrow + Cu(OH)_2\downarrow}$,故C错误;D.按少量的物质定系
数,$\mathrm{HCO_3^- + Ca^{2+} + OH^- = CaCO_3\downarrow + H_2O}$,故D正确。
3.(2023·巢湖高一期中)下列离子方程式书写正确的是 (
A.水中投入少量 $\mathrm{Na}_2\mathrm{O}_2$ 固体:$4\mathrm{Na}^+ + 2\mathrm{O}_2^{2-} + 2\mathrm{H}_2\mathrm{O} = 4\mathrm{Na}^+ + 4\mathrm{OH}^- + \mathrm{O}_2\uparrow$
B.$\mathrm{CuSO}_4$ 溶液中加入 $\mathrm{Ba(OH)}_2$ 溶液:$\mathrm{Ba}^{2+} + \mathrm{SO}_4^{2-} = \mathrm{BaSO}_4\downarrow$
C.醋酸与碳酸钙反应:$\mathrm{CaCO}_3 + 2\mathrm{H}^+ = \mathrm{Ca}^{2+} + \mathrm{CO}_2\uparrow + \mathrm{H}_2\mathrm{O}$
D.$\mathrm{Ca(HCO}_3\mathrm{)}_2$ 溶液与少量 $\mathrm{NaOH}$ 溶液反应:$\mathrm{HCO}_3^- + \mathrm{Ca}^{2+} + \mathrm{OH}^- = \mathrm{CaCO}_3\downarrow + \mathrm{H}_2\mathrm{O}$
D
)A.水中投入少量 $\mathrm{Na}_2\mathrm{O}_2$ 固体:$4\mathrm{Na}^+ + 2\mathrm{O}_2^{2-} + 2\mathrm{H}_2\mathrm{O} = 4\mathrm{Na}^+ + 4\mathrm{OH}^- + \mathrm{O}_2\uparrow$
B.$\mathrm{CuSO}_4$ 溶液中加入 $\mathrm{Ba(OH)}_2$ 溶液:$\mathrm{Ba}^{2+} + \mathrm{SO}_4^{2-} = \mathrm{BaSO}_4\downarrow$
C.醋酸与碳酸钙反应:$\mathrm{CaCO}_3 + 2\mathrm{H}^+ = \mathrm{Ca}^{2+} + \mathrm{CO}_2\uparrow + \mathrm{H}_2\mathrm{O}$
D.$\mathrm{Ca(HCO}_3\mathrm{)}_2$ 溶液与少量 $\mathrm{NaOH}$ 溶液反应:$\mathrm{HCO}_3^- + \mathrm{Ca}^{2+} + \mathrm{OH}^- = \mathrm{CaCO}_3\downarrow + \mathrm{H}_2\mathrm{O}$
答案:
3.D A.$\mathrm{Na_2O_2}$与水反应时,过氧化钠不能拆分,A错误;
B.$\mathrm{CuSO_4}$溶液中加入$\mathrm{Ba(OH)_2}$溶液反应生成$\mathrm{BaSO_4}$沉淀
和$\mathrm{Cu(OH)_2}$沉淀,正确的离子方程式为$\mathrm{Cu^{2+} + 2OH^- +}$
$\mathrm{Ba^{2+} + SO_4^{2-} = BaSO_4\downarrow + Cu(OH)_2\downarrow}$,B错误;C.醋酸
为弱酸,不能拆成离子,正确离子方程式为$\mathrm{CaCO_3 +}$
$\mathrm{2CH_3COOH = Ca^{2+} + 2CH_3COO^- + CO_2\uparrow + H_2O}$,
C错误;D.$\mathrm{Ca(HCO_3)_2}$溶液与少量$\mathrm{NaOH}$溶液反应生成碳
酸钙和水,离子方程式为$\mathrm{HCO_3^- + Ca^{2+} + OH^- = CaCO_3}$
$\mathrm{\downarrow + H_2O}$,D正确。
B.$\mathrm{CuSO_4}$溶液中加入$\mathrm{Ba(OH)_2}$溶液反应生成$\mathrm{BaSO_4}$沉淀
和$\mathrm{Cu(OH)_2}$沉淀,正确的离子方程式为$\mathrm{Cu^{2+} + 2OH^- +}$
$\mathrm{Ba^{2+} + SO_4^{2-} = BaSO_4\downarrow + Cu(OH)_2\downarrow}$,B错误;C.醋酸
为弱酸,不能拆成离子,正确离子方程式为$\mathrm{CaCO_3 +}$
$\mathrm{2CH_3COOH = Ca^{2+} + 2CH_3COO^- + CO_2\uparrow + H_2O}$,
C错误;D.$\mathrm{Ca(HCO_3)_2}$溶液与少量$\mathrm{NaOH}$溶液反应生成碳
酸钙和水,离子方程式为$\mathrm{HCO_3^- + Ca^{2+} + OH^- = CaCO_3}$
$\mathrm{\downarrow + H_2O}$,D正确。
4.(2023·山东青州高一期中)下列离子方程式书写正确的是 (
A.金属镁与稀盐酸反应有气泡逸出:$\mathrm{Mg} + 2\mathrm{H}^+ + 2\mathrm{Cl}^- = \mathrm{MgCl}_2 + \mathrm{H}_2\uparrow$
B.氯化钡溶液与稀硫酸反应有白色沉淀生成:$\mathrm{Ba}^{2+} + \mathrm{SO}_4^{2-} = \mathrm{BaSO}_4\downarrow$
C.碳酸钠溶液与盐酸反应有气泡逸出:$\mathrm{Na}_2\mathrm{CO}_3 + 2\mathrm{H}^+ = 2\mathrm{Na}^+ + \mathrm{CO}_2\uparrow + \mathrm{H}_2\mathrm{O}$
D.向氢氧化钠溶液中通入少量 $\mathrm{CO}_2$:$\mathrm{CO}_2 + \mathrm{OH}^- = \mathrm{HCO}_3^-$
B
)A.金属镁与稀盐酸反应有气泡逸出:$\mathrm{Mg} + 2\mathrm{H}^+ + 2\mathrm{Cl}^- = \mathrm{MgCl}_2 + \mathrm{H}_2\uparrow$
B.氯化钡溶液与稀硫酸反应有白色沉淀生成:$\mathrm{Ba}^{2+} + \mathrm{SO}_4^{2-} = \mathrm{BaSO}_4\downarrow$
C.碳酸钠溶液与盐酸反应有气泡逸出:$\mathrm{Na}_2\mathrm{CO}_3 + 2\mathrm{H}^+ = 2\mathrm{Na}^+ + \mathrm{CO}_2\uparrow + \mathrm{H}_2\mathrm{O}$
D.向氢氧化钠溶液中通入少量 $\mathrm{CO}_2$:$\mathrm{CO}_2 + \mathrm{OH}^- = \mathrm{HCO}_3^-$
答案:
4.B 镁与稀盐酸反应产生$\mathrm{H_2}$的离子方程式为$\mathrm{Mg + 2H^+ =}$
$\mathrm{Mg^{2+} + H_2\uparrow}$,故A项错误;$\mathrm{BaCl_2}$溶液与稀硫酸反应产
生白色沉淀的离子方程式为$\mathrm{Ba^{2+} + SO_4^{2-} = BaSO_4\downarrow}$,故
B项正确;$\mathrm{Na_2CO_3}$溶液与盐酸反应逸出气泡的离子方程式
为$\mathrm{CO_3^{2-} + 2H^+ = CO_2\uparrow + H_2O}$,故C项错误;向$\mathrm{NaOH}$
溶液中通入少量$\mathrm{CO_2}$的离子方程式为$\mathrm{CO_2 + 2OH^- =}$
$\mathrm{CO_3^{2-} + H_2O}$,故D项错误。
$\mathrm{Mg^{2+} + H_2\uparrow}$,故A项错误;$\mathrm{BaCl_2}$溶液与稀硫酸反应产
生白色沉淀的离子方程式为$\mathrm{Ba^{2+} + SO_4^{2-} = BaSO_4\downarrow}$,故
B项正确;$\mathrm{Na_2CO_3}$溶液与盐酸反应逸出气泡的离子方程式
为$\mathrm{CO_3^{2-} + 2H^+ = CO_2\uparrow + H_2O}$,故C项错误;向$\mathrm{NaOH}$
溶液中通入少量$\mathrm{CO_2}$的离子方程式为$\mathrm{CO_2 + 2OH^- =}$
$\mathrm{CO_3^{2-} + H_2O}$,故D项错误。
5.(2024·山东齐河高一期末)下列离子方程式书
写正确的是 (
A.向 $\mathrm{Ca(ClO)}_2$ 溶液中通入过量的 $\mathrm{CO}_2$ 气体:$\mathrm{Ca}^{2+} + 2\mathrm{ClO}^- + \mathrm{H}_2\mathrm{O} + \mathrm{CO}_2 = \mathrm{CaCO}_3\downarrow + 2\mathrm{HClO}$
B.向 $\mathrm{Na}_2\mathrm{CO}_3$ 溶液中滴加少量的稀盐酸:$\mathrm{CO}_3^{2-} + 2\mathrm{H}^+ = \mathrm{CO}_2\uparrow + \mathrm{H}_2\mathrm{O}$
C.向 $\mathrm{CuSO}_4$ 溶液中滴入少量的 $\mathrm{Ba(OH)}_2$ 溶液:$\mathrm{SO}_4^{2-} + \mathrm{Ba}^{2+} = \mathrm{BaSO}_4\downarrow$
D.$\mathrm{CaCO}_3$ 与足量稀硝酸反应:$\mathrm{CaCO}_3 + 2\mathrm{H}^+ = \mathrm{H}_2\mathrm{O} + \mathrm{CO}_2\uparrow + \mathrm{Ca}^{2+}$
写正确的是 (
D
)A.向 $\mathrm{Ca(ClO)}_2$ 溶液中通入过量的 $\mathrm{CO}_2$ 气体:$\mathrm{Ca}^{2+} + 2\mathrm{ClO}^- + \mathrm{H}_2\mathrm{O} + \mathrm{CO}_2 = \mathrm{CaCO}_3\downarrow + 2\mathrm{HClO}$
B.向 $\mathrm{Na}_2\mathrm{CO}_3$ 溶液中滴加少量的稀盐酸:$\mathrm{CO}_3^{2-} + 2\mathrm{H}^+ = \mathrm{CO}_2\uparrow + \mathrm{H}_2\mathrm{O}$
C.向 $\mathrm{CuSO}_4$ 溶液中滴入少量的 $\mathrm{Ba(OH)}_2$ 溶液:$\mathrm{SO}_4^{2-} + \mathrm{Ba}^{2+} = \mathrm{BaSO}_4\downarrow$
D.$\mathrm{CaCO}_3$ 与足量稀硝酸反应:$\mathrm{CaCO}_3 + 2\mathrm{H}^+ = \mathrm{H}_2\mathrm{O} + \mathrm{CO}_2\uparrow + \mathrm{Ca}^{2+}$
答案:
5.D 过量$\mathrm{CO_2}$与$\mathrm{Ca(ClO)_2}$溶液反应,应生成$\mathrm{Ca(HCO_3)_2}$和
$\mathrm{HClO}$,其离子方程式为$\mathrm{ClO^- + H_2O + CO_2 = HCO_3^- +}$
$\mathrm{HClO}$,A项错误;少量的稀盐酸与$\mathrm{Na_2CO_3}$溶液反应,产物
为$\mathrm{NaHCO_3}$和$\mathrm{NaCl}$,其离子方程式为$\mathrm{CO_3^{2-} + H^+ =}$
$\mathrm{HCO_3^-}$,B项错误;$\mathrm{Ba^{2+}}$与$\mathrm{SO_4^{2-}}$反应的同时,$\mathrm{Cu^{2+}}$与$\mathrm{OH^-}$
反应生成$\mathrm{Cu(OH)_2}$沉淀,C项错误。
$\mathrm{HClO}$,其离子方程式为$\mathrm{ClO^- + H_2O + CO_2 = HCO_3^- +}$
$\mathrm{HClO}$,A项错误;少量的稀盐酸与$\mathrm{Na_2CO_3}$溶液反应,产物
为$\mathrm{NaHCO_3}$和$\mathrm{NaCl}$,其离子方程式为$\mathrm{CO_3^{2-} + H^+ =}$
$\mathrm{HCO_3^-}$,B项错误;$\mathrm{Ba^{2+}}$与$\mathrm{SO_4^{2-}}$反应的同时,$\mathrm{Cu^{2+}}$与$\mathrm{OH^-}$
反应生成$\mathrm{Cu(OH)_2}$沉淀,C项错误。
1. 三种常见离子的检验
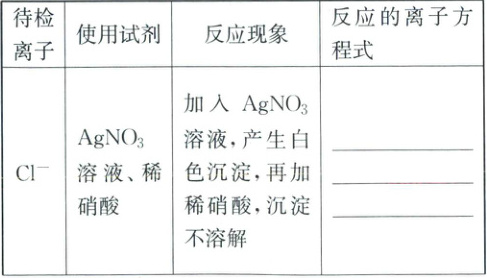

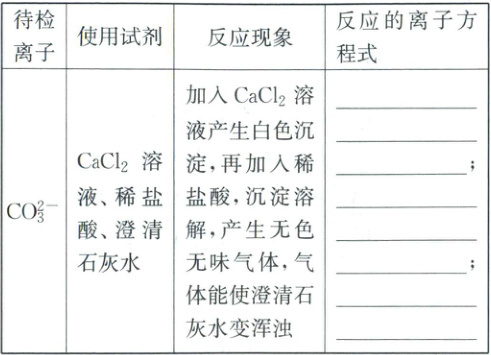



答案:
1. $\mathrm{Cl^- + Ag^+ \longrightarrow AgCl \downarrow}$ $\mathrm{Ba^{2+} + SO_4^{2-} \longrightarrow BaSO_4 \downarrow}$ $\mathrm{Ca^{2+} + CO_3^{2-} \longrightarrow CaCO_3 \downarrow}$ $\mathrm{CaCO_3 + 2H^+ \longrightarrow Ca^{2+} + CO_2 \uparrow + H_2O}$ $\mathrm{CO_2 + Ca^{2+} + 2OH^- \longrightarrow CaCO_3 \downarrow + H_2O}$
查看更多完整答案,请扫码查看


