2025年优化探究同步导学案高中化学必修第一册人教版
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2025年优化探究同步导学案高中化学必修第一册人教版 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
第16页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
1. (新情境命题)目前科学家已发现一种新型氢分子,其化学式为${H_{3}}$,在相同条件下,等质量的${H_{3}}$和${H_{2}}$相同的是
A.原子数
B.分子数
C.体积
D.物质的量
A
A.原子数
B.分子数
C.体积
D.物质的量
答案:
1.A 由于$H_3$和$H_2$均由氢原子构成,因此等质量的$H_3$和$H_2$分子中具有相同的原子数,因此它们的分子数一定不同,因而体积不同,物质的量也不同,A项正确。
2. 如图所示,相同状况下,分别用氯化氢和四种混合气体吹出体积相等的五个气球。A、B、C、D四个气球中,与氯化氢所含原子数一定相等的是
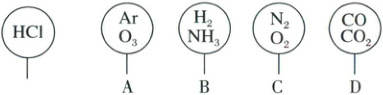
C

答案:
2.C 相同状况下、体积相等的气球中,气体的物质的量相等。HCl是双原子分子,只要混合气体的平均原子数等于2即满足题意。A项有可能等于2,B项一定大于2,C项一定等于2,D项一定大于2,故选C。
3. 在一个恒容密闭容器中盛有$11\ g\ X$气体($ X$的摩尔质量为$44\ g· mol^{-1}$)时,压强为$1× 10^{4}\ Pa$。如果在相同温度下,把更多的气体$ X$充入容器,使容器内压强增至$5× 10^{4}\ Pa$,这时容器内气体$ X$的分子数约为
A.$3.3× 10^{25}$
B.$3.3× 10^{24}$
C.$7.5× 10^{23}$
D.$7.5× 10^{22}$
C
A.$3.3× 10^{25}$
B.$3.3× 10^{24}$
C.$7.5× 10^{23}$
D.$7.5× 10^{22}$
答案:
3.C 11 g X气体的物质的量$n_1=\frac{11 g}{44 g· mol^{-1}}=0.25 mol$,由同温同体积时$\frac{n_1}{n_2}=\frac{p_1}{p_2}$得,$\frac{0.25 mol}{n_2}=\frac{1×10^4 Pa}{5×10^4 Pa}$,$n_2=1.25 mol$,$N=1.25 mol×6.02×10^{23} mol^{-1}≈7.5×10^{23}$,C项正确。
4. 同温同压下等质量的${SO_{2}}$气体和${CO_{2}}$气体,下列有关比较的叙述正确的是
①密度比为$16:11$ ②密度比为$11:16$
③体积比为$16:11$ ④体积比为$11:16$
①④
(填序号)。①密度比为$16:11$ ②密度比为$11:16$
③体积比为$16:11$ ④体积比为$11:16$
答案:
4.答案:①④
解析:同温同压下,$\frac{\rho(SO_2)}{\rho(CO_2)}=\frac{M(SO_2)}{M(CO_2)}=\frac{64}{44}=\frac{16}{11}$,故①正确;
$\frac{n(SO_2)}{n(CO_2)}=\frac{\frac{mg}{64 g· mol^{-1}}}{\frac{mg}{44 g· mol^{-1}}}=\frac{11}{16}$,因同温同压下,$\frac{V(SO_2)}{V(CO_2)}=\frac{n(SO_2)}{n(CO_2)}=\frac{11}{16}$,故④正确。
解析:同温同压下,$\frac{\rho(SO_2)}{\rho(CO_2)}=\frac{M(SO_2)}{M(CO_2)}=\frac{64}{44}=\frac{16}{11}$,故①正确;
$\frac{n(SO_2)}{n(CO_2)}=\frac{\frac{mg}{64 g· mol^{-1}}}{\frac{mg}{44 g· mol^{-1}}}=\frac{11}{16}$,因同温同压下,$\frac{V(SO_2)}{V(CO_2)}=\frac{n(SO_2)}{n(CO_2)}=\frac{11}{16}$,故④正确。
1. 定义:
单位体积
溶液所含溶质 B 的物质的量
叫作溶质 B 的物质的量浓度。符号为$c_{B}$。
答案:
1. 定义:单位体积 物质的量
2. 物质的量浓度表达式:$c_{B} =$
$\frac{n_{\mathrm{B}}}{V}$
。
答案:
2. $\frac{n_{\mathrm{B}}}{V}$
3. 常用单位:
$\mathrm{mol· L^{-1}}$
或$mol· m^{-3}$。
答案:
3. $\mathrm{mol· L^{-1}}$
4. 意义:$1\ mol· L^{-1}\ NaCl$溶液表示
$1\ \mathrm{L\ NaCl}$溶液
中含有$1\ mol\ NaCl$。
答案:
4. $1\ \mathrm{L\ NaCl}$溶液
[正误判断]
1. 表示溶液的组成除了可以用溶质的质量分数,还可以用溶质的物质的量浓度。 (
2. 标准状况下,将$2.24\ L\ HCl$气体溶于$1\ L$水,得到$3.24\ L$溶液。 (
3. $0.3\ mol· L^{-1}\ Na_{2}SO_{4}$溶液中含有$Na^{+}$和$SO^{2-}_{4}$的总物质的量为$0.9\ mol$。 (
1. 表示溶液的组成除了可以用溶质的质量分数,还可以用溶质的物质的量浓度。 (
√
)2. 标准状况下,将$2.24\ L\ HCl$气体溶于$1\ L$水,得到$3.24\ L$溶液。 (
×
)3. $0.3\ mol· L^{-1}\ Na_{2}SO_{4}$溶液中含有$Na^{+}$和$SO^{2-}_{4}$的总物质的量为$0.9\ mol$。 (
×
)
答案:
1.√ 2.× 3.×
1. $1\ L\ 0.5\ mol· L^{-1}$的$Al_{2}(SO_{4})_{3}$溶液中
$n(Al^{3 +}) =$
$n(SO^{2-}_{4}) =$
$c[Al_{2}(SO_{4})_{3}]:c(Al^{3 +}):c(SO^{2-}_{4}) =$
由此可知,同一溶质的不同微粒的浓度之比等于
。
$n(Al^{3 +}) =$
$1\ \mathrm{mol}$
,$c(Al^{3 +}) =$$1\ \mathrm{mol· L^{-1}}$
,$n(SO^{2-}_{4}) =$
$1.5\ \mathrm{mol}$
,$c(SO^{2-}_{4}) =$$1.5\ \mathrm{mol· L^{-1}}$
,$c[Al_{2}(SO_{4})_{3}]:c(Al^{3 +}):c(SO^{2-}_{4}) =$
$1:2:3$
。由此可知,同一溶质的不同微粒的浓度之比等于
微粒个数之比
。
答案:
1.提示:$1\ \mathrm{mol}$ $1\ \mathrm{mol· L^{-1}}$ $1.5\ \mathrm{mol}$ $1.5\ \mathrm{mol· L^{-1}}$ $1:2:3$ 微粒个数之比
查看更多完整答案,请扫码查看


