2025年优化探究同步导学案高中化学必修第一册人教版
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2025年优化探究同步导学案高中化学必修第一册人教版 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
第17页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
2. 某$BaCl_{2}$溶液中,测得$c(Cl^{-}) = 0.5\ mol· L^{-1}$,则$c(Ba^{2 +}) =$
$0.25\ \mathrm{mol· L^{-1}}$
。
答案:
2.提示:$0.25\ \mathrm{mol· L^{-1}}$
3. 下列与$0.2\ mol· L^{-1}\ AlCl_{3}$溶液中$c(Cl^{-})$相同的是
①$0.2\ mol· L^{-1}\ NaCl$溶液
②$0.3\ mol· L^{-1}\ MgCl_{2}$溶液
③$0.6\ mol· L^{-1}\ KCl$溶液
④$0.2\ mol· L^{-1}\ BaCl_{2}$溶液
②③
(填序号)。①$0.2\ mol· L^{-1}\ NaCl$溶液
②$0.3\ mol· L^{-1}\ MgCl_{2}$溶液
③$0.6\ mol· L^{-1}\ KCl$溶液
④$0.2\ mol· L^{-1}\ BaCl_{2}$溶液
答案:
3.提示:②③
1. (2024·安徽亳州高一期末) 血液中葡萄糖(简称血糖,分子式为$C_{6}H_{12}O_{6}$)的含量,常以$``mmol· L^{-1}"$和$``mg· dL^{-1}"$为参考指标$(1\ L = 10\ dL)$,以$``mmol· L^{-1}"$表示时,人的血糖正常值在$4.9\sim 6.1\ mmol· L^{-1}$之间。下列说法正确的是 (
A.葡萄糖的摩尔质量为 180
B.无偿献血后,体内血糖浓度会变小
C.某病人$1\ mL$血液中含葡萄糖$0.60\ mg$,相当于$3.3\ mol· L^{-1}$
D.若病人的血糖检测结果为$92\ mg· dL^{-1}$,则血糖值在正常范围内
D
)A.葡萄糖的摩尔质量为 180
B.无偿献血后,体内血糖浓度会变小
C.某病人$1\ mL$血液中含葡萄糖$0.60\ mg$,相当于$3.3\ mol· L^{-1}$
D.若病人的血糖检测结果为$92\ mg· dL^{-1}$,则血糖值在正常范围内
答案:
1.D A.葡萄糖的摩尔质量为$180\ \mathrm{g· mol^{-1}}$,A错误;B.浓度与所取溶液体积无关,所以无偿献血后,体内血糖浓度不变,B错误;C.某病人$1\ \mathrm{mL}$血液中含葡萄糖$0.60\ \mathrm{mg}$,其物质的量浓度为$3.3\ \mathrm{mmol· L^{-1}}$,C错误;D.若病人的血糖检测结果为$92\ \mathrm{mg· dL^{-1}}$,则血糖值为$5.11\ \mathrm{mmol· L^{-1}}$,在正常范围内,D正确。
2. 将$2.86\ g\ Na_{2}CO_{3}· 10H_{2}O$溶于水配成$1\ L$溶液,则:
(1) 该溶液的溶质为
(2) 从所配溶液中取出$10\ mL$溶液,取出溶液的物质的量浓度为
(1) 该溶液的溶质为
$\mathrm{Na_{2}CO_{3}}$
,其物质的量浓度为0.01
$mol· L^{-1}$。(2) 从所配溶液中取出$10\ mL$溶液,取出溶液的物质的量浓度为
0.01
$mol· L^{-1}$,$Na^{+}$的物质的量浓度为0.02
$mol· L^{-1}$。
答案:
2.
(1)$\mathrm{Na_{2}CO_{3}}$ $0.01$
(2)$0.01$ $0.02$
(1)$\mathrm{Na_{2}CO_{3}}$ $0.01$
(2)$0.01$ $0.02$
1. 容量瓶
(1) 容量瓶的构造
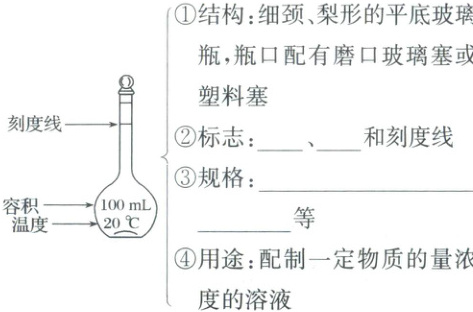
(2) 容量瓶的选择与使用
①容量瓶是配制一定物质的量浓度溶液的专用仪器,选择容量瓶应遵循$``$大而近$"$的原则:所配溶液的体积等于或略小于容量瓶的容积。
②使用前要检验容量瓶是否漏水。检验程序:加水→塞瓶塞→倒立→查漏→正立,瓶塞旋转$180^{\circ}$→倒立→查漏。
(1) 容量瓶的构造

(2) 容量瓶的选择与使用
①容量瓶是配制一定物质的量浓度溶液的专用仪器,选择容量瓶应遵循$``$大而近$"$的原则:所配溶液的体积等于或略小于容量瓶的容积。
②使用前要检验容量瓶是否漏水。检验程序:加水→塞瓶塞→倒立→查漏→正立,瓶塞旋转$180^{\circ}$→倒立→查漏。
答案:
1.
(1)温度 容积 $100\ \mathrm{mL}$、$250\ \mathrm{mL}$、$500\ \mathrm{mL}$、$1000\ \mathrm{mL}$
(1)温度 容积 $100\ \mathrm{mL}$、$250\ \mathrm{mL}$、$500\ \mathrm{mL}$、$1000\ \mathrm{mL}$
2. 配制一定量物质的量浓度的溶液
以配制100\ mL\
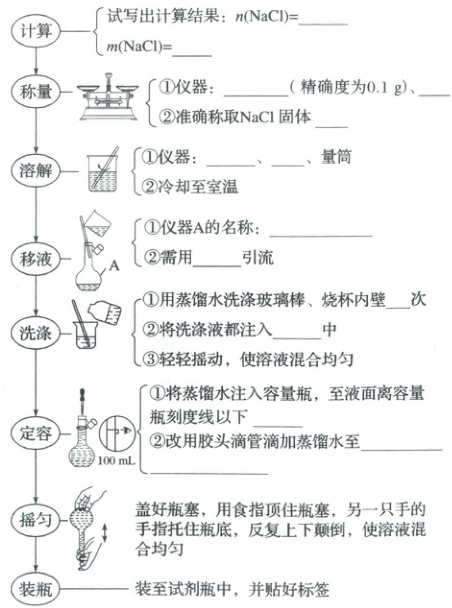
以配制100\ mL\
$0.1\ \mathrm{mol}$
$1.00\ mol· L^{-1}$氯化钠溶液为例
答案:
2.$0.1\ \mathrm{mol}$ $5.85\ \mathrm{g}$ 托盘天平 药匙 $5.9\ \mathrm{g}$ 玻璃棒 烧杯 $100\ \mathrm{mL}$容量瓶 玻璃棒 $2\sim3$ 容量瓶 $1\sim2\ \mathrm{cm}$ 溶液的凹液面与刻度线相切
查看更多完整答案,请扫码查看


