第44页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
- 第107页
- 第108页
- 第109页
- 第110页
- 第111页
- 第112页
- 第113页
- 第114页
- 第115页
- 第116页
- 第117页
- 第118页
- 第119页
- 第120页
- 第121页
- 第122页
- 第123页
- 第124页
- 第125页
- 第126页
- 第127页
- 第128页
- 第129页
- 第130页
- 第131页
- 第132页
- 第133页
- 第134页
- 第135页
- 第136页
- 第137页
- 第138页
- 第139页
- 第140页
- 第141页
- 第142页
- 第143页
- 第144页
- 第145页
- 第146页
- 第147页
- 第148页
- 第149页
- 第150页
- 第151页
- 第152页
- 第153页
- 第154页
- 第155页
- 第156页
- 第157页
- 第158页
- 第159页
- 第160页
- 第161页
- 第162页
- 第163页
- 第164页
- 第165页
- 第166页
- 第167页
- 第168页
- 第169页
- 第170页
- 第171页
- 第172页
- 第173页
- 第174页
- 第175页
- 第176页
16. 水是重要的物质,在实验室中常用于溶解物质、配制溶液。
(1)在50 mL水(密度为1 g/mL)中溶解一定量$KNO_3$固体的操作如图所示。请根据如图所示的实验现象和溶解度曲线回答下列问题。
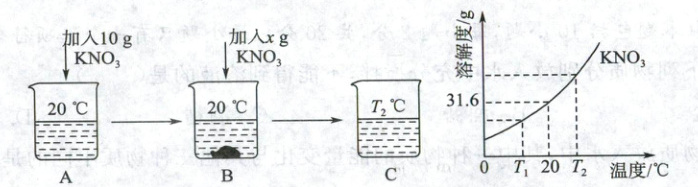
① A、B、C中一定是饱和溶液的是
② 当x=
③ 硝酸钾从溶液中析出晶体常用降温结晶的方法,这是因为
(2)现用氯化钠固体配制50 g溶质质量分数为10%的氯化钠溶液。
① 主要的实验步骤是:计算、
② 整个配制过程中,不需要用到的实验仪器是(
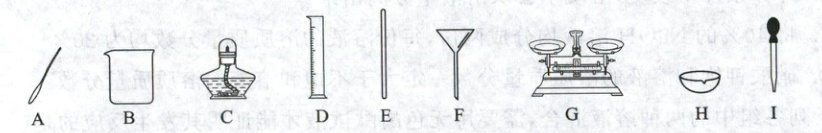
③ 量取所需水的体积时,应选用
(1)在50 mL水(密度为1 g/mL)中溶解一定量$KNO_3$固体的操作如图所示。请根据如图所示的实验现象和溶解度曲线回答下列问题。

① A、B、C中一定是饱和溶液的是
B
,一定是不饱和溶液的是A
(1分)。② 当x=
5.8
时,B中恰好没有固体剩余。③ 硝酸钾从溶液中析出晶体常用降温结晶的方法,这是因为
硝酸钾的溶解度随温度升高而显著增大
。(2)现用氯化钠固体配制50 g溶质质量分数为10%的氯化钠溶液。
① 主要的实验步骤是:计算、
称量
、溶解
、装瓶保存。② 整个配制过程中,不需要用到的实验仪器是(
C
)(填下图的仪器字母,1分)。
③ 量取所需水的体积时,应选用
50
(填“10”“50”或“100”,1分)mL量筒。在量取水的体积时俯视读数,则配制溶液的溶质质量分数会偏大
(填“偏大”“偏小”或“不变”)。
答案:
(1)① B;A
② 5.8
③ 硝酸钾的溶解度随温度升高而显著增大
(2)① 称量;溶解
② C
③ 50;偏大
② 5.8
③ 硝酸钾的溶解度随温度升高而显著增大
(2)① 称量;溶解
② C
③ 50;偏大
17. 海洋蕴藏着丰富的资源,人类应合理开发利用。
Ⅰ. 了解海水资源
(1)海水中含钠总量约$4×10^{13}$ t,“钠”指的是 (
(2)海水中还含有KCl和$MgSO_4$等物质,其在不同温度时的溶解度如表所示,下图是对应的溶解度曲线。
① 图中曲线 (
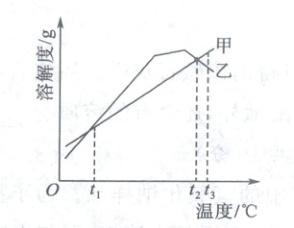
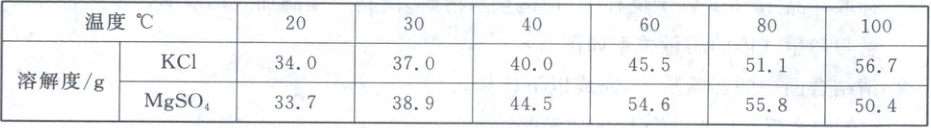
② 40℃时,将50 g KCl固体加入100 g水中, (
③ $t_2$℃时,将等质量的甲、乙两物质的饱和溶液降温到$t_1$℃,析出晶体的质量相等。上述说法 (
④ 现有$t_3$℃时100 g $MgSO_4$的饱和溶液,逐渐降温经$t_2$℃直至$t_1$℃,其溶质质量分数的变化趋势为
Ⅱ. 海水资源化利用线
(3)海水制镁:查找资料,提供两种提取金属镁的路径方案(如图所示)。
方案1:富集$MgCl_1$的海水 石灰乳 $Mg(OH)_2$ 稀盐酸 $MgCl_2$溶液 … Mg
方案2:菱镁矿 煅烧 MgO 硅铁还原 Mg

结合地理位置,因地制宜,选择烟台市提取金属镁的最佳方案。你的选择是方案 (
Ⅰ. 了解海水资源
(1)海水中含钠总量约$4×10^{13}$ t,“钠”指的是 (
元素
)。(2)海水中还含有KCl和$MgSO_4$等物质,其在不同温度时的溶解度如表所示,下图是对应的溶解度曲线。
① 图中曲线 (
乙
)代表KCl的溶解度曲线。

② 40℃时,将50 g KCl固体加入100 g水中, (
不能
)得到150 g KCl溶液。③ $t_2$℃时,将等质量的甲、乙两物质的饱和溶液降温到$t_1$℃,析出晶体的质量相等。上述说法 (
错误
)。④ 现有$t_3$℃时100 g $MgSO_4$的饱和溶液,逐渐降温经$t_2$℃直至$t_1$℃,其溶质质量分数的变化趋势为
先不变后减小
。Ⅱ. 海水资源化利用线
(3)海水制镁:查找资料,提供两种提取金属镁的路径方案(如图所示)。
方案1:富集$MgCl_1$的海水 石灰乳 $Mg(OH)_2$ 稀盐酸 $MgCl_2$溶液 … Mg
方案2:菱镁矿 煅烧 MgO 硅铁还原 Mg

结合地理位置,因地制宜,选择烟台市提取金属镁的最佳方案。你的选择是方案 (
1
),理由是 烟台沿海,海水资源丰富,原料易得;方案1成本较低(或步骤简便等)
。
答案:
(1)元素;
(2)①乙;②不能;③错误;④先不变后减小;
(3)1;烟台沿海,海水资源丰富,原料易得;方案1成本较低(或步骤简便等)
(1)元素;
(2)①乙;②不能;③错误;④先不变后减小;
(3)1;烟台沿海,海水资源丰富,原料易得;方案1成本较低(或步骤简便等)
查看更多完整答案,请扫码查看


