第105页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
- 第107页
- 第108页
- 第109页
- 第110页
- 第111页
- 第112页
- 第113页
- 第114页
- 第115页
- 第116页
- 第117页
- 第118页
- 第119页
- 第120页
- 第121页
- 第122页
- 第123页
- 第124页
- 第125页
- 第126页
- 第127页
- 第128页
- 第129页
- 第130页
- 第131页
- 第132页
- 第133页
- 第134页
- 第135页
- 第136页
- 第137页
- 第138页
- 第139页
- 第140页
- 第141页
- 第142页
- 第143页
- 第144页
- 第145页
- 第146页
- 第147页
- 第148页
- 第149页
- 第150页
- 第151页
- 第152页
- 第153页
- 第154页
- 第155页
- 第156页
- 第157页
- 第158页
- 第159页
- 第160页
- 第161页
- 第162页
- 第163页
- 第164页
- 第165页
- 第166页
- 第167页
- 第168页
- 第169页
- 第170页
- 第171页
- 第172页
- 第173页
- 第174页
- 第175页
- 第176页
19. 某兴趣小组在实验室探究氢氧化钠与稀硫酸是否发生化学反应。
Ⅰ. 从温度变化角度探究
(1)甲同学将NaOH固体放入盛有稀硫酸的试管中并振荡,管壁发烫,得出“酸碱中和反应放出热量”的结论。乙同学认为推理不合理,理由是
(2)乙同学将实验改进如下:将稀硫酸慢慢滴入装有NaOH溶液的烧杯中,用温度计测出NaOH溶液温度随加入稀硫酸质量的变化(如图所示):
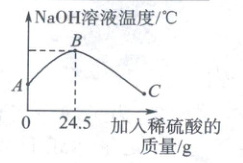
① 由图可知,稀硫酸与NaOH溶液发生的反应
② 从A到B的过程中,烧杯中溶液的pH逐渐
③ 从B到C的过程中,烧杯内溶液中的阴离子有
Ⅱ. 从指示剂角度探究
(3)向盛有无色酚酞试液和NaOH溶液的烧杯中滴加稀硫酸至恰好完全反应,证明反应发生的实验现象为
(4)中和反应的微观实质是
Ⅲ. 从产物角度探究
(5)丁同学认为NaOH溶液与稀硫酸混合没有明显现象,于是他想借助下列物质来验证反应是否发生,你觉得可行的是
A. pH试纸
$B. BaCl_2 $
$C. CuSO_4 $
$D. KNO_3$
Ⅰ. 从温度变化角度探究
(1)甲同学将NaOH固体放入盛有稀硫酸的试管中并振荡,管壁发烫,得出“酸碱中和反应放出热量”的结论。乙同学认为推理不合理,理由是
NaOH固体溶于水也会放出热量,无法说明就是中和反应放热
。 (2)乙同学将实验改进如下:将稀硫酸慢慢滴入装有NaOH溶液的烧杯中,用温度计测出NaOH溶液温度随加入稀硫酸质量的变化(如图所示):

① 由图可知,稀硫酸与NaOH溶液发生的反应
放出
(填“放出”或“吸收”)热量,B点表示的含义是稀硫酸与NaOH溶液恰好完全反应
。 ② 从A到B的过程中,烧杯中溶液的pH逐渐
减小
(填“增大”“减小”或“不变”)。 ③ 从B到C的过程中,烧杯内溶液中的阴离子有
SO₄²⁻
(填离子符号)。 Ⅱ. 从指示剂角度探究
(3)向盛有无色酚酞试液和NaOH溶液的烧杯中滴加稀硫酸至恰好完全反应,证明反应发生的实验现象为
溶液由红色恰好变为无色
。 (4)中和反应的微观实质是
氢离子和氢氧根离子结合生成水分子
。 Ⅲ. 从产物角度探究
(5)丁同学认为NaOH溶液与稀硫酸混合没有明显现象,于是他想借助下列物质来验证反应是否发生,你觉得可行的是
AC
(填字母)。 A. pH试纸
$B. BaCl_2 $
$C. CuSO_4 $
$D. KNO_3$
答案:
(1)NaOH固体溶于水也会放出热量,无法说明就是中和反应放热
(2)①放出;稀硫酸与NaOH溶液恰好完全反应
②减小
③$SO_{4}^{2 - }$
(3)溶液由红色恰好变为无色
(4)氢离子和氢氧根离子结合生成水分子
(5)AC
(1)NaOH固体溶于水也会放出热量,无法说明就是中和反应放热
(2)①放出;稀硫酸与NaOH溶液恰好完全反应
②减小
③$SO_{4}^{2 - }$
(3)溶液由红色恰好变为无色
(4)氢离子和氢氧根离子结合生成水分子
(5)AC
20. 海洋是巨大的资源宝库,人类应合理开发利用。下面是某市海水综合利用的部分工艺流程图(部分过程和产物略),据图回答下列问题。
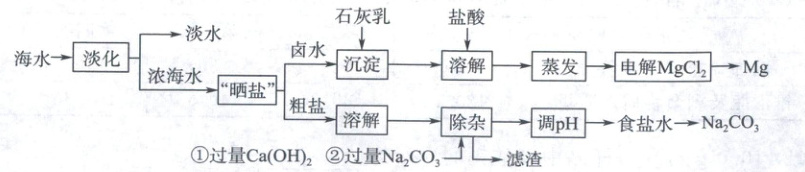
(1)海水淡化:可采用膜隔离技术(如图所示),下列分析错误的是(
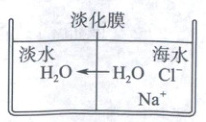
A. 右侧池中氯化钠的质量分数不变
B. 用膜分离技术可以得到淡水
C. 淡化膜可用普通滤纸代替
(2)海水“晒盐”:“晒盐”时,采用的结晶方法是
(3)海水制镁:在用卤水制镁的过程中,没有涉及的基本化学反应类型是
(4)海水“制碱”:在用粗盐(含$MgCl_2、$$CaCl_2$杂质)制纯碱的过程中,除杂时,向粗盐水中先后加入① 过量的$Ca(OH)_2$溶液、② 过量的$Na_2CO_3$溶液。试剂①②的顺序是否可以颠倒?为什么?

(1)海水淡化:可采用膜隔离技术(如图所示),下列分析错误的是(
AC
)。 
A. 右侧池中氯化钠的质量分数不变
B. 用膜分离技术可以得到淡水
C. 淡化膜可用普通滤纸代替
(2)海水“晒盐”:“晒盐”时,采用的结晶方法是
蒸发结晶
;海水晒盐后得到的卤水是氯化钠的饱和
溶液。 (3)海水制镁:在用卤水制镁的过程中,没有涉及的基本化学反应类型是
化合反应
。向卤水中加入石灰乳,发生反应的化学方程式是$MgCl_{2}+Ca(OH)_{2}=Mg(OH)_{2}\downarrow +CaCl_{2}$
。 (4)海水“制碱”:在用粗盐(含$MgCl_2、$$CaCl_2$杂质)制纯碱的过程中,除杂时,向粗盐水中先后加入① 过量的$Ca(OH)_2$溶液、② 过量的$Na_2CO_3$溶液。试剂①②的顺序是否可以颠倒?为什么?
不可以;若颠倒,过量的$Ca(OH)_2$无法除去,会引入新杂质
。
答案:
(1)AC
(2)蒸发结晶;饱和
(3)化合反应;$MgCl_{2}+Ca(OH)_{2}=Mg(OH)_{2}\downarrow +CaCl_{2}$
(4)不可以;若颠倒,过量的$Ca(OH)_{2}$无法除去,会引入新杂质
(1)AC
(2)蒸发结晶;饱和
(3)化合反应;$MgCl_{2}+Ca(OH)_{2}=Mg(OH)_{2}\downarrow +CaCl_{2}$
(4)不可以;若颠倒,过量的$Ca(OH)_{2}$无法除去,会引入新杂质
查看更多完整答案,请扫码查看


