第176页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
- 第107页
- 第108页
- 第109页
- 第110页
- 第111页
- 第112页
- 第113页
- 第114页
- 第115页
- 第116页
- 第117页
- 第118页
- 第119页
- 第120页
- 第121页
- 第122页
- 第123页
- 第124页
- 第125页
- 第126页
- 第127页
- 第128页
- 第129页
- 第130页
- 第131页
- 第132页
- 第133页
- 第134页
- 第135页
- 第136页
- 第137页
- 第138页
- 第139页
- 第140页
- 第141页
- 第142页
- 第143页
- 第144页
- 第145页
- 第146页
- 第147页
- 第148页
- 第149页
- 第150页
- 第151页
- 第152页
- 第153页
- 第154页
- 第155页
- 第156页
- 第157页
- 第158页
- 第159页
- 第160页
- 第161页
- 第162页
- 第163页
- 第164页
- 第165页
- 第166页
- 第167页
- 第168页
- 第169页
- 第170页
- 第171页
- 第172页
- 第173页
- 第174页
- 第175页
- 第176页
16. (8 分)氢能具有广阔的发展前景,安全高效的制氢和储氢是氢能成为主要能源的关键。
(1) 电解水制氢气可用铁作电极,是利用了铁的
(2) 高压气态储氢是通过恒温高压将氢气储存在压力容器中,从微观角度解释,该过程主要发生改变的是
(3) 氢化物储氢是利用氢气与金属(如 $Al$)反应生成金属氢化物(如 $AlH_{3}$),从而进行氢的储存。该过程属于
(4) 活性炭具有疏松多孔的结构,可用作储氢材料,这是利用了活性炭的
(5) 我国科学家实现了天然气 $(CH_{4})$ 制氢的突破,在 $400\ ^{\circ}C$ 条件下,将天然气与水蒸气直接转化为氢气与二氧化碳。请写出该反应的化学方程式:
(6) 氢气是未来理想的清洁能源,原因是
(1) 电解水制氢气可用铁作电极,是利用了铁的
导电性
。氢气在与电源 负
极相连的电极上产生。(2) 高压气态储氢是通过恒温高压将氢气储存在压力容器中,从微观角度解释,该过程主要发生改变的是
分子间间隔
。(3) 氢化物储氢是利用氢气与金属(如 $Al$)反应生成金属氢化物(如 $AlH_{3}$),从而进行氢的储存。该过程属于
化学变化
(填“物理变化”或“化学变化”)。(4) 活性炭具有疏松多孔的结构,可用作储氢材料,这是利用了活性炭的
吸附
性。(5) 我国科学家实现了天然气 $(CH_{4})$ 制氢的突破,在 $400\ ^{\circ}C$ 条件下,将天然气与水蒸气直接转化为氢气与二氧化碳。请写出该反应的化学方程式:
CH₄ + 2H₂O $\xlongequal{400^{\circ}C}$ 4H₂ + CO₂
。(6) 氢气是未来理想的清洁能源,原因是
燃烧产物是水,无污染(或热值高)
。
答案:
(1)导电性;负
(2)分子间间隔
(3)化学变化
(4)吸附
(5)CH₄ + 2H₂O $\xlongequal{400^{\circ}C}$ 4H₂ + CO₂
(6)燃烧产物是水,无污染(或热值高)
(1)导电性;负
(2)分子间间隔
(3)化学变化
(4)吸附
(5)CH₄ + 2H₂O $\xlongequal{400^{\circ}C}$ 4H₂ + CO₂
(6)燃烧产物是水,无污染(或热值高)
17. (10 分)海洋是一个巨大的资源宝库。
(Ⅰ)海水资源综合利用的部分途径如图所示。
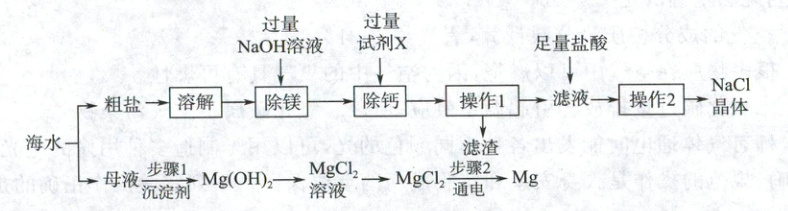
已知: 粗盐中的杂质有泥沙、$MgCl_{2}$、$CaCl_{2}$,流程中部分操作及试剂已省略。
(1) 试剂 $X$ 的作用是除去粗盐中的 $Ca^{2+}$,则试剂 $X$ 为 (
(2) “操作 1”中玻璃棒的作用是
(3) 滤渣中除泥沙外,还含有
(4) 实际生产中,步骤 1 常选用
(5) 步骤 2 需电解
(Ⅱ)二氧化氯 $(ClO_{2})$ 可用于自来水消毒,用氯化钠生产 $ClO_{2}$ 的主要流程如图所示。
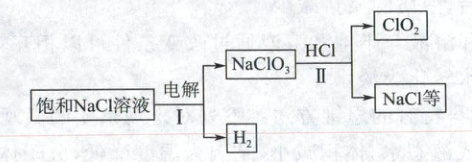
(1) 反应Ⅰ中的反应物一定有水,从元素守恒角度,说明理由:
(2) 上述流程所示的含氯物质中,氯元素的化合价共有
(3) 上述流程中,可循环利用的物质是
(Ⅰ)海水资源综合利用的部分途径如图所示。

已知: 粗盐中的杂质有泥沙、$MgCl_{2}$、$CaCl_{2}$,流程中部分操作及试剂已省略。
(1) 试剂 $X$ 的作用是除去粗盐中的 $Ca^{2+}$,则试剂 $X$ 为 (
Na₂CO₃
)。(2) “操作 1”中玻璃棒的作用是
引流
,“操作 2”的名称为 蒸发(或蒸发结晶)
。(3) 滤渣中除泥沙外,还含有
Mg(OH)₂、CaCO₃
。(4) 实际生产中,步骤 1 常选用
Ca(OH)₂(或氢氧化钙)
作为沉淀剂。(5) 步骤 2 需电解
熔融
状态的 $MgCl_{2}$ 以获得金属镁。(Ⅱ)二氧化氯 $(ClO_{2})$ 可用于自来水消毒,用氯化钠生产 $ClO_{2}$ 的主要流程如图所示。

(1) 反应Ⅰ中的反应物一定有水,从元素守恒角度,说明理由:
产物中含氢元素,反应物氯化钠不含氢元素,故一定有水
。(2) 上述流程所示的含氯物质中,氯元素的化合价共有
3
种(填数字)。(3) 上述流程中,可循环利用的物质是
NaCl(或氯化钠)
。
答案:
(Ⅰ)
(1)Na₂CO₃
(2)引流;蒸发(或蒸发结晶)
(3)Mg(OH)₂、CaCO₃
(4)Ca(OH)₂(或氢氧化钙)
(5)熔融
(Ⅱ)
(1)产物中含氢元素,反应物氯化钠不含氢元素,故一定有水
(2)3
(3)NaCl(或氯化钠)
(1)Na₂CO₃
(2)引流;蒸发(或蒸发结晶)
(3)Mg(OH)₂、CaCO₃
(4)Ca(OH)₂(或氢氧化钙)
(5)熔融
(Ⅱ)
(1)产物中含氢元素,反应物氯化钠不含氢元素,故一定有水
(2)3
(3)NaCl(或氯化钠)
查看更多完整答案,请扫码查看


