第62页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
19. 酸雨主要是因为大量燃烧含硫量高的煤而形成的,此外,各种机动车排放的尾气也是形成酸雨的重要原因。
【提出问题】通过实验证明煤中含有碳元素和硫元素。
【查阅资料】(1)“二氧化硫能使高锰酸钾溶液褪色(由紫红色变为无色),该反应的化学方程式为$5SO_2 + 2KMnO_4 + 2H_2O = K_2SO_4 + 2MnSO_4 + 2X”。$这个化学方程式中最后一种物质X的化学式是
(2)“二氧化硫和二氧化碳一样,也能使澄清石灰水变浑浊。”请写出二氧化硫与澄清石灰水反应的化学方程式:
根据上述资料,甲同学、乙同学和丙同学分别设计实验方案进行探究。
【实验探究】(3)甲同学进行了如图1中A、B两步实验。
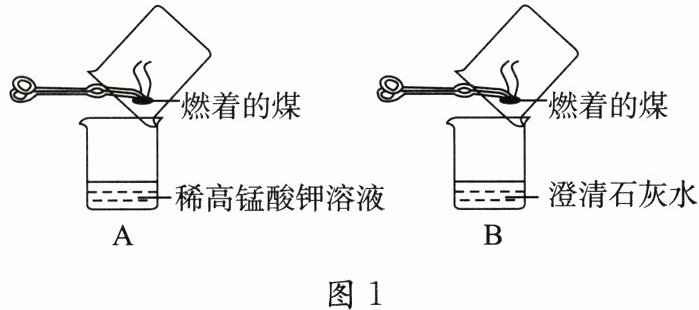
“实验现象”:A中稀高锰酸钾溶液褪色,B中澄清石灰水变浑浊。
“得出结论”:煤燃烧生成二氧化硫和二氧化碳,证明煤中含有碳元素和硫元素。
(4)乙同学认为甲同学的实验方案不合理,其理由是
(5)丙同学进行了如图2所示实验(部分装置在图中略去)。

【探究与结论】(6)图2中E装置的作用是
(7)利用图2装置证明煤中含有碳元素和硫元素的现象是
【提出问题】通过实验证明煤中含有碳元素和硫元素。
【查阅资料】(1)“二氧化硫能使高锰酸钾溶液褪色(由紫红色变为无色),该反应的化学方程式为$5SO_2 + 2KMnO_4 + 2H_2O = K_2SO_4 + 2MnSO_4 + 2X”。$这个化学方程式中最后一种物质X的化学式是
${H2SO4}$
。(2)“二氧化硫和二氧化碳一样,也能使澄清石灰水变浑浊。”请写出二氧化硫与澄清石灰水反应的化学方程式:
${SO2 +Ca(OH)2\xlongequal{}CaSO3\downarrow +H2O}$
。根据上述资料,甲同学、乙同学和丙同学分别设计实验方案进行探究。
【实验探究】(3)甲同学进行了如图1中A、B两步实验。

“实验现象”:A中稀高锰酸钾溶液褪色,B中澄清石灰水变浑浊。
“得出结论”:煤燃烧生成二氧化硫和二氧化碳,证明煤中含有碳元素和硫元素。
(4)乙同学认为甲同学的实验方案不合理,其理由是
二氧化硫也会使澄清石灰水变浑浊,无法证明煤中含有碳元素
。(5)丙同学进行了如图2所示实验(部分装置在图中略去)。

【探究与结论】(6)图2中E装置的作用是
除去过多的二氧化硫(或排除二氧化硫的干扰)
。(7)利用图2装置证明煤中含有碳元素和硫元素的现象是
D中的溶液褪色,E中的溶液不褪色,F中澄清石灰水变浑浊
。
答案:
(1)${H2SO4}$
(2)${SO2 +Ca(OH)2\xlongequal{}CaSO3\downarrow +H2O}$
(4)二氧化硫也会使澄清石灰水变浑浊,无法证明煤中含有碳元素
(6)除去过多的二氧化硫(或排除二氧化硫的干扰)
(7)D中的溶液褪色,E中的溶液不褪色,F中澄清石灰水变浑浊解析
(1)由化学方程式${5SO2 +2KMnO4 +2H2O\xlongequal{}K2SO4 +2MnSO4 +2X}$知:反应前比反应后多4个氢原子,2个硫原子,8个氧原子,所以每个X中有2个氢原子,1个硫原子,4个氧原子,即X的化学式为${H2SO4}$。
(2)二氧化硫与澄清石灰水反应的化学方程式为${SO2 +Ca(OH)2\xlongequal{}CaSO3\downarrow +H2O}$。
(4)乙同学认为甲同学的实验方案不合理,其理由是:二氧化硫也会使澄清石灰水变浑浊,无法证明煤中含有碳元素。
(6)图E装置内的浓高锰酸钾溶液能与二氧化硫反应,所以它的作用是除去过多的二氧化硫或排除二氧化硫的干扰。
(7)证明煤中含有碳元素和硫元素的现象是:丙同学的实验中D中的溶液褪色,E中的溶液不褪色,F中澄清石灰水变浑浊,D中褪色说明有二氧化硫,E中不褪色说明二氧化硫已经被除去,F中变浑浊说明有二氧化碳生成,可以说明有碳元素和硫元素。
(1)${H2SO4}$
(2)${SO2 +Ca(OH)2\xlongequal{}CaSO3\downarrow +H2O}$
(4)二氧化硫也会使澄清石灰水变浑浊,无法证明煤中含有碳元素
(6)除去过多的二氧化硫(或排除二氧化硫的干扰)
(7)D中的溶液褪色,E中的溶液不褪色,F中澄清石灰水变浑浊解析
(1)由化学方程式${5SO2 +2KMnO4 +2H2O\xlongequal{}K2SO4 +2MnSO4 +2X}$知:反应前比反应后多4个氢原子,2个硫原子,8个氧原子,所以每个X中有2个氢原子,1个硫原子,4个氧原子,即X的化学式为${H2SO4}$。
(2)二氧化硫与澄清石灰水反应的化学方程式为${SO2 +Ca(OH)2\xlongequal{}CaSO3\downarrow +H2O}$。
(4)乙同学认为甲同学的实验方案不合理,其理由是:二氧化硫也会使澄清石灰水变浑浊,无法证明煤中含有碳元素。
(6)图E装置内的浓高锰酸钾溶液能与二氧化硫反应,所以它的作用是除去过多的二氧化硫或排除二氧化硫的干扰。
(7)证明煤中含有碳元素和硫元素的现象是:丙同学的实验中D中的溶液褪色,E中的溶液不褪色,F中澄清石灰水变浑浊,D中褪色说明有二氧化硫,E中不褪色说明二氧化硫已经被除去,F中变浑浊说明有二氧化碳生成,可以说明有碳元素和硫元素。
查看更多完整答案,请扫码查看


