第24页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
9. 化学与人体健康密切相关。市场上有“高钙牛奶”“加氟牙膏”“葡萄糖酸锌”等商品,这里的“钙、氟、锌”应理解为(
A.原子
B.离子
C.分子
D.元素
D
)A.原子
B.离子
C.分子
D.元素
答案:
D 解析 物质是由元素组成的,市场上的"高钙牛奶""加氟牙膏""葡萄糖酸锌"等商品提到的"钙、氟、锌"应理解为元素。
10. 分子、原子和离子是构成物质的粒子。下列有关三种粒子的说法正确的是(
A.同种原子可以构成不同的分子
B.原子通过得失电子形成离子,但离子不能转变成原子
C.物质有热胀冷缩现象,主要是因为物质中的粒子大小随温度的改变而改变
D.分子、原子的根本区别是分子可以再分,原子不能再分
A
)A.同种原子可以构成不同的分子
B.原子通过得失电子形成离子,但离子不能转变成原子
C.物质有热胀冷缩现象,主要是因为物质中的粒子大小随温度的改变而改变
D.分子、原子的根本区别是分子可以再分,原子不能再分
答案:
A 解析 同种原子可以构成不同的分子,如氧原子可构成氧分子、臭氧分子,A项正确;原子可以通过得到或失去电子变为离子,离子也能转变成原子,B项错误;物质有热胀冷缩现象,主要是因为物质中的粒子间隔随温度的改变而改变,C项错误;分子、原子的根本区别是在化学变化中,分子可以再分,原子不能再分,D项错误。
11. 对下列有关粒子结构示意图的说法正确的是(

A.③和④的元素在元素周期表中属于同一周期
B.③和⑦表示同一种粒子
C.①和②、⑤和⑥的化学性质相似
D.④是具有稳定结构的原子
D
)
A.③和④的元素在元素周期表中属于同一周期
B.③和⑦表示同一种粒子
C.①和②、⑤和⑥的化学性质相似
D.④是具有稳定结构的原子
答案:
D 解析 ③的质子数是11,对应原子的核外有三个电子层,位于第三周期;④的质子数是10,原子的核外有2个电子层,位于第二周期,二者在元素周期表中不属于同一周期,A项错误。同种粒子要求质子数及核外电子数均一致,而③和⑦的核外电子数不同,B项错误。①只有一个电子层,最外层有2个电子,属于稳定结构,②的最外层有2个电子,小于4,易失去电子,①和②的化学性质不相似;⑤和⑥最外层电子数相同,化学性质相似,C项错误。在④中,质子数等于核外电子数,最外层的电子数是8,是具有稳定结构的原子,D项正确。
12. 如图是元素周期表的一部分,下列有关说法正确的是(
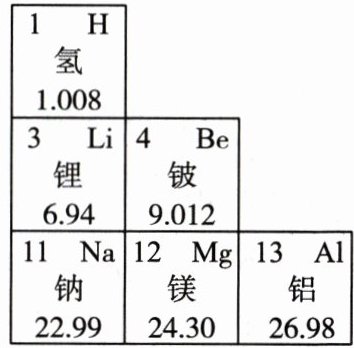
A.图中有四种金属元素
B.铍的相对原子质量为 9.012
C.氢、锂、钠三种元素位于同一周期
D.钠、镁、铝三种元素的化学性质相似
B
)
A.图中有四种金属元素
B.铍的相对原子质量为 9.012
C.氢、锂、钠三种元素位于同一周期
D.钠、镁、铝三种元素的化学性质相似
答案:
B 解析 题图中有锂、铍、钠、镁、铝五种金属元素,A项错误;由题图中铍元素的单元格信息可知,铍的相对原子质量为9.012,B项正确;氢、锂、钠三种元素位于同一族,C项错误;钠、镁、铝三种元素位于同一周期,其原子核外最外层电子数不相等,化学性质不相似,D项错误。
13. 具有相同质子数的粒子一定是(
A.同一种原子
B.同一种分子
C.同一种元素
D.无法确定
D
)A.同一种原子
B.同一种分子
C.同一种元素
D.无法确定
答案:
D 解析 水分子、氨分子等具有相同的质子数(都是10),但它们不是同一种原子,A项错误。钠离子和铵根离子的质子数都是11,则具有相同质子数的粒子可能是两种离子;再如水分子和氖原子具有相同的质子数(均是10),则它们也可能是一种分子和一种原子,B项错误。水分子、氨分子、氖原子等具有相同的质子数(都是10),但不属于同种元素,C项错误。综上所述,具有相同质子数的粒子,可能为分子、原子、离子,D项正确。
14. 1911 年,著名物理学家卢瑟福为探索原子的内部结构进行了实验。在用一束带正电的、质量比电子大得多的高速运动的α粒子轰击金箔时发现:
①大多数α粒子能穿透金箔而不改变原来的运动方向;
②一小部分α粒子改变了原来的运动方向;
③有极少部分α粒子被反弹了回来。
下列对原子结构的认识错误的是(
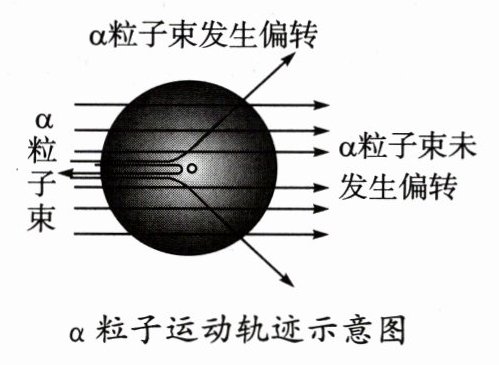
A.原子核体积很小
B.原子核带正电
C.α粒子的质量很小
D.电子带负电
①大多数α粒子能穿透金箔而不改变原来的运动方向;
②一小部分α粒子改变了原来的运动方向;
③有极少部分α粒子被反弹了回来。
下列对原子结构的认识错误的是(
D
)
A.原子核体积很小
B.原子核带正电
C.α粒子的质量很小
D.电子带负电
答案:
D 解析 根据大多数α粒子能穿透金箔而不改变原来的运动方向,说明金原子中有一个很大的空间,原子不是实心球体;一小部分α粒子改变了原来的运动方向,说明原子核内有带正电的粒子;有极少部分α粒子被反弹了回来,说明金原子核体积很小,质量大。由此可知:原子核体积很小,A项正确;原子核带正电,B项正确;α粒子的质量很小,C项正确;不能说明电子带负电,D项错误。
查看更多完整答案,请扫码查看


