第82页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
4. (2024·无锡滨湖模拟节选)碳是人类最早接触到的元素之一,也是人类最早利用的元素之一。
Ⅰ. 自然之碳。
46 亿年前,在地心引力的作用下,碳以尘埃的形式慢慢进入地幔中。外来天体对地球“轰炸”形成岩浆,大量的二氧化碳和水蒸气从岩浆中释放,成为地球的早期大气层。当温度下降,水蒸气凝结成雨水汇入了海洋。
(1)写出雨水与二氧化碳的反应:______(用化学方程式表示)。
Ⅱ. 生命之碳。
38 亿年前,在海洋深处,碳元素与氧、氢、氮等元素结合在一起,演变成细胞。从此以碳元素为核心的碳基生命诞生。
(2)兴趣小组同学用如图所示实验装置测定人体呼出气体中二氧化碳的含量。实验步骤如下:

①连接装置后关闭止水夹,拉动注射器活塞,白鹤鹑蛋向下滑动。把注射器活塞推回顶端,白鹤鹑蛋向上滑动至原处。上述操作说明装置______(填“漏气”或“不漏气”)。②用同一白鹤鹑蛋反复多次实验发现,注射器内气体体积(mL)改变量与白鹤鹑蛋下降距离(cm)的比例均约为 4.8∶1。③用 625 mL 的烧瓶收集一瓶人体呼出的气体,恒压漏斗内加入足量氢氧化钠溶液(氢氧化钠溶液能吸收二氧化碳)。记录量气管内白鹤鹑蛋对应的刻度为 a cm。④打开恒压漏斗开关,同时打开磁力搅拌器使反应充分后,打开止水夹,白鹤鹑蛋向下滑动至刻度 b cm 处。⑤多次实验取平均值,测得 a= 20、b= 25.5。
(3)数据分析:人体呼出气体中二氧化碳的体积分数为______(计算结果保留 1 位小数)。
Ⅲ. 绿色之碳。
(4)目前科学家们正致力于攻克“碳中和”的难题。
方法一:将 CO_2转化成甲醇(CH_3OH):${CO2 + 3H2 \xlongequal{催化剂} CH3OH + H2O}。$
①甲醇在常温下是一种无色液体,易溶于水,沸点为 64.7 ℃,若需将甲醇从其水溶液中分离出来,可采用______(填“过滤”或“蒸馏”)的方法。
方法二:将 CO_2和 H_2O 转化为甲烷(CH_4)和氧气。催化剂的催化效率和甲烷的生成速率随温度的变化关系如图所示。
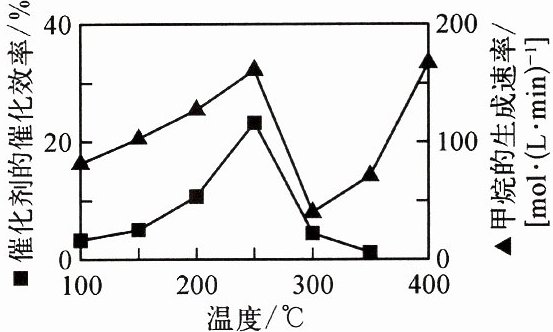
②300 ℃~400 ℃,甲烷生成速率加快的原因是______。
(5)关于绿色之碳,下列说法正确的是______(填字母)。
a. 二氧化碳会导致温室效应,对人类的生活有百害无一利
b. 人类过多的工业活动打破了碳循环的平衡
c. 二氧化碳在自然界中只能转化为葡萄糖
d. 人类要停止使用化石燃料,积极开发利用风能、太阳能和潮汐能
Ⅰ. 自然之碳。
46 亿年前,在地心引力的作用下,碳以尘埃的形式慢慢进入地幔中。外来天体对地球“轰炸”形成岩浆,大量的二氧化碳和水蒸气从岩浆中释放,成为地球的早期大气层。当温度下降,水蒸气凝结成雨水汇入了海洋。
(1)写出雨水与二氧化碳的反应:______(用化学方程式表示)。
Ⅱ. 生命之碳。
38 亿年前,在海洋深处,碳元素与氧、氢、氮等元素结合在一起,演变成细胞。从此以碳元素为核心的碳基生命诞生。
(2)兴趣小组同学用如图所示实验装置测定人体呼出气体中二氧化碳的含量。实验步骤如下:

①连接装置后关闭止水夹,拉动注射器活塞,白鹤鹑蛋向下滑动。把注射器活塞推回顶端,白鹤鹑蛋向上滑动至原处。上述操作说明装置______(填“漏气”或“不漏气”)。②用同一白鹤鹑蛋反复多次实验发现,注射器内气体体积(mL)改变量与白鹤鹑蛋下降距离(cm)的比例均约为 4.8∶1。③用 625 mL 的烧瓶收集一瓶人体呼出的气体,恒压漏斗内加入足量氢氧化钠溶液(氢氧化钠溶液能吸收二氧化碳)。记录量气管内白鹤鹑蛋对应的刻度为 a cm。④打开恒压漏斗开关,同时打开磁力搅拌器使反应充分后,打开止水夹,白鹤鹑蛋向下滑动至刻度 b cm 处。⑤多次实验取平均值,测得 a= 20、b= 25.5。
(3)数据分析:人体呼出气体中二氧化碳的体积分数为______(计算结果保留 1 位小数)。
Ⅲ. 绿色之碳。
(4)目前科学家们正致力于攻克“碳中和”的难题。
方法一:将 CO_2转化成甲醇(CH_3OH):${CO2 + 3H2 \xlongequal{催化剂} CH3OH + H2O}。$
①甲醇在常温下是一种无色液体,易溶于水,沸点为 64.7 ℃,若需将甲醇从其水溶液中分离出来,可采用______(填“过滤”或“蒸馏”)的方法。
方法二:将 CO_2和 H_2O 转化为甲烷(CH_4)和氧气。催化剂的催化效率和甲烷的生成速率随温度的变化关系如图所示。

②300 ℃~400 ℃,甲烷生成速率加快的原因是______。
(5)关于绿色之碳,下列说法正确的是______(填字母)。
a. 二氧化碳会导致温室效应,对人类的生活有百害无一利
b. 人类过多的工业活动打破了碳循环的平衡
c. 二氧化碳在自然界中只能转化为葡萄糖
d. 人类要停止使用化石燃料,积极开发利用风能、太阳能和潮汐能
答案:
(1)$\mathrm{C}{\mathrm{O}}_{2}+{\mathrm{H}}_{2}\mathrm{O}\xlongequal{\;\;}{\mathrm{H}}_{2}\mathrm{C}{\mathrm{O}}_{3}$ (2)不漏气 (3)$4.2\%$ (4)①蒸馏 ②温度越高,反应速率越快 (5)bd 提示:
(1)空气中的二氧化碳能与水反应生成碳酸。
(2)连接装置后关闭止水夹,拉动注射器活塞,白鹤鹑蛋向下滑动。把注射器活塞推回顶端,白鹤鹑蛋向上滑动至原处,若装置漏气,则白鹤鹑蛋在重力作用下不会向上滑动。
(3)氢氧化钠溶液能吸收二氧化碳,根据题意,注射器内气体体积(mL)改变量与白鹤鹑蛋下降距离(cm)的比例均约为$4.8:1$,步骤③中收集到的呼出气体为$625\space \mathrm{m}\mathrm{L}$,量气管内白鹤鹑蛋对应的刻度为$a\space \mathrm{c}\mathrm{m}$,步骤④中二氧化碳被吸收后,白鹤鹑蛋向下滑动至刻度$b\space \mathrm{c}\mathrm{m}$处,代入测得数据,则人体呼出气体中二氧化碳的体积分数为$\frac{(25.5\space \mathrm{c}\mathrm{m}-20\space \mathrm{c}\mathrm{m})× \frac{4.8\space \mathrm{m}\mathrm{L}}{1\space \mathrm{c}\mathrm{m}}}{625\space \mathrm{m}\mathrm{L}}× 100\%=4.2\%$。
(4)①过滤可分离液体与不溶性固体,而甲醇在常温下是一种无色液体,易溶于水,沸点为$64.7\space {}^{\circ }\mathrm{C}$,而水的沸点为$100\space {}^{\circ }\mathrm{C}$,可利用沸点不同采用蒸馏法分离甲醇与水。②根据图像,$300\space {}^{\circ }\mathrm{C}\sim 400\space {}^{\circ }\mathrm{C}$,催化剂的催化作用逐渐消失,而温度在不断增大,所以甲烷生成速率加快的原因是温度越高,反应速率越快。
(1)空气中的二氧化碳能与水反应生成碳酸。
(2)连接装置后关闭止水夹,拉动注射器活塞,白鹤鹑蛋向下滑动。把注射器活塞推回顶端,白鹤鹑蛋向上滑动至原处,若装置漏气,则白鹤鹑蛋在重力作用下不会向上滑动。
(3)氢氧化钠溶液能吸收二氧化碳,根据题意,注射器内气体体积(mL)改变量与白鹤鹑蛋下降距离(cm)的比例均约为$4.8:1$,步骤③中收集到的呼出气体为$625\space \mathrm{m}\mathrm{L}$,量气管内白鹤鹑蛋对应的刻度为$a\space \mathrm{c}\mathrm{m}$,步骤④中二氧化碳被吸收后,白鹤鹑蛋向下滑动至刻度$b\space \mathrm{c}\mathrm{m}$处,代入测得数据,则人体呼出气体中二氧化碳的体积分数为$\frac{(25.5\space \mathrm{c}\mathrm{m}-20\space \mathrm{c}\mathrm{m})× \frac{4.8\space \mathrm{m}\mathrm{L}}{1\space \mathrm{c}\mathrm{m}}}{625\space \mathrm{m}\mathrm{L}}× 100\%=4.2\%$。
(4)①过滤可分离液体与不溶性固体,而甲醇在常温下是一种无色液体,易溶于水,沸点为$64.7\space {}^{\circ }\mathrm{C}$,而水的沸点为$100\space {}^{\circ }\mathrm{C}$,可利用沸点不同采用蒸馏法分离甲醇与水。②根据图像,$300\space {}^{\circ }\mathrm{C}\sim 400\space {}^{\circ }\mathrm{C}$,催化剂的催化作用逐渐消失,而温度在不断增大,所以甲烷生成速率加快的原因是温度越高,反应速率越快。
查看更多完整答案,请扫码查看


