第51页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
1. 次氯酸钠(NaClO)和二氧化氯($ClO_2$)都可用作消毒剂。下列有关说法正确的是( )
A.次氯酸钠属于氧化物
B.二氧化氯由1个氯原子和2个氧原子构成
C.次氯酸钠中钠元素、氯元素和氧元素的质量比为1∶1∶1
D.次氯酸钠中氯元素的质量分数比二氧化氯中氯元素的质量分数小
A.次氯酸钠属于氧化物
B.二氧化氯由1个氯原子和2个氧原子构成
C.次氯酸钠中钠元素、氯元素和氧元素的质量比为1∶1∶1
D.次氯酸钠中氯元素的质量分数比二氧化氯中氯元素的质量分数小
答案:
D 提示:氧化物是由两种元素组成,其中一种是氧元素的化合物,次氯酸钠由Na、Cl、O三种元素组成,不属于氧化物;二氧化氯(ClO₂)是由ClO₂分子构成的,一个ClO₂分子是由1个氯原子和2个氧原子构成的;次氯酸钠(NaClO)中钠元素、氯元素和氧元素的质量比为23:35.5:16=46:71:32;次氯酸钠中氯元素的质量分数为$\frac {35.5}{23+35.5+16}×100\% \approx 47.7\% $,二氧化氯中氯元素的质量分数为$\frac {35.5}{35.5+16×2}×100\% \approx 52.6\% $。
2. (2024·临沂)“临沂炒鸡”是临沂一张靓丽的美食名片,其特色是麻辣鲜香。“麻”的灵魂源于花椒中的花椒酰胺($C_{16}H_{25}NO$),下列有关花椒酰胺的说法错误的是( )
A.1个花椒酰胺分子由43个原子构成
B.花椒酰胺的相对分子质量为247
C.花椒酰胺中碳、氧元素的质量比为16∶1
D.247 g花椒酰胺中含氮元素的质量为14 g
A.1个花椒酰胺分子由43个原子构成
B.花椒酰胺的相对分子质量为247
C.花椒酰胺中碳、氧元素的质量比为16∶1
D.247 g花椒酰胺中含氮元素的质量为14 g
答案:
C 提示:花椒酰胺是由花椒酰胺分子构成的,一个花椒酰胺分子是由$16+25+1+1=43$个原子构成;花椒酰胺的相对分子质量为$12×16+1×25+14+16=247$;花椒酰胺中碳、氧元素的质量比为$(12×16):16=12:1$;247g花椒酰胺中含氮元素的质量为$247g×\frac {14}{247}×100\% =14g$。
3. 金银花作为常见的中药材,具有清热解毒、消炎退肿等功效,其有效成分之一是绿原酸($C_{16}H_{18}O_9$)。下列有关绿原酸的说法正确的是( )
A.绿原酸分子由碳、氢、氧三个元素组成
B.绿原酸中碳元素的质量分数最大
C.绿原酸的相对分子质量是354 g
D.绿原酸中碳、氢、氧元素的质量之比为16∶18∶9
A.绿原酸分子由碳、氢、氧三个元素组成
B.绿原酸中碳元素的质量分数最大
C.绿原酸的相对分子质量是354 g
D.绿原酸中碳、氢、氧元素的质量之比为16∶18∶9
答案:
B 提示:元素只讲种类,不讲个数,绿原酸由碳、氢、氧三种元素组成;绿原酸中碳、氢、氧三种元素的质量比为$(16×12):(18×1):(9×16)=32:3:24$,故碳元素的质量分数最大;相对分子质量的单位为"1",不是"g",故绿原酸的相对分子质量是354。
4. 完成下表并回答问题:
| 名称 | 氢气 | 甲烷 | 一氧化碳 | 氧气 | 二氧化碳 |
| 化学式 | |$ CH_4 $| | | |
| 相对分子质量 | | | | | |
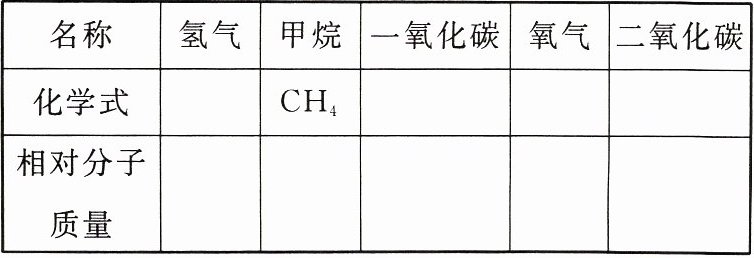
(1)上表中五种气体为初中化学中常见的气体,相对分子质量较大的单质是______。
(2)上述五种气体中按照分子中原子总数由多到少排列的化合物依次是______。
(3)一氧化碳与二氧化碳的化学性质______(填“相同”或“不同”),因为______。
| 名称 | 氢气 | 甲烷 | 一氧化碳 | 氧气 | 二氧化碳 |
| 化学式 | |$ CH_4 $| | | |
| 相对分子质量 | | | | | |

(1)上表中五种气体为初中化学中常见的气体,相对分子质量较大的单质是______。
(2)上述五种气体中按照分子中原子总数由多到少排列的化合物依次是______。
(3)一氧化碳与二氧化碳的化学性质______(填“相同”或“不同”),因为______。
答案:
名称氢气甲烷一氧化碳氧气二氧化碳化学式H₂ CH₄ CO O₂ CO₂相对分子质量2 16 28 32 44
(1)氧气(或O₂)
(2)甲烷(或CH₄)、二氧化碳(或CO₂)、一氧化碳(或CO)
(3)不同 分子构成不同 提示:
(2)化合物有甲烷、一氧化碳、二氧化碳,其中一个甲烷分子中含有5个原子,一个一氧化碳分子中含有2个原子,一个二氧化碳分子中含有3个原子,故按照分子中原子总数由多到少排列为甲烷、二氧化碳、一氧化碳。
(1)氧气(或O₂)
(2)甲烷(或CH₄)、二氧化碳(或CO₂)、一氧化碳(或CO)
(3)不同 分子构成不同 提示:
(2)化合物有甲烷、一氧化碳、二氧化碳,其中一个甲烷分子中含有5个原子,一个一氧化碳分子中含有2个原子,一个二氧化碳分子中含有3个原子,故按照分子中原子总数由多到少排列为甲烷、二氧化碳、一氧化碳。
5. 钙是人体必需的常量元素,人体缺钙时可适当使用补钙剂。碳酸钙($CaCO_3$)、乳酸钙($C_6H_{10}O_6Ca$)是补钙剂中常用的含钙物质。
(1)乳酸钙中氢原子和氧原子的个数比为______(填最简整数比,下同),碳元素和钙元素的质量比为______。
(2)碳酸钙中钙元素的质量分数为______;从元素质量分数的角度推断,用______(填物质名称)做补钙剂中的含钙物质更好。
(1)乳酸钙中氢原子和氧原子的个数比为______(填最简整数比,下同),碳元素和钙元素的质量比为______。
(2)碳酸钙中钙元素的质量分数为______;从元素质量分数的角度推断,用______(填物质名称)做补钙剂中的含钙物质更好。
答案:
(1)$5:3$ $9:5$
(2)40% 碳酸钙 提示:
(1)C₆H₁₀O₆Ca中氢原子和氧原子的个数比为$10:6=5:3$;碳元素和钙元素的质量比为$(12×6):40=9:5$。
(2)CaCO₃中钙元素的质量分数为$\frac {40}{40+12+16×3}×100\% =40\% $;C₆H₁₀O₆Ca中钙元素的质量分数为$\frac {40}{12×6+1×10+16×6+40}×100\% \approx 18.3\% $,碳酸钙中钙的含量更高,故用碳酸钙做补钙剂中的含钙物质更好。
(1)$5:3$ $9:5$
(2)40% 碳酸钙 提示:
(1)C₆H₁₀O₆Ca中氢原子和氧原子的个数比为$10:6=5:3$;碳元素和钙元素的质量比为$(12×6):40=9:5$。
(2)CaCO₃中钙元素的质量分数为$\frac {40}{40+12+16×3}×100\% =40\% $;C₆H₁₀O₆Ca中钙元素的质量分数为$\frac {40}{12×6+1×10+16×6+40}×100\% \approx 18.3\% $,碳酸钙中钙的含量更高,故用碳酸钙做补钙剂中的含钙物质更好。
6. (2024·宿迁泗阳期中)“端午节”是我国的传统节日,在该节日我国民间有一些习俗,如赛龙舟、吃粽子、挂艾草、饮雄黄等。已知雄黄酒中酒精的化学式为$CH_3CH_2OH$。请回答下列问题:
(1)一个酒精分子中共有______个原子。
(2)酒精的相对分子质量为______。
(3)92 g酒精中含氧元素的质量与多少克二氧化碳中所含氧元素的质量相等。(请写出计算过程)
(1)一个酒精分子中共有______个原子。
(2)酒精的相对分子质量为______。
(3)92 g酒精中含氧元素的质量与多少克二氧化碳中所含氧元素的质量相等。(请写出计算过程)
答案:
(1)9(或九)
(2)46
(3)解:设二氧化碳的质量为x。
$92g×\frac {16}{46}×100\% =x×\frac {16×2}{44}×100\% $
解得:$x=44g$。
答:92g酒精中含氧元素的质量与44g二氧化碳中所含氧元素的质量相等。
提示:
(1)根据酒精的化学式,可知一个酒精分子中有2个碳原子、6个氢原子和1个氧原子,共有$2+6+1=9$个原子。
(2)根据酒精的化学式,酒精的相对分子质量为$12×2+1×6+16=46$。
(1)9(或九)
(2)46
(3)解:设二氧化碳的质量为x。
$92g×\frac {16}{46}×100\% =x×\frac {16×2}{44}×100\% $
解得:$x=44g$。
答:92g酒精中含氧元素的质量与44g二氧化碳中所含氧元素的质量相等。
提示:
(1)根据酒精的化学式,可知一个酒精分子中有2个碳原子、6个氢原子和1个氧原子,共有$2+6+1=9$个原子。
(2)根据酒精的化学式,酒精的相对分子质量为$12×2+1×6+16=46$。
查看更多完整答案,请扫码查看


