第31页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
1.(2024·无锡江阴期中)物质是由微观粒子构成的。下列物质中由离子构成的是( )
A.硫酸铜
B.汞
C.氮气
D.二氧化碳
A.硫酸铜
B.汞
C.氮气
D.二氧化碳
答案:
A 提示:硫酸铜是由铜离子、硫酸根离子构成的;汞是金属,是由原子直接构成的;氮气、二氧化碳是由分子构成的。
2.(2024·南京模拟)下列粒子结构示意图中,表示阳离子的是( )

A.
B.
C.
D.

A.
B.
C.
D.
答案:
C 提示:A粒子核内质子数为2,电子数为2,质子数=核外电子数,为原子;B粒子核内质子数为9,电子数为10,质子数<核外电子数,为阴离子;C粒子核内质子数为11,电子数为10,质子数>核外电子数,为阳离子;D粒子核内质子数为17,电子数为18,质子数<核外电子数,为阴离子。
3. 右下图为某元素的阴离子的结构示意图。下列有关叙述正确的是( )
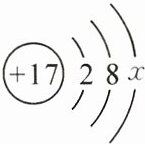
A.该阴离子的结构示意图中x= 7
B.该元素为硫,是一种非金属元素
C.该元素的原子在化学反应中容易失去电子
D.该阴离子中,核电荷数小于核外电子数

A.该阴离子的结构示意图中x= 7
B.该元素为硫,是一种非金属元素
C.该元素的原子在化学反应中容易失去电子
D.该阴离子中,核电荷数小于核外电子数
答案:
D 提示:根据题意可知,图为某元素的阴离子结构示意图,当x=7时,该粒子的质子数=核外电子数=17,是原子;当质子数<核外电子数时,为阴离子,则x=8。该粒子的核内质子数为17,为氯元素,是一种非金属元素;当x=7时为原子,在化学反应中易得到1个电子而形成阴离子;质子数=核电荷数,当质子数<核外电子数,为阴离子,则核电荷数小于核外电子数。
4.(2024·云南)如图所示为金属钠与氯气反应生成氯化钠的示意图,下列说法错误的是( )

A.每个氯离子带一个单位负电荷
B.钠原子在该反应中形成了阴离子
C.氯化钠是由钠离子和氯离子构成的
D.钠离子和氯离子的结构都相对稳定

A.每个氯离子带一个单位负电荷
B.钠原子在该反应中形成了阴离子
C.氯化钠是由钠离子和氯离子构成的
D.钠离子和氯离子的结构都相对稳定
答案:
B 提示:氯离子是氯原子得到1个电子后形成的,故每个氯离子带一个单位的负电荷;在该反应中,钠原子失去电子形成阳离子;氯化钠是由钠离子和氯离子构成的;钠离子和氯离子的最外层电子数均是8,均达到了相对稳定结构。
5. 下列微粒中,核电荷数少于核外电子数的是( )
$A. Na⁺ B. OH⁻ C. O_2 D. Mg$
$A. Na⁺ B. OH⁻ C. O_2 D. Mg$
答案:
B 提示:Na⁺带正电荷,为阳离子,核电荷数大于核外电子数;OH⁻带负电荷,为阴离子,核电荷数少于核外电子数;分子是由原子构成的,原子不显电性,分子也不显电性,核电荷数等于核外电子数。
6.(2024·西安月考)含氟物质有利于保护牙齿。已知一种氟原子的原子核中质子数为9,中子数为10,相对原子质量为19,下列说法正确的是( )
A.氟原子的核电荷数为9
B.一个氟原子的质量为19 g
C.氟原子的核外电子数为10
D.氟原子核外电子共带有10个单位的负电荷
A.氟原子的核电荷数为9
B.一个氟原子的质量为19 g
C.氟原子的核外电子数为10
D.氟原子核外电子共带有10个单位的负电荷
答案:
A 提示:在原子中,原子的质子数等于核电荷数,所以核电荷数为9;相对原子质量的单位是"1",省略不写;原子的核外电子数等于质子数,所以核外电子数为9;原子的核外电子数等于质子数,每一个电子带一个单位负电荷,故氟原子核外电子共带有9个单位负电荷。
7. 下列有关粒子的说法正确的是( )
A.分子可分,原子不可分
B.原子得到电子后带正电荷
C.分子、原子和离子都可以直接构成物质
D.原子的原子核都由质子和中子构成
A.分子可分,原子不可分
B.原子得到电子后带正电荷
C.分子、原子和离子都可以直接构成物质
D.原子的原子核都由质子和中子构成
答案:
C 提示:原子可分为原子核和电子,原子核分为质子和中子,但在化学变化中分子可分,原子不可再分;电子带负电,原子得到电子后带负电荷;原子核中不一定含有中子,如H-1原子的原子核内只有质子,没有中子。
8. 填写下表空白格。
|原子种类|核电荷数|质子数|核外电子数|中子数|相对原子质量|
|氢|1| | | |1|
|碳| | |6|6| |
|钠| |11| |12| |
|铝| | |13| |27|

认真分析表中的数字,进行归纳,总结出某些规律。例如:在原子中,核电荷数=质子数=核外电子数。还能总结出:
(1)______。
(2)______。
(3)______。
|原子种类|核电荷数|质子数|核外电子数|中子数|相对原子质量|
|氢|1| | | |1|
|碳| | |6|6| |
|钠| |11| |12| |
|铝| | |13| |27|

认真分析表中的数字,进行归纳,总结出某些规律。例如:在原子中,核电荷数=质子数=核外电子数。还能总结出:
(1)______。
(2)______。
(3)______。
答案:
氢:1 1 0 碳:6 6 12 钠:11 11 23 铝:13 13 14
(1)不是所有的原子都有中子
(2)质子数和中子数不一定相等
(3)相对原子质量(整数)=质子数+中子数
(1)不是所有的原子都有中子
(2)质子数和中子数不一定相等
(3)相对原子质量(整数)=质子数+中子数
9. 原子失去或得到电子后,一定不会引起改变的是( )
①原子核 ②化学性质 ③电子总数 ④微粒的电性 ⑤相对原子质量 ⑥中子数 ⑦质子数 ⑧物理性质
A.①⑤⑥⑦
B.①④⑤⑥
C.②⑤⑥⑦
D.①⑥⑦⑧
①原子核 ②化学性质 ③电子总数 ④微粒的电性 ⑤相对原子质量 ⑥中子数 ⑦质子数 ⑧物理性质
A.①⑤⑥⑦
B.①④⑤⑥
C.②⑤⑥⑦
D.①⑥⑦⑧
答案:
A 提示:原子核是由质子和中子构成的,原子得失电子以后,原子核肯定不变;中子数和质子数也不变;相对原子质量(整数)等于质子数和中子数之和,也不变。
查看更多完整答案,请扫码查看


