第15页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
10. 某校科学兴趣小组的同学利用稀盐酸、碳酸钠、$ Ba(OH)_{2} $ 溶液三种物质探究“复分解反应发生的条件”,做了以下实验。
(1)大家一致认为在试管①中还需要加入
(2)试管②中观察到的现象是
(3)通过三组实验,同学们得出复分解反应发生的条件是
(4)兴趣小组的同学将试管③反应后的物质过滤,对滤液中溶质的成分进一步探究。
【提出问题】滤液中溶质的成分是什么?
【猜想假设】
猜想一:$ NaOH $;
猜想二:$ Ba(OH)_{2} $、$ NaOH $;
猜想三:
【设计实验】
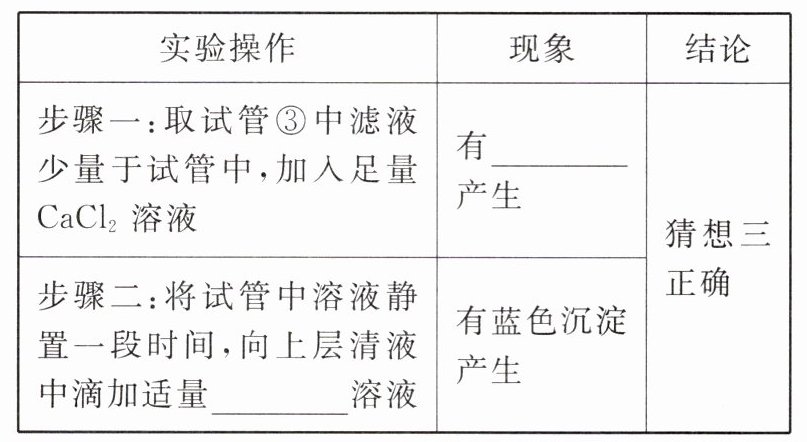
【反思拓展】通过探究实验,小组同学们发现 $ Ba(OH)_{2} $ 和 $ NaOH $ 的化学性质相似,你认为固体 $ Ba(OH)_{2} $ 的保存方法是

(1)大家一致认为在试管①中还需要加入
无色酚酞试液(或紫色石蕊试液)
才能证明发生了复分解反应。(2)试管②中观察到的现象是
固体溶解,有气泡产生
,试管③中反应的化学方程式为$Ba(OH)_{2}+Na_{2}CO_{3}=BaCO_{3}\downarrow +2NaOH$
。(3)通过三组实验,同学们得出复分解反应发生的条件是
要有沉淀或有气体或有水生成
。(4)兴趣小组的同学将试管③反应后的物质过滤,对滤液中溶质的成分进一步探究。
【提出问题】滤液中溶质的成分是什么?
【猜想假设】
猜想一:$ NaOH $;
猜想二:$ Ba(OH)_{2} $、$ NaOH $;
猜想三:
NaOH、$Na_{2}CO_{3}$
。【设计实验】

【反思拓展】通过探究实验,小组同学们发现 $ Ba(OH)_{2} $ 和 $ NaOH $ 的化学性质相似,你认为固体 $ Ba(OH)_{2} $ 的保存方法是
密封干燥保存
。
答案:
(1)无色酚酞试液(或紫色石蕊试液)
(2)固体溶解,有气泡产生$Ba(OH)_{2}+Na_{2}CO_{3}=BaCO_{3}\downarrow +2NaOH$
(3)要有沉淀或有气体或有水生成
(4)【猜想假设】NaOH、$Na_{2}CO_{3}$【设计实验】白色沉淀$CuSO_{4}$[或$CuCl_{2}$、$Cu(NO_{3})_{2}$等]【反思拓展】密封干燥保存
(1)无色酚酞试液(或紫色石蕊试液)
(2)固体溶解,有气泡产生$Ba(OH)_{2}+Na_{2}CO_{3}=BaCO_{3}\downarrow +2NaOH$
(3)要有沉淀或有气体或有水生成
(4)【猜想假设】NaOH、$Na_{2}CO_{3}$【设计实验】白色沉淀$CuSO_{4}$[或$CuCl_{2}$、$Cu(NO_{3})_{2}$等]【反思拓展】密封干燥保存
11. 我国制碱工业的先驱——侯德榜成功地摸索和改进了制碱方法。表中为侯氏制碱法中部分物质的溶解度。

(1)由表可知,在 $ 10 \sim 40^{\circ}C $ 之间溶解度随温度变化最小的物质是
(2)$ 40^{\circ}C $ 时,将等质量的三种表中物质的饱和溶液降温至 $ 20^{\circ}C $,所得溶液中溶质的质量分数由大到小的顺序是
(3)侯氏制碱法制得的碱为纯碱,则纯碱的化学式为
(4)制碱原理为向饱和的 $ NaCl $ 溶液中通入足量 $ NH_{3} $ 和 $ CO_{2} $ 生成 $ NaHCO_{3} $ 晶体和 $ NH_{4}Cl $, $ NaHCO_{3} $ 加热分解即制得纯碱。
①生成 $ NaHCO_{3} $ 的化学方程式为
②结合表格分析,析出 $ NaHCO_{3} $ 晶体的原因可能有
A. 溶剂质量减少
B. 同温下 $ NaHCO_{3} $ 溶解度小于 $ NaCl $
C. 生成的 $ NaHCO_{3} $ 质量大于消耗的 $ NaCl $ 质量

(1)由表可知,在 $ 10 \sim 40^{\circ}C $ 之间溶解度随温度变化最小的物质是
氯化钠
(填名称)。(2)$ 40^{\circ}C $ 时,将等质量的三种表中物质的饱和溶液降温至 $ 20^{\circ}C $,所得溶液中溶质的质量分数由大到小的顺序是
$NaCl>Na_{2}CO_{3}>NaHCO_{3}$
(用化学式表示)。(3)侯氏制碱法制得的碱为纯碱,则纯碱的化学式为
$Na_{2}CO_{3}$
。(4)制碱原理为向饱和的 $ NaCl $ 溶液中通入足量 $ NH_{3} $ 和 $ CO_{2} $ 生成 $ NaHCO_{3} $ 晶体和 $ NH_{4}Cl $, $ NaHCO_{3} $ 加热分解即制得纯碱。
①生成 $ NaHCO_{3} $ 的化学方程式为
$NaCl+NH_{3}+CO_{2}+H_{2}O=NaHCO_{3}\downarrow +NH_{4}Cl$
。②结合表格分析,析出 $ NaHCO_{3} $ 晶体的原因可能有
AB
(填字母)。A. 溶剂质量减少
B. 同温下 $ NaHCO_{3} $ 溶解度小于 $ NaCl $
C. 生成的 $ NaHCO_{3} $ 质量大于消耗的 $ NaCl $ 质量
答案:
(1)氯化钠
(2)$NaCl>Na_{2}CO_{3}>NaHCO_{3}$
(3)$Na_{2}CO_{3}$
(4)①$NaCl+NH_{3}+CO_{2}+H_{2}O=NaHCO_{3}\downarrow +NH_{4}Cl$②AB
(1)氯化钠
(2)$NaCl>Na_{2}CO_{3}>NaHCO_{3}$
(3)$Na_{2}CO_{3}$
(4)①$NaCl+NH_{3}+CO_{2}+H_{2}O=NaHCO_{3}\downarrow +NH_{4}Cl$②AB
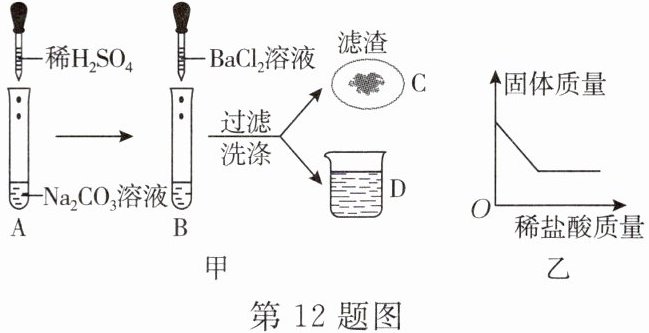
12. 科学兴趣小组的同学们在学习了盐的化学性质后,进行了如图甲所示的实验,请回答下列问题。
(1)B 试管中观察到的现象是
(2)同学们将 B 试管中的固液混合物过滤,得到滤渣 C 和滤液 D,同学们想要探究滤渣 C 和滤液 D 中溶质的成分。小丽同学取滤渣少许于试管中,向其中加入稀盐酸,固体质量变化情况如图乙所示,则推测出滤渣的成分为
(3)【提出问题】滤液 D 中含有哪些离子?
【猜想与假设】甲同学猜想:$ Na^{+} $、$ Cl^{-} $、$ CO_{3}^{2-} $;
乙同学猜想:$ Na^{+} $、$ Cl^{-} $、$ CO_{3}^{2-} $、$ SO_{4}^{2-} $;
你的猜想是:
(4)【实验验证】小明同学的验证方案是:先向滤液 D 中加入足量的硝酸溶液,若溶液中出现产生气泡的现象,而后再加入
(1)B 试管中观察到的现象是
产生白色沉淀
。(2)同学们将 B 试管中的固液混合物过滤,得到滤渣 C 和滤液 D,同学们想要探究滤渣 C 和滤液 D 中溶质的成分。小丽同学取滤渣少许于试管中,向其中加入稀盐酸,固体质量变化情况如图乙所示,则推测出滤渣的成分为
$BaCO_{3}$、$BaSO_{4}$
(填化学式)。(3)【提出问题】滤液 D 中含有哪些离子?
【猜想与假设】甲同学猜想:$ Na^{+} $、$ Cl^{-} $、$ CO_{3}^{2-} $;
乙同学猜想:$ Na^{+} $、$ Cl^{-} $、$ CO_{3}^{2-} $、$ SO_{4}^{2-} $;
你的猜想是:
$Na^{+}$、$Cl^{-}$(或$Na^{+}$、$Cl^{-}$、$Ba^{2+}$)
(写出一种即可)。(4)【实验验证】小明同学的验证方案是:先向滤液 D 中加入足量的硝酸溶液,若溶液中出现产生气泡的现象,而后再加入
硝酸钡
溶液,可以得出乙同学猜想的结论是正确的。
答案:
(1)产生白色沉淀
(2)$BaCO_{3}$、$BaSO_{4}$
(3)$Na^{+}$、$Cl^{-}$(或$Na^{+}$、$Cl^{-}$、$Ba^{2+}$)
(4)硝酸钡
(1)产生白色沉淀
(2)$BaCO_{3}$、$BaSO_{4}$
(3)$Na^{+}$、$Cl^{-}$(或$Na^{+}$、$Cl^{-}$、$Ba^{2+}$)
(4)硝酸钡
查看更多完整答案,请扫码查看


