2025年书立方跟踪测试卷九年级化学下册人教版
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2025年书立方跟踪测试卷九年级化学下册人教版 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
第7页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
1. 甲、乙、丙三种金属,分别投入稀盐酸中,只有甲能产生气体;将乙、丙分别放入硝酸银溶液中,一段时间后,丙的表面有银析出,乙没有变化。则甲、乙、丙三种金属的活动性顺序为( )
A. 甲>乙>丙 B. 甲>丙>乙 C. 乙>甲>丙 D. 丙>乙>甲
A. 甲>乙>丙 B. 甲>丙>乙 C. 乙>甲>丙 D. 丙>乙>甲
答案:
B [解析]由题意可知,甲、乙、丙三种金属,分别投入稀盐酸中,只有甲能产生气体,可推出甲的活动性强于乙、丙;将乙、丙分别放入硝酸银溶液中,一段时间后,丙的表面有银析出,乙没有变化说明丙的活动性强于乙。由此可得出甲、乙、丙三种的金属活动性是:甲>丙>乙。
故选:B。
故选:B。
2. 铬(Cr)及其化合物在作为催化剂、金属防腐剂等方面具有重要应用,金属活动性介于锌和铅之间。下列有关推理不正确的是( )
A. 铬能与氧气反应
B. 金属铬单质能与稀硫酸反应
C. 金属铬不能置换出硫酸铜溶液中的铜
D. 可用洁净的铅片、CrSO₄溶液和洁净的锌片验证三种金属的活动性强弱
A. 铬能与氧气反应
B. 金属铬单质能与稀硫酸反应
C. 金属铬不能置换出硫酸铜溶液中的铜
D. 可用洁净的铅片、CrSO₄溶液和洁净的锌片验证三种金属的活动性强弱
答案:
C [解析]A.铬的金属活动性介于锌和铅之间,则铬能与氧气反应,故A选项说法正确。
B.在金属活动性顺序中,位于氢前面的金属能置换出酸中的氢,铬的金属活动性介于锌和铅之间,则铬的位置排在氢之前,能与稀硫酸反应,故B选项说法正确。
C.铬的金属活动性介于锌和铅之间,铬的位置排在铜的前面,能置换出硫酸铜溶液中的铜,故C选项说法错误。
D.铅片不能与CrSO₄溶液反应,说明了金属活动性铬>铅;锌片能与CrSO₄溶液反应,说明了金属活动性锌>铬,可得出金属活动性锌>铬>铅,故D选项说法正确。
故选:C。
B.在金属活动性顺序中,位于氢前面的金属能置换出酸中的氢,铬的金属活动性介于锌和铅之间,则铬的位置排在氢之前,能与稀硫酸反应,故B选项说法正确。
C.铬的金属活动性介于锌和铅之间,铬的位置排在铜的前面,能置换出硫酸铜溶液中的铜,故C选项说法错误。
D.铅片不能与CrSO₄溶液反应,说明了金属活动性铬>铅;锌片能与CrSO₄溶液反应,说明了金属活动性锌>铬,可得出金属活动性锌>铬>铅,故D选项说法正确。
故选:C。
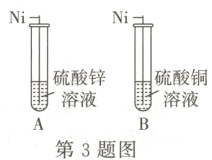
3. 金属镍在制造钱币、不锈钢、催化剂等方面有着广泛的应用。为探究镍、锌、铜的金属活动性顺序,小明做了如图所示的实验,发现A试管中镍丝表面无现象,B试管中镍丝表面出现红色物质,则三种金属活动性由强到弱的顺序是( )
A. Ni、Zn、Cu
B. Zn、Cu、Ni
C. Zn、Ni、Cu
D. Cu、Ni、Zn
A. Ni、Zn、Cu
B. Zn、Cu、Ni
C. Zn、Ni、Cu
D. Cu、Ni、Zn

答案:
C [解析]在金属活动性顺序中,活动性强的金属能将活动性弱的金属从它的盐溶液中置换出来;如图所示的实验中,将镍放入硫酸锌溶液中,发现A试管中镍丝表面无现象,说明镍的金属活动性比锌弱,将镍放入硫酸铜溶液中,发现B试管中镍丝表面出现红色物质,说明镍的金属活动性比铜强,所以三种金属活动性由强到弱的顺序是:Zn、Ni、Cu。故选:C。
4. 跨学科《宋会要辑稿》记载:“浸铜之法,先取生铁打成薄片,……浸渍数日,铁片为胆水(硫酸铜溶液)所薄,上生赤煤,取出刮洗……入炉烹炼,……方成铜。”下列理解错误的是( )
A. “打成薄片”增大了反应的接触面积
B. “铁片为胆水所薄”发生了置换反应
C. “上生赤煤”指铁片上生成了红色的煤
D. “浸铜之法”可知铁的金属活动性比铜强
A. “打成薄片”增大了反应的接触面积
B. “铁片为胆水所薄”发生了置换反应
C. “上生赤煤”指铁片上生成了红色的煤
D. “浸铜之法”可知铁的金属活动性比铜强
答案:
C [解析]A.“打成薄片”增大了反应的接触面积,该选项正确。
B.“铁片为胆水所薄”发生了置换反应,即铁和硫酸铜反应生成硫酸亚铁和铜,该选项正确。
C.“上生赤煤”指铁片上生成了红色的铜,该选项不正确。
D.“浸铜之法”可知,铁能和铜盐溶液反应,说明铁的金属活动性比铜强,该选项正确。
故选:C。
B.“铁片为胆水所薄”发生了置换反应,即铁和硫酸铜反应生成硫酸亚铁和铜,该选项正确。
C.“上生赤煤”指铁片上生成了红色的铜,该选项不正确。
D.“浸铜之法”可知,铁能和铜盐溶液反应,说明铁的金属活动性比铜强,该选项正确。
故选:C。
5. 将一定量的锌粉加入盛有AgNO₃溶液的烧杯中,不断搅拌,充分反应后过滤,得到滤渣和滤液,向滤渣中加入足量稀盐酸,搅拌,滤渣部分溶解,有气泡产生,下列说法错误的是( )
A. 滤渣中有Zn和Ag B. 金属活动性:Zn>Ag
C. 滤液中含Zn(NO₃)₂和AgNO₃ D. 上述过程中只发生置换反应
A. 滤渣中有Zn和Ag B. 金属活动性:Zn>Ag
C. 滤液中含Zn(NO₃)₂和AgNO₃ D. 上述过程中只发生置换反应
答案:
C [解析]A.将一定量的锌粉加入盛有AgNO₃溶液的烧杯中,不断搅拌,锌与硝酸银反应生成硝酸锌和银,不断搅拌,充分反应后过滤,得到滤渣和滤液,向滤渣中加入足量稀盐酸,搅拌,滤渣部分溶解,有气泡产生,由于银不与稀盐酸反应,说明滤渣中含有锌,说明加入的锌是过量的,则滤渣中有Zn和Ag,故A选项说法正确。
B.锌能与硝酸银溶液反应,说明金属活动性:Zn>Ag,故B选项说法正确。
C.由于锌是过量的,则滤液中含Zn(NO₃)₂,不可能含有AgNO₃,故C选项说法错误。
D.上述过程中只发生了锌和硝酸银反应生成硝酸锌和银,锌和稀盐酸反应生成氯化锌和氢气,均属于置换反应,故D选项说法正确。
故选:C。
B.锌能与硝酸银溶液反应,说明金属活动性:Zn>Ag,故B选项说法正确。
C.由于锌是过量的,则滤液中含Zn(NO₃)₂,不可能含有AgNO₃,故C选项说法错误。
D.上述过程中只发生了锌和硝酸银反应生成硝酸锌和银,锌和稀盐酸反应生成氯化锌和氢气,均属于置换反应,故D选项说法正确。
故选:C。
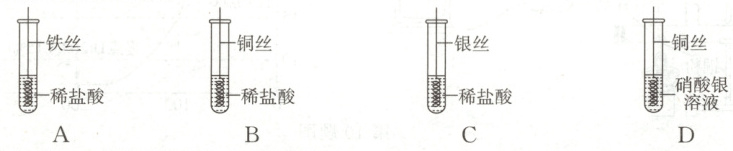
6. 某化学兴趣小组为了验证铁、铜、银三种金属的活动性强弱,设计了下面4个实验,其中不需要进行也能得出结果的实验是( )

答案:
C [解析]A实验,铁和稀盐酸反应产生气泡,能证明活动性:Fe>H;B实验,无明显现象,能证明H>Cu;C实验,无明显现象,能证明活动性:H>Ag,D实验,铜丝表面覆盖一层银白色物质,能证明活动性:Cu>Ag,由此可知,A、B、D组合即可证明三种金属活动性强弱,C不必进行。故选:C。
7. 下列物质能由酸和金属置换反应生成的是( )
A. AgCl B. CuCl₂ C. Fe₂(SO₄)₃ D. MgSO₄
A. AgCl B. CuCl₂ C. Fe₂(SO₄)₃ D. MgSO₄
答案:
D [解析]A.银的金属活动性在氢后,所以不能与稀盐酸发生置换反应生成氢气,故A错误;
B.铜的金属活动性在氢后,所以不能与稀盐酸反应生成氯化铜,故B错误;
C.铁的金属活动性在氢前,所以能与稀硫酸反应生成氢气,但生成氢气的同时会生成硫酸亚铁,而非硫酸铁,故C错误;
D.镁的金属活动性在氢前,所以能与稀硫酸发生置换反应生成氢气和MgSO₄,故D正确。
故选:D。
B.铜的金属活动性在氢后,所以不能与稀盐酸反应生成氯化铜,故B错误;
C.铁的金属活动性在氢前,所以能与稀硫酸反应生成氢气,但生成氢气的同时会生成硫酸亚铁,而非硫酸铁,故C错误;
D.镁的金属活动性在氢前,所以能与稀硫酸发生置换反应生成氢气和MgSO₄,故D正确。
故选:D。
8. 中国应用的湿法炼铜技术,是对世界化学史的一个贡献。现将一根光亮的铁钉放入硫酸铜溶液里充分反应。下列说法的组合中正确的是( )
①反应能证明两种金属的活动性 ②反应后溶液的质量增加
③反应生成的溶质为硫酸铁 ④反应后固体表面附着一层红色物质
A. ①④ B. ②③ C. ①②④ D. ②③④
①反应能证明两种金属的活动性 ②反应后溶液的质量增加
③反应生成的溶质为硫酸铁 ④反应后固体表面附着一层红色物质
A. ①④ B. ②③ C. ①②④ D. ②③④
答案:
A [解析]将一根光亮的铁钉放入硫酸铜溶液里充分反应,铁和硫酸铜反应生成硫酸亚铁和铜;①铁能置换出铜,说明铁的活动性强于铜,该反应能证明两种金属的活动性,故①选项符合题意;②铁和硫酸铜反应的化学方程式及其质量关系如下:
Fe+CuSO₄ = FeSO₄+Cu
56 160 152 64
则反应后溶液的质量减少,故②选项不符合题意;③反应生成的溶质为硫酸亚铁,故③选项不符合题意;
④该反应有铜生成,反应后固体表面附着一层红色物质,故选④项符合题意;
综上所述,正确的是:①④。
故选:A。
Fe+CuSO₄ = FeSO₄+Cu
56 160 152 64
则反应后溶液的质量减少,故②选项不符合题意;③反应生成的溶质为硫酸亚铁,故③选项不符合题意;
④该反应有铜生成,反应后固体表面附着一层红色物质,故选④项符合题意;
综上所述,正确的是:①④。
故选:A。
查看更多完整答案,请扫码查看


