2025年新课程学习与测评单元双测九年级化学全一册鲁教版
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2025年新课程学习与测评单元双测九年级化学全一册鲁教版 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
第77页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
- 第107页
- 第108页
- 第109页
- 第110页
- 第111页
- 第112页
- 第113页
- 第114页
- 第115页
- 第116页
23. 物质的酸碱性与我们的生活密切相关。
(1)物质具有酸性是因为其能电离出
(2)溶液酸碱性的强弱可用 pH 来表示。为了更有效地清除头发和头皮上的油脂及污垢,洗发水通常被设计为弱碱性,pH
(3)我国古代劳动人民在长期的实践中,积累了丰富的关于物质变化的知识与经验。春秋战国时期,齐国的工艺官书《考工记》记载了一种名为“涑帛”的方法。这种方法巧妙地利用了“灰(即草木灰,主要成分为碳酸钾)”与“蜃(主要成分为氧化钙)”混合后加水所得的溶液,来洗涤丝帛。“蜃”与水反应的化学方程式为
(1)物质具有酸性是因为其能电离出
H⁺
(写离子符号),可以使紫色石蕊试液变红
色。(2)溶液酸碱性的强弱可用 pH 来表示。为了更有效地清除头发和头皮上的油脂及污垢,洗发水通常被设计为弱碱性,pH
>
(填“>”“<”或“=”,下同)7。然而,自然状态下,头皮表面呈弱酸性,这有利于头发的健康生长。因此,在使用洗发水之后,建议再使用护发素,以帮助头皮恢复并维持弱酸性环境。由此推测,护发素的 pH<
7。(3)我国古代劳动人民在长期的实践中,积累了丰富的关于物质变化的知识与经验。春秋战国时期,齐国的工艺官书《考工记》记载了一种名为“涑帛”的方法。这种方法巧妙地利用了“灰(即草木灰,主要成分为碳酸钾)”与“蜃(主要成分为氧化钙)”混合后加水所得的溶液,来洗涤丝帛。“蜃”与水反应的化学方程式为
CaO+H₂O=Ca(OH)₂
。这种溶液能洗涤丝帛,主要是因为其中一定含有一种碱:KOH
(写化学式)。
答案:
23.
(1)H⁺ 红
(2)> <
(3)CaO+H₂O=Ca(OH)₂ KOH
(1)H⁺ 红
(2)> <
(3)CaO+H₂O=Ca(OH)₂ KOH
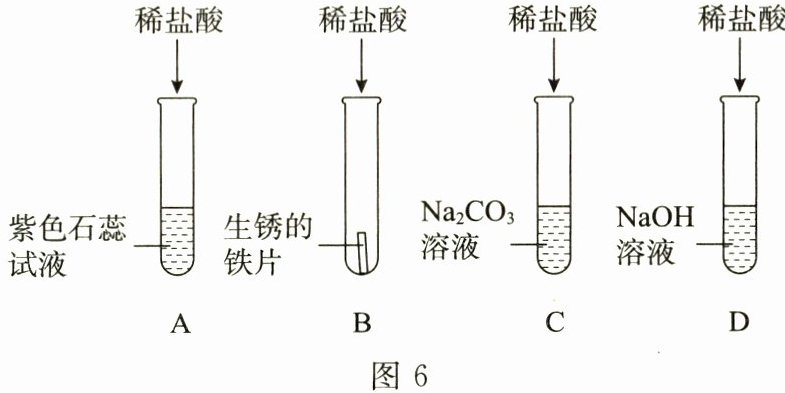
24. 某化学兴趣小组的同学为探究盐酸的化学性质,进行了图 6 所示的实验(所加稀盐酸均过量)。
(1)试管 B 中稀盐酸先与铁锈反应,铁锈的主要成分是
(2)试管 C 中发生反应的化学方程式为
(3)向试管 D 中加稀盐酸至过量,始终没有观察到明显现象。请你设计实验方案证明试管 D 中的 NaOH 与 HCl 发生了反应:
(1)试管 B 中稀盐酸先与铁锈反应,铁锈的主要成分是
Fe₂O₃
(写化学式);一段时间后观察到有气泡产生,产生气泡的反应的化学方程式为Fe+2HCl=FeCl₂+H₂↑
。(2)试管 C 中发生反应的化学方程式为
Na₂CO₃+2HCl=2NaCl+H₂O+CO₂↑
,实验现象为产生大量气泡
。(3)向试管 D 中加稀盐酸至过量,始终没有观察到明显现象。请你设计实验方案证明试管 D 中的 NaOH 与 HCl 发生了反应:
向NaOH溶液中滴入几滴酚酞试液,再逐滴加入稀盐酸,溶液由红色变为无色
(写出操作及现象)。
答案:
24.
(1)Fe₂O₃ Fe+2HCl=FeCl₂+H₂↑
(2)Na₂CO₃+2HCl=2NaCl+H₂O+CO₂↑ 产生大量气泡
(3)向NaOH溶液中滴入几滴酚酞试液,再逐滴加入稀盐酸,溶液由红色变为无色
(1)Fe₂O₃ Fe+2HCl=FeCl₂+H₂↑
(2)Na₂CO₃+2HCl=2NaCl+H₂O+CO₂↑ 产生大量气泡
(3)向NaOH溶液中滴入几滴酚酞试液,再逐滴加入稀盐酸,溶液由红色变为无色
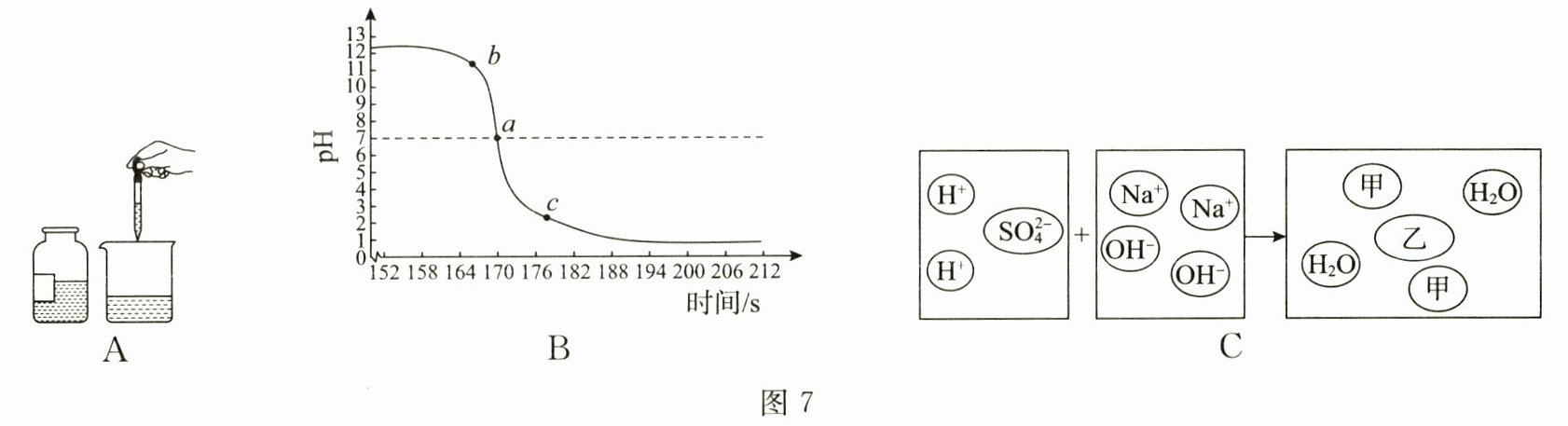
25. 某化学兴趣小组的同学在学习了硫酸与氢氧化钠的反应后,分别结合自己在实验室里所做的实验,从不同角度对该反应进行了描述。图 7A 是实际操作图,图 7B 是反应过程中溶液的酸碱度变化图,图 7C 是微观粒子结合过程示意图。
结合图示,回答问题。
(1)依据图 7A 和图 7B 可知,该实验是将
(2)图 7B 中,表示硫酸与氢氧化钠恰好完全反应的是
(3)向图 7B 中 c 点对应的溶液内滴加氯化钡溶液,发生反应的化学方程式为
(4)写出图 7C 中方框内微观粒子乙的符号:
结合图示,回答问题。
(1)依据图 7A 和图 7B 可知,该实验是将
硫酸(或H₂SO₄)
滴加到另一种溶液中。(2)图 7B 中,表示硫酸与氢氧化钠恰好完全反应的是
a
(填“a”“b”或“c”)点,b 点对应溶液的溶质是NaOH、Na₂SO₄
。(3)向图 7B 中 c 点对应的溶液内滴加氯化钡溶液,发生反应的化学方程式为
H₂SO₄+BaCl₂=BaSO₄↓+2HCl
(写出一个即可)。(4)写出图 7C 中方框内微观粒子乙的符号:
SO₄²⁻
。
答案:
25.
(1)硫酸(或H₂SO₄)
(2)a NaOH、Na₂SO₄
(3)H₂SO₄+BaCl₂=BaSO₄↓+2HCl
(4)SO₄²⁻
(1)硫酸(或H₂SO₄)
(2)a NaOH、Na₂SO₄
(3)H₂SO₄+BaCl₂=BaSO₄↓+2HCl
(4)SO₄²⁻
查看更多完整答案,请扫码查看


