第27页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
- 第107页
- 第108页
- 第109页
- 第110页
- 第111页
- 第112页
任务一 探究过氧化氢分解制取氧气中二氧化锰的作用
|原理探究|
[提出问题]在使用过氧化氢溶液制取氧气时,通常加入少量二氧化锰,这是为什么呢?
[作出猜想]猜想一:二氧化锰与过氧化氢溶液发生反应。
猜想二:二氧化锰可以促进过氧化氢的分解。
[方案设计]设计如下三组实验进行对照分析。
[进行实验]
|实验操作|实验装置|实验现象|
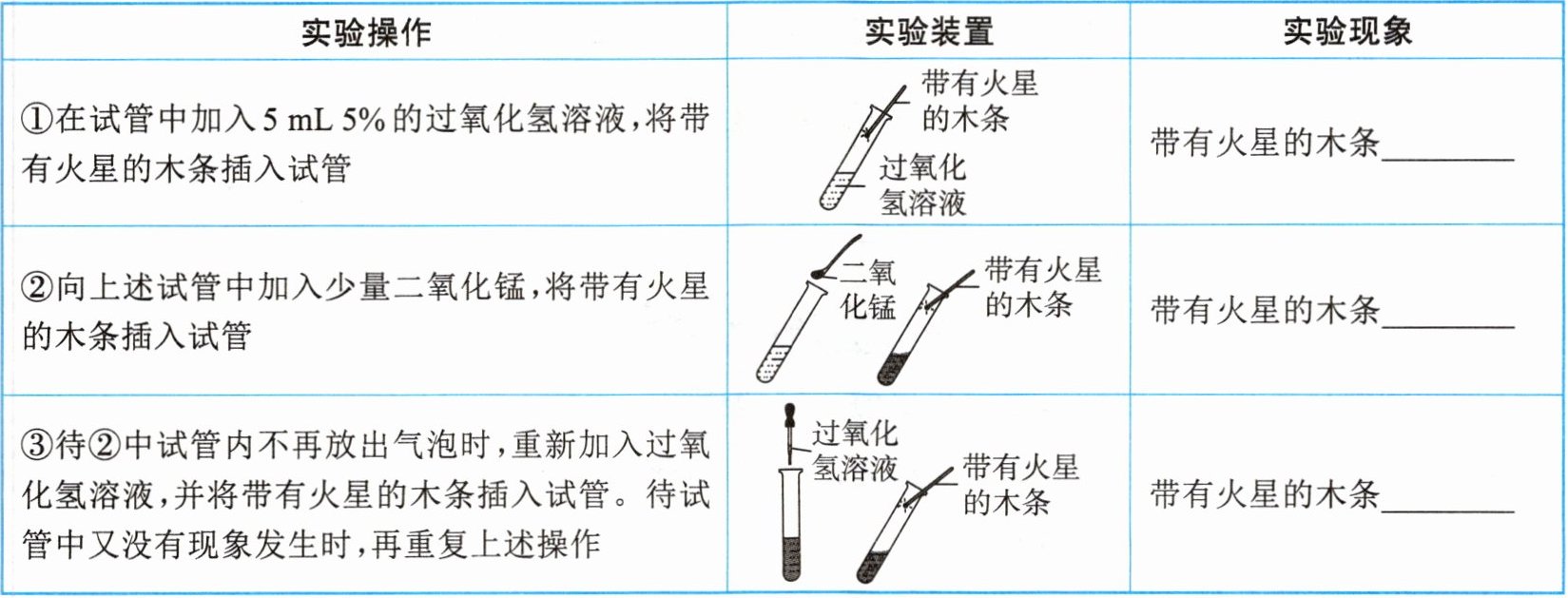

|①在试管中加入 5 mL 5%的过氧化氢溶液,将带有火星的木条插入试管||带有火星的木条______|
|②向上述试管中加入少量二氧化锰,将带有火星的木条插入试管||带有火星的木条______|
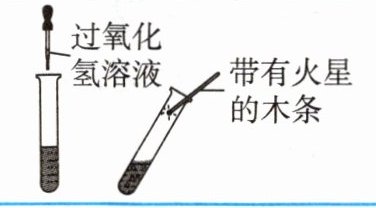
|③待②中试管内不再放出气泡时,重新加入过氧化氢溶液,并将带有火星的木条插入试管。待试管中又没有现象发生时,再重复上述操作||带有火星的木条______|
若将反应后的二氧化锰洗净、干燥、称重,与其反应前的质量比较,可发现其质量没有改变。将二氧化锰再加到过氧化氢溶液中,还可以加速过氧化氢分解。
[实验分析]由实验操作①和②的现象分析可知:常温下过氧化氢分解缓慢,二氧化锰可以加速过氧化氢的分解,放出的氧气使木条复燃。由实验操作③的现象分析可知:氧气是过氧化氢分解产生的,二氧化锰只起促进过氧化氢分解的作用。
[实验结论]通过对三组实验的对比分析可知,过氧化氢在二氧化锰作用下迅速分解,放出氧气,且二氧化锰在过氧化氢分解过程中______和______不发生变化。
[思路与方法]实验探究的一般思路:明确探究目的→设计实验方案→实施实验→获取证据→分析推理→形成结论。
任务二 催化剂及分解反应
|知识形成|
1. 催化剂:在化学反应里能改变其他物质的______,而本身的______和______在反应前后都没有发生变化的物质叫作催化剂。
[点拨]①催化剂的特点:一变两不变。
一变:改变化学反应速率(改变包括增大和减小)。两不变:质量不变,化学性质不变。
②关于催化剂要牢记:催化剂可增大或减小化学反应速率,但不能增大或减小生成物的质量。
2. 分解反应。
(1)定义:由一种反应物生成______其他物质的反应,叫作分解反应。
(2)分解反应的特征:一变多。
(3)分解反应的表达式:X→A+B+……
|原理探究|
[提出问题]在使用过氧化氢溶液制取氧气时,通常加入少量二氧化锰,这是为什么呢?
[作出猜想]猜想一:二氧化锰与过氧化氢溶液发生反应。
猜想二:二氧化锰可以促进过氧化氢的分解。
[方案设计]设计如下三组实验进行对照分析。
[进行实验]
|实验操作|实验装置|实验现象|



|①在试管中加入 5 mL 5%的过氧化氢溶液,将带有火星的木条插入试管||带有火星的木条______|
|②向上述试管中加入少量二氧化锰,将带有火星的木条插入试管||带有火星的木条______|
|③待②中试管内不再放出气泡时,重新加入过氧化氢溶液,并将带有火星的木条插入试管。待试管中又没有现象发生时,再重复上述操作||带有火星的木条______|
若将反应后的二氧化锰洗净、干燥、称重,与其反应前的质量比较,可发现其质量没有改变。将二氧化锰再加到过氧化氢溶液中,还可以加速过氧化氢分解。
[实验分析]由实验操作①和②的现象分析可知:常温下过氧化氢分解缓慢,二氧化锰可以加速过氧化氢的分解,放出的氧气使木条复燃。由实验操作③的现象分析可知:氧气是过氧化氢分解产生的,二氧化锰只起促进过氧化氢分解的作用。
[实验结论]通过对三组实验的对比分析可知,过氧化氢在二氧化锰作用下迅速分解,放出氧气,且二氧化锰在过氧化氢分解过程中______和______不发生变化。
[思路与方法]实验探究的一般思路:明确探究目的→设计实验方案→实施实验→获取证据→分析推理→形成结论。
任务二 催化剂及分解反应
|知识形成|
1. 催化剂:在化学反应里能改变其他物质的______,而本身的______和______在反应前后都没有发生变化的物质叫作催化剂。
[点拨]①催化剂的特点:一变两不变。
一变:改变化学反应速率(改变包括增大和减小)。两不变:质量不变,化学性质不变。
②关于催化剂要牢记:催化剂可增大或减小化学反应速率,但不能增大或减小生成物的质量。
2. 分解反应。
(1)定义:由一种反应物生成______其他物质的反应,叫作分解反应。
(2)分解反应的特征:一变多。
(3)分解反应的表达式:X→A+B+……
答案:
[进行实验]不复燃 复燃 复燃 [实验结论]质量 化学性质 任务二 1.化学反应速率 质量 化学性质 2.
(1)两种或两种以上
(1)两种或两种以上
查看更多完整答案,请扫码查看


