1. 如图为氢氧化钙的溶解度曲线,下列说法不正确的是 ( )

A. 氢氧化钙的溶解度随温度的升高而减小
B. 30℃时,100 g水中最多溶解0.15 g氢氧化钙
C. 30℃恰好饱和的石灰水升温到50℃,溶质的质量分数不变
D. 70℃时,饱和石灰水中溶质和溶剂的质量比为1:1 000

A. 氢氧化钙的溶解度随温度的升高而减小
B. 30℃时,100 g水中最多溶解0.15 g氢氧化钙
C. 30℃恰好饱和的石灰水升温到50℃,溶质的质量分数不变
D. 70℃时,饱和石灰水中溶质和溶剂的质量比为1:1 000
答案:
C [解析]A.由溶解度曲线可知:氢氧化钙的溶解度随温度的升高而减少,正确但不符合题意;
B.30℃时,100g水中最多溶解0.15g氢氧化钙,正确但不符合题意;C.30℃恰好饱和的石灰水升温到50℃,溶质的质量分数不变错误,因为升温后有固体析出,符合题意;D.70℃时,饱和石灰水中溶质和溶剂的质量比=0.10g:100g=1:1000,正确但不符合题意。故选C。
B.30℃时,100g水中最多溶解0.15g氢氧化钙,正确但不符合题意;C.30℃恰好饱和的石灰水升温到50℃,溶质的质量分数不变错误,因为升温后有固体析出,符合题意;D.70℃时,饱和石灰水中溶质和溶剂的质量比=0.10g:100g=1:1000,正确但不符合题意。故选C。
2. (海南中考)如图为甲、乙两种固体在水中的溶解度曲线。下列说法正确的是 ( )

A. 甲物质的溶解度比乙物质的大
B. t₂℃时,a g甲溶于100 g水中形成甲的不饱和溶液
C. t₁℃时,甲、乙的饱和溶液中溶质的质量分数都是25%
D. 将t₁℃时甲和乙的饱和溶液升温至t₂℃,仍然都是饱和溶液

A. 甲物质的溶解度比乙物质的大
B. t₂℃时,a g甲溶于100 g水中形成甲的不饱和溶液
C. t₁℃时,甲、乙的饱和溶液中溶质的质量分数都是25%
D. 将t₁℃时甲和乙的饱和溶液升温至t₂℃,仍然都是饱和溶液
答案:
B [解析]比较物质的溶解度时,必须指明温度,A错误;t₂℃时,甲的溶解度大于ag,故ag甲溶于100g水中形成甲的不饱和溶液,B正确;t₁℃时,甲和乙的溶解度相等,均为25g,则该温度下甲和乙的饱和溶液中溶质的质量分数为$\frac{25g}{100g + 25g}\times100\% = 20\%$,C错误;甲的溶解度随温度升高而增大,乙的溶解度随温度升高而减小,将t₁℃时甲和乙的饱和溶液升温至t₂℃时,乙仍为饱和溶液,甲为不饱和溶液,D错误。
3. (泰安中考改编)甲、乙、丙三种固体物质的溶解度曲线如图所示。下列说法正确的是 ( )

A. 10℃时,甲、乙、丙三种物质中,甲的溶解度最大
B. 若甲中混有少量乙,可用蒸发结晶的方法提纯甲
C. 20℃时,甲、乙、丙饱和溶液降温至10℃,甲溶液中析出固体最多
D. 20℃时,向130 g乙的饱和溶液中加入20 g水,所得溶液的溶质质量分数为20%

A. 10℃时,甲、乙、丙三种物质中,甲的溶解度最大
B. 若甲中混有少量乙,可用蒸发结晶的方法提纯甲
C. 20℃时,甲、乙、丙饱和溶液降温至10℃,甲溶液中析出固体最多
D. 20℃时,向130 g乙的饱和溶液中加入20 g水,所得溶液的溶质质量分数为20%
答案:
D [解析]10℃时,三种物质中丙的溶解度最大,A错误;甲的溶解度随温度降低减小的程度比乙大,若甲中混有少量乙,应用降温结晶的方法提纯甲,B错误;丙的溶解度随温度的降低而增大,降温不会析出晶体,甲、乙的溶解度随温度的降低而减小,且甲物质的溶解度受温度的影响比乙大,但题中没有指明饱和溶液的质量,无法比较析出晶体的多少,C错误;20℃时,130g乙的饱和溶液中含有100g水、30g乙,加入20g水后所得溶液的溶质质量分数为$\frac{30g}{150g}\times100\% = 20\%$,D正确。
4. (怀化中考)如图是A、B、C三种固体物质的溶解度曲线,请回答下列问题。
(1)在______℃时,A、B两种物质的溶解度相等。
(2)t₂℃时,A、B、C三种物质中溶解度最大的是______。
(3)若A中含有少量B时,可用______的方法提纯A。
(4)t₂℃时,将35 g A固体加入100 g水中,充分溶解并恢复到原温度后,形成A物质的______(填“饱和”或“不饱和”)溶液,溶液的质量为______g,溶液中溶质的质量分数为______。

(1)在______℃时,A、B两种物质的溶解度相等。
(2)t₂℃时,A、B、C三种物质中溶解度最大的是______。
(3)若A中含有少量B时,可用______的方法提纯A。
(4)t₂℃时,将35 g A固体加入100 g水中,充分溶解并恢复到原温度后,形成A物质的______(填“饱和”或“不饱和”)溶液,溶液的质量为______g,溶液中溶质的质量分数为______。

答案:
(1)t₁
(2)A
(3)降温结晶
(4)饱和 125 20%
[解析]
(1)在t₁℃时,A、B两种物质的溶解度曲线相交于一点,表示该温度条件下两物质的溶解度相等。
(3)A物质的溶解度受温度影响变化较大,B物质的溶解度受温度影响变化较小,若A中混有少量的B时,可用降温结晶的方法提纯A。
(4)t₂℃时,A物质的溶解度为25g,将35gA固体加入100g水中,充分溶解并恢复到原温度后,溶解A的质量为25g,形成t₂℃时A物质的饱和溶液,溶液质量为100g+25g=125g,溶液的溶质质量分数为$\frac{25g}{25g + 100g}\times100\% = 20\%$。
(1)t₁
(2)A
(3)降温结晶
(4)饱和 125 20%
[解析]
(1)在t₁℃时,A、B两种物质的溶解度曲线相交于一点,表示该温度条件下两物质的溶解度相等。
(3)A物质的溶解度受温度影响变化较大,B物质的溶解度受温度影响变化较小,若A中混有少量的B时,可用降温结晶的方法提纯A。
(4)t₂℃时,A物质的溶解度为25g,将35gA固体加入100g水中,充分溶解并恢复到原温度后,溶解A的质量为25g,形成t₂℃时A物质的饱和溶液,溶液质量为100g+25g=125g,溶液的溶质质量分数为$\frac{25g}{25g + 100g}\times100\% = 20\%$。
5. (广东广州七中二模)溶液在生活、生产、科研中具有广泛的用途。如图1是A、B、C三种固体物质的溶解度曲线,下列说法错误的是 ( )

A. t₁℃时,将固体A、B、C各a g分别加入50 g水中,得到两种饱和溶液,则a的取值范围是30≤a<70
B. t₂℃时,取等质量的A、B两种物质的饱和溶液分别蒸发等量的水后,恢复到t₂℃,析出晶体的质量:A<B
C. t₃℃时,A、B、C三种物质溶解度的大小关系是A = B>C
D. 为使图2试管中的饱和C溶液变浑浊,可向烧杯中加入氢氧化钠固体

A. t₁℃时,将固体A、B、C各a g分别加入50 g水中,得到两种饱和溶液,则a的取值范围是30≤a<70
B. t₂℃时,取等质量的A、B两种物质的饱和溶液分别蒸发等量的水后,恢复到t₂℃,析出晶体的质量:A<B
C. t₃℃时,A、B、C三种物质溶解度的大小关系是A = B>C
D. 为使图2试管中的饱和C溶液变浑浊,可向烧杯中加入氢氧化钠固体
答案:
A [解析]t₁℃时,B物质的溶解度是70g,A、C两物质的溶解度均是30g,将固体A、B、C各ag分别加入50g水中,得到两种饱和溶液,则a的取值范围是15≤a<35;t₂℃时,B物质的溶解度大于A物质的溶解度,取等质量的A、B两种物质的饱和溶液分别蒸发等量的水后,恢复到t₂℃,析出晶体的质量:A<B;t₃℃时,A、B、C三种物质溶解度的大小关系是A=B>C;氢氧化钠溶于水放热,C物质的溶解度随温度的升高而减小,为使试管中的饱和C溶液变浑浊,可向烧杯中加入氢氧化钠固体。
6. (连云港中考)KCl和KNO₃的部分溶解度见下表,溶解度曲线见下图。下列说法正确的是 ( )
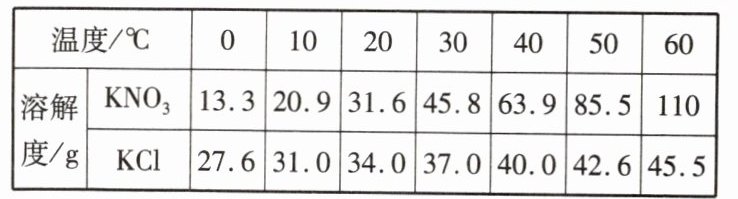
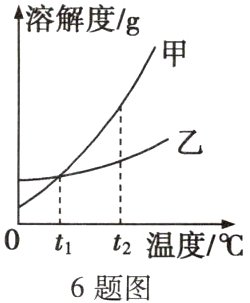
A. 曲线甲代表KCl的溶解度曲线
B. 40℃时KNO₃饱和溶液中KNO₃的质量分数为63.9%
C. t₁的值在20~30之间
D. 将t₁℃时甲和乙的饱和溶液分别升温至t₂℃,溶液中溶质的质量分数:甲>乙


A. 曲线甲代表KCl的溶解度曲线
B. 40℃时KNO₃饱和溶液中KNO₃的质量分数为63.9%
C. t₁的值在20~30之间
D. 将t₁℃时甲和乙的饱和溶液分别升温至t₂℃,溶液中溶质的质量分数:甲>乙
答案:
C [解析]KNO₃的溶解度受温度影响较大,KCl的溶解度受温度影响较小,则曲线乙表示KCl的溶解度曲线,A错误;40℃时KNO₃的溶解度是63.9g,该温度下其饱和溶液的溶质质量分数为$\frac{63.9g}{63.9g + 100g}\times100\%\lt63.9\%$,B错误;20℃时,KCl和KNO₃的溶解度较大的是KCl,30℃时两种物质中溶解度较大的是KNO₃,则两物质溶解度相同时的温度在20~30℃之间,C正确;t₁℃时甲和乙的溶解度相等,该温度下二者饱和溶液的溶质质量分数相等,把t₁℃时甲和乙的饱和溶液分别升温至t₂℃,两物质的溶解度都变大,两溶液都变为不饱和溶液,溶质、溶剂、溶液质量都不变,所以溶质的质量分数也不变,仍然相等,D错误。
查看更多完整答案,请扫码查看


