2025年活动单导学课程高中化学选择性必修第三册苏教版
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2025年活动单导学课程高中化学选择性必修第三册苏教版 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
第84页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
1. 学习教材第101页的“基础实验”,观察乙酸乙酯的制取实验,装置如图所示。

讨论下列问题:
(1) 实验中小心加热的目的是什么?
(2) 浓硫酸的作用是什么?
(3) 饱和 $\mathrm{Na_2CO_3}$ 的作用是什么?能否用 $\mathrm{NaOH}$ 代替 $\mathrm{Na_2CO_3}$?
(4) 长直导管的作用是什么?为什么不能插入液面以下?
(5) 根据化学平衡移动原理设计提高乙酸乙酯产率的方法。

讨论下列问题:
(1) 实验中小心加热的目的是什么?
(2) 浓硫酸的作用是什么?
(3) 饱和 $\mathrm{Na_2CO_3}$ 的作用是什么?能否用 $\mathrm{NaOH}$ 代替 $\mathrm{Na_2CO_3}$?
(4) 长直导管的作用是什么?为什么不能插入液面以下?
(5) 根据化学平衡移动原理设计提高乙酸乙酯产率的方法。
答案:
(1)减少乙酸、乙醇的挥发。
(2)浓硫酸在反应中作催化剂、吸水剂。
(3)饱和$ Na_2 CO_3$可溶解乙醇,除去乙酸,降低乙酸乙酯的溶解度,有利于乙酸乙酯的回收。 不能用$ NaOH$代替$ Na_2 CO_3$,因为乙酸乙酯会在$ NaOH$溶液中发生水解。
(4)长直导管除可以导气外,还起冷凝的作用。不插入液面以下,防止倒吸。
(5)①由于乙酸乙酯沸点比乙酸、乙醇低,因此从反应物中不断蒸出乙酸乙酯,可提高其产率。②使用过量的乙醇,可提高乙酸转化为乙酸乙酯的转化率。③使用浓硫酸作吸水剂,提高乙醇、乙酸的转化率。
(1)减少乙酸、乙醇的挥发。
(2)浓硫酸在反应中作催化剂、吸水剂。
(3)饱和$ Na_2 CO_3$可溶解乙醇,除去乙酸,降低乙酸乙酯的溶解度,有利于乙酸乙酯的回收。 不能用$ NaOH$代替$ Na_2 CO_3$,因为乙酸乙酯会在$ NaOH$溶液中发生水解。
(4)长直导管除可以导气外,还起冷凝的作用。不插入液面以下,防止倒吸。
(5)①由于乙酸乙酯沸点比乙酸、乙醇低,因此从反应物中不断蒸出乙酸乙酯,可提高其产率。②使用过量的乙醇,可提高乙酸转化为乙酸乙酯的转化率。③使用浓硫酸作吸水剂,提高乙醇、乙酸的转化率。
2. 探究乙酸乙酯的性质。
酯类中含酯基:
乙酸乙酯在酸性或碱性条件下能发生水解反应,完成教材【实验2】,观察到什么现象?能得出什么结论?
活动五:了解甲酸、对苯二甲酸的结构与性质
酯类中含酯基:

乙酸乙酯在酸性或碱性条件下能发生水解反应,完成教材【实验2】,观察到什么现象?能得出什么结论?
活动五:了解甲酸、对苯二甲酸的结构与性质
答案:
加蒸馏水的试管中无明显变化,加$5\ mL$稀硫酸的试管中油状的乙酸乙酯体积减小;加$ NaOH$溶液的试管中油状物几乎消失。可得出乙酸乙酯水解需酸或碱作催化剂,在碱性条件下水解程度更大,水解生成的酸在碱性条件下被碱中和,使平衡向正反应方向移动,从而使酯的水解趋于完全。
1. 甲酸的结构与性质
分析图中甲酸的结构式,甲酸中有什么官能团?讨论、预测甲酸有哪些性质?
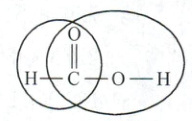
分析图中甲酸的结构式,甲酸中有什么官能团?讨论、预测甲酸有哪些性质?

答案:
甲酸中含有羧基和醛基。有酸的通性,能发生酯化反应,有醛的通性,能与新制的氢氧化铜或银氨溶液反应。
2. 认识对苯二甲酸,了解缩聚反应。
(1) 阅读教材,了解什么是缩聚反应?
(2) 阅读教材第102页“跨学科链接”的内容,了解酯化反应与高分子材料。
世界上产量最大的合成纤维是以对苯二甲酸和乙二醇为原料合成得到的聚对苯二甲酸乙二酯(PET)。试写出生成聚对苯二甲酸乙二酯的化学方程式。
(1) 阅读教材,了解什么是缩聚反应?
(2) 阅读教材第102页“跨学科链接”的内容,了解酯化反应与高分子材料。
世界上产量最大的合成纤维是以对苯二甲酸和乙二醇为原料合成得到的聚对苯二甲酸乙二酯(PET)。试写出生成聚对苯二甲酸乙二酯的化学方程式。
答案:
(1)由有机化合物分子间脱去小分子获得高分子化合物的反应是缩聚反应。

(1)由有机化合物分子间脱去小分子获得高分子化合物的反应是缩聚反应。

查看更多完整答案,请扫码查看


