2025年活动单导学课程高中化学选择性必修第三册苏教版
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2025年活动单导学课程高中化学选择性必修第三册苏教版 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
第20页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
5. 拓展:碳原子的几种杂化轨道形状示意图如下:
(1) 阅读教材第24页“拓展视野”的内容,$\sigma$键与$\pi$键是如何形成的?
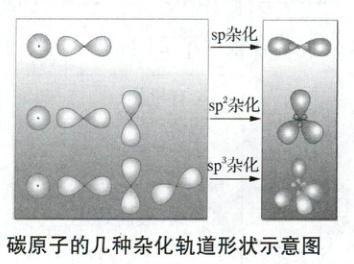
(2) $ sp^3$、$ sp^2$和$ sp$杂化的碳原子分别可以形成多少个$\sigma$键与$\pi$键?
(3) $\sigma$键与$\pi$键哪个更稳定,为什么?
(4) 下表是常见烃分子中碳原子的杂化方式。

各分子中碳原子与其他原子形成的共价键各有哪些类型?分别形成几种?
(1) 阅读教材第24页“拓展视野”的内容,$\sigma$键与$\pi$键是如何形成的?

(2) $ sp^3$、$ sp^2$和$ sp$杂化的碳原子分别可以形成多少个$\sigma$键与$\pi$键?
(3) $\sigma$键与$\pi$键哪个更稳定,为什么?
(4) 下表是常见烃分子中碳原子的杂化方式。

各分子中碳原子与其他原子形成的共价键各有哪些类型?分别形成几种?
答案:
5.(1)沿轨道对称轴方向重叠形成的键叫$\sigma$键。原子中没有参与杂化的p轨道沿对称轴平行的方向重叠形成的键叫$\pi$键。(2)$sp^{3}$杂化的碳原子的轨道上各有一个未成对的电子,可以与4个氢原子的1s轨道沿轨道对称轴方向重叠成键,形成四个等同的$\sigma$键;$sp^{2}$杂化的碳原子3个杂化轨道,可以形成3个$\sigma$键,一个未杂化的p轨道可以沿键轴平行方向形成一个$\pi$键;$sp$杂化的碳原子2个杂化轨道,可以形成2个$\sigma$键,2个未杂化的p轨道可以沿键轴平行方向形成2个$\pi$键。(3)形成$\sigma$键时电子云达到了最大的重叠程度,$\sigma$键比较牢固并且能围绕对称轴自由旋转;形成$\pi$键时,电子云重叠程度比$\sigma$键小,$\pi$键的稳定性比$\sigma$键差。(4)甲烷中碳原子与氢原子形成4个$\sigma$键;乙烯中的1个碳原子与其他原子形成3个$\sigma$键和1个$\pi$键;乙炔中的1个碳原子与其他原子形成2个$\sigma$键和2个$\pi$键;苯分子中的碳原子与氢原子间形成$\sigma$键,碳原子与碳原子间除了形成$\sigma$键外,六个碳原子还共同形成一个环状的大$\pi$键。
查看更多完整答案,请扫码查看


