第29页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
11. 帕拉米韦注射液是我国自主研发的可用于治疗H7N9禽流感的一种药。帕拉米韦的化学式为$C_1_5H_2_8N_4O_4,$下列关于帕拉米韦的叙述正确的是 ( )
A.帕拉米韦由碳、氢、氧、氮四种元素组成
B.帕拉米韦中含有15个碳原子、28个氢原子、4个氧原子和4个氮原子
C.帕拉米韦的相对分子质量为328g
D.使用新药帕拉米韦后,就没有必要再研发新的抗禽流感药物
A.帕拉米韦由碳、氢、氧、氮四种元素组成
B.帕拉米韦中含有15个碳原子、28个氢原子、4个氧原子和4个氮原子
C.帕拉米韦的相对分子质量为328g
D.使用新药帕拉米韦后,就没有必要再研发新的抗禽流感药物
答案:
A
12. 有机物是自然界物质中的一个大家族。
(1)下列物质是生活中常见的物质:① 尿素$[CO(NH_2)_2]、$② 纯碱$(Na_2CO_3)、$③ 阿司匹林$(C_9H_8O_4)、$④ 葡萄糖$(C_6H_1_2O_6),$其中属于有机物的是______(填序号,多选)。
(2)食醋是生活中常用的调味品,其主要成分是乙酸$(CH_3COOH),$在乙酸分子中碳、氢、氧三种原子的个数比是______。
(3)一定质量的某有机化合物X与8g氧气恰好完全反应,生成8.8g二氧化碳和1.8g水。X中各元素的质量比为______。
(1)下列物质是生活中常见的物质:① 尿素$[CO(NH_2)_2]、$② 纯碱$(Na_2CO_3)、$③ 阿司匹林$(C_9H_8O_4)、$④ 葡萄糖$(C_6H_1_2O_6),$其中属于有机物的是______(填序号,多选)。
(2)食醋是生活中常用的调味品,其主要成分是乙酸$(CH_3COOH),$在乙酸分子中碳、氢、氧三种原子的个数比是______。
(3)一定质量的某有机化合物X与8g氧气恰好完全反应,生成8.8g二氧化碳和1.8g水。X中各元素的质量比为______。
答案:
【解析】:
(1) 有机物通常含有碳元素,但排除少数例外(如CO、CO₂、碳酸盐等)。
① 尿素[CO(NH₂)₂]含碳且非例外,属于有机物。
② 纯碱(Na₂CO₃)为碳酸盐,属于无机物。
③ 阿司匹林(C₉H₈O₄)含碳且为典型有机物。
④ 葡萄糖(C₆H₁₂O₆)含碳且为有机物。
答案:①③④
(2) 乙酸(CH₃COOH)的分子式为C₂H₄O₂,碳、氢、氧原子个数比为2:4:2,化简为1:2:1。
答案:1:2:1
(3) 根据质量守恒定律:
二氧化碳中碳的质量:8.8g × (12/44) = 2.4g
水中氢的质量:1.8g × (2/18) = 0.2g
氧的总质量:8.8g(CO₂) + 1.8g(H₂O) - 8g(O₂) = 2.6g
其中,生成物中氧来自X和O₂:
CO₂中氧:8.8g - 2.4g = 6.4g,H₂O中氧:1.8g - 0.2g = 1.6g,总氧8g。
X中氧质量:6.4g + 1.6g - 8g = 0(X中无氧)。
X中C:H质量比为2.4g:0.2g = 12:1。
答案:12:1
【答案】:
(1) ①③④
(2) 1:2:1
(3) 12:1
(1) 有机物通常含有碳元素,但排除少数例外(如CO、CO₂、碳酸盐等)。
① 尿素[CO(NH₂)₂]含碳且非例外,属于有机物。
② 纯碱(Na₂CO₃)为碳酸盐,属于无机物。
③ 阿司匹林(C₉H₈O₄)含碳且为典型有机物。
④ 葡萄糖(C₆H₁₂O₆)含碳且为有机物。
答案:①③④
(2) 乙酸(CH₃COOH)的分子式为C₂H₄O₂,碳、氢、氧原子个数比为2:4:2,化简为1:2:1。
答案:1:2:1
(3) 根据质量守恒定律:
二氧化碳中碳的质量:8.8g × (12/44) = 2.4g
水中氢的质量:1.8g × (2/18) = 0.2g
氧的总质量:8.8g(CO₂) + 1.8g(H₂O) - 8g(O₂) = 2.6g
其中,生成物中氧来自X和O₂:
CO₂中氧:8.8g - 2.4g = 6.4g,H₂O中氧:1.8g - 0.2g = 1.6g,总氧8g。
X中氧质量:6.4g + 1.6g - 8g = 0(X中无氧)。
X中C:H质量比为2.4g:0.2g = 12:1。
答案:12:1
【答案】:
(1) ①③④
(2) 1:2:1
(3) 12:1
13. 甲酸是一种无色、有刺激性气味的液体,有较强的腐蚀性。小科想知道甲酸是否具有酸性,做了如下探究:
滴加蒸馏水 甲酸 A
滴加氯化钠溶液 甲酸 B
滴加紫色石蕊试液 甲酸 C
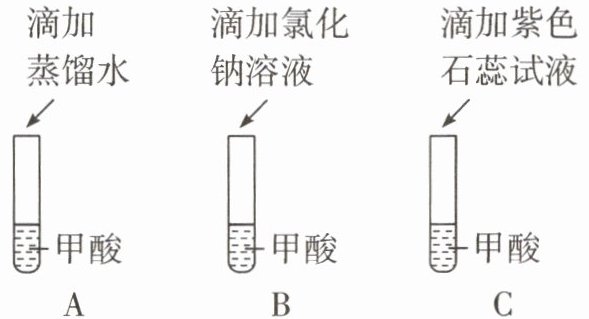
(1)他作出的猜想是“甲酸具有酸性”,实验设计______(填字母)能够检验这一猜想。
(2)如果小科的猜想是正确的,那么甲酸就会像盐酸那样,能与碳酸钠反应,产生______气体。
(3)甲酸(HCOOH)是有机物,浓硫酸能将有机物中的氢元素和氧元素按照水分子中氢原子、氧原子个数比“脱出”生成水,这就是浓硫酸的脱水性。实验室里将甲酸和浓硫酸混合加热进行反应,该反应中甲酸脱水后会生成______气体。
滴加蒸馏水 甲酸 A
滴加氯化钠溶液 甲酸 B
滴加紫色石蕊试液 甲酸 C

(1)他作出的猜想是“甲酸具有酸性”,实验设计______(填字母)能够检验这一猜想。
(2)如果小科的猜想是正确的,那么甲酸就会像盐酸那样,能与碳酸钠反应,产生______气体。
(3)甲酸(HCOOH)是有机物,浓硫酸能将有机物中的氢元素和氧元素按照水分子中氢原子、氧原子个数比“脱出”生成水,这就是浓硫酸的脱水性。实验室里将甲酸和浓硫酸混合加热进行反应,该反应中甲酸脱水后会生成______气体。
答案:
(1)C;
(2)二氧化碳;
(3)一氧化碳。
(1)C;
(2)二氧化碳;
(3)一氧化碳。
14. 某天凌晨,一辆载有苯酚的槽罐车转弯时由于操作不慎发生侧翻,约有10t的苯酚泄漏,空气中弥漫着浓烈的酸臭气味。事发地的下游有许多饮用水的取水口,情况危急。苯酚(化学式为$C_6H_6O)$是一种有毒的物质,对皮肤、黏膜有强烈的腐蚀作用。
(1)现场救护人员必须佩戴呼吸器、穿好防化服的原因是______。
(2)下列事故的处理方法合理的是______(填字母,多选)。
A. 用水冲洗或用泥土填埋
B. 挖隔离沟、铺薄膜以防止扩散,并回收泄漏的苯酚
C. 随时监测附近水源、土壤中的苯酚含量
(3)残余的苯酚用木屑吸附,然后点火燃烧除去。写出苯酚在空气中充分燃烧生成二氧化碳和水的化学方程式:______。
(1)现场救护人员必须佩戴呼吸器、穿好防化服的原因是______。
(2)下列事故的处理方法合理的是______(填字母,多选)。
A. 用水冲洗或用泥土填埋
B. 挖隔离沟、铺薄膜以防止扩散,并回收泄漏的苯酚
C. 随时监测附近水源、土壤中的苯酚含量
(3)残余的苯酚用木屑吸附,然后点火燃烧除去。写出苯酚在空气中充分燃烧生成二氧化碳和水的化学方程式:______。
答案:
(1) 苯酚具有强烈腐蚀性和毒性,挥发后可能通过呼吸道或皮肤接触危害健康
(2) BC
(3) $C_6H_6O + 7O_2 \xrightarrow{点燃} 6CO_2 + 3H_2O$
(1) 苯酚具有强烈腐蚀性和毒性,挥发后可能通过呼吸道或皮肤接触危害健康
(2) BC
(3) $C_6H_6O + 7O_2 \xrightarrow{点燃} 6CO_2 + 3H_2O$
查看更多完整答案,请扫码查看


